1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
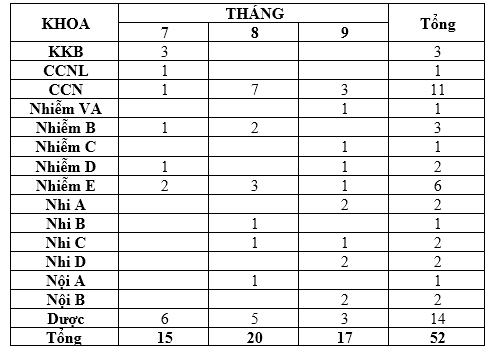
Quý 3-2023 ghi nhận có 52 báo cáo ADR xảy ra tại 15 khoa. Trong đó, khoa Dược báo cáo 14 ca, chủ yếu là bệnh nhân ngoại trú. So với 2 quý trước, báo cáo ADR Quý 3-2023 tăng số khoa và số báo cáo ca, vì có ghi nhận báo cáo ADR của chế phẩm IVIg mới (IMMUGLO). Tháng 9-2023 ghi nhận số ca dị ứng với kháng sinh có xu hướng tăng, đặc biệt ở các khoa nhi và có 01 ca chuyển đổi kháng sinh khi bị dị ứng chưa phù hợp. Khuyến cáo các khoa lâm sàng tiếp tục tăng cường giám sát, theo dõi, xử trí phù hợp khi đổi thuốc (nếu cần hội ý DLS và tham khảo thêm cách thức tiếp cận các trường hợp này ở phần Chuyên Đề - Bản tin dược lâm sàng Quí 1-2020) và báo cáo tác dụng phụ không mong muốn của thuốc gửi về khoa Dược trên phần mềm Ehospital.
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
Khoa Nội A và phòng Điều dưỡng phản hồi sự cố rò rỉ túi dịch NaCl 0.9% thể tích 100ml và 500ml vì hở mối ép túi truyền dịch. Hai sản phẩm có cùng nhà sản xuất là Công ty TNHH DP Allomed-Việt Nam và do Công ty DP Trường Khang phân phối. Khoa dược đã phản ánh với nhà cung ứng và tiếp tục theo dõi chất lượng thuốc tại các kho, khoa lâm sàng. Công ty sản xuất và phân phối đồng ý thay thế các sản phẩm bị lỗi nguyên nhân từ đóng gói.
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 3-2023
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 498 TH nội trú (tăng so với quý 2/2023) và 1853 toa thuốc ngoại trú (tăng 2 lần so với quý 2/2023) do tình hình bệnh tăng. Đơn vị dược lâm sàng thực hiện 370 can thiệp dược lâm sàng chiếm 15,7% trong các hoạt động thường quy của DLS (tăng về số lượng nhưng về tỷ lệ hoạt động thì giảm nhẹ so với Quý 2/2023 là 16.7%). Chủ yếu là các can thiệp hội ý/hội chẩn về thuốc: liều kháng sinh (trong đó có 62 ca vancomycin, tỷ lệ sử dụng vancomycin tăng nhẹ so với Quí 2-2023), phối hợp/lựa chọn kháng sinh và tư vấn về nguy cơ tác dụng bất lợi của thuốc,…và can thiệp trực tiếp khi duyệt nội trú y lệnh hàng ngày. Trong 370 can thiệp có 88.4% là can thiệp trong việc sử dụng thuốc và tăng so với với Quý 2/2023. Trong Quý 3/2023, sự thống nhất ý kiến giữa dược lâm sàng và bác sĩ điều trị giảm nhẹ với quý 2/2023: 97%, có 10 trường hợp không đồng ý chủ yếu ở các khoa khám ngoại trú và nhà thuốc bệnh viện; 01 ca không đồng ý khi điều chỉnh liều kháng sinh trong nội trú.

3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
Toàn bệnh viện đạt 13 tiêu chí về sử dụng thuốc 94% (giảm nhẹ so với Quí 2/2023 là 95%).
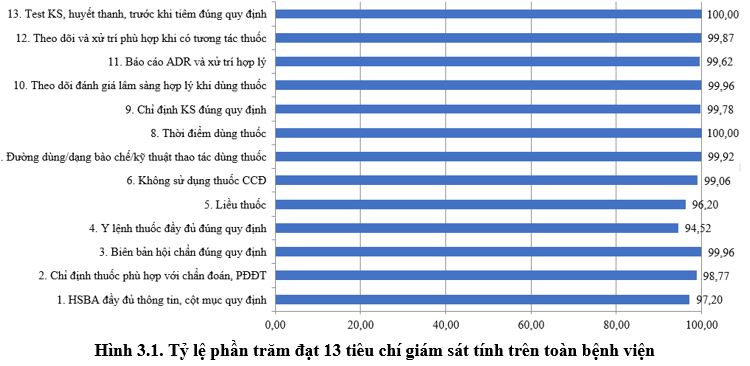
Tiêu chí liều thuốc và y lệnh đầy đủ giảm nhẹ so với Quý 2/2023. Các khoa thuộc Khối Nhi thực hiện các khuyến cáo về liều thuốc được cảnh báo có cải thiện; các khoa hồi sức, đông bệnh (CCNL, CCTE, Nhiễm Việt Anh, và E) cần lưu ý hơn về liều thuốc do tình trạng bệnh nặng kèm thay đổi chức năng gan, thận. Đồng thời, các bác sĩ/điều dưỡng khi nạp y lệnh trên HIS cần chú ý để tránh trùng hoặc sai y lệnh, sai ngày giờ dùng thuốc, ở KKB và KKBYC trong Quý 3-2023 lỗi đánh máy tăng so với Quý 2-2023.


3.2. Khuyến cáo dược lâm sàng:
Quy chế kê đơn:
Khi nạp y lệnh trùng trên hệ thống HIS hoặc đánh nhầm số lượng, tên thuốc, trùng y lệnh; đặc biệt lưu ý khi choàng cử thuốc. Các sai sót này chưa xảy ra và ngăn chặn kịp thời tuy nhiên vẫn lặp lại sai sót trong Quý 3/2023 và tăng nhiều so với quý trước. Khuyến cáo các khoa khám bệnh kiểm tra lại đơn thuốc.
Ví dụ:
• Sai hàm lượng: 09 trường hợp
• Sai số lượng: 09 trường hợp
• Sai tên thuốc: 16 trường hợp
-
Kê đơn nhầm CLORPHENIRAMIN 4mg thành KALI CLORID 500mg.
-
Kê đơn nhầm AZOGET 500mg (AZITHROMYCIN) thành AZOLTEL 400mg (Albendazol).
-
Kê đơn nhầm ENTECAVIR 0,5g thành TENOFOVIR 300mg.
-
Kê đơn nhầm URSODEOXYCHOLIC ACID 250mg thành GINGO BILOBA 80mg.
-
Kê đơn nhầm LIVOSIL thành SILYMARIN cùng hoạt chất – toa viết tay khác máy.
-
Kê đơn nhầm EVICTAL thành VIHACAPS khác hoạt chất.
-
Kê đơn nhầm VASMETIN 8MG (Acrivastine) thành VASTEC 35MR (Trimetazidin).
-
Kê đơn nhầm ESSEROSE (phospholipid đậu nành) thành SOMEXWELL (esomeprazole).
-
Kê đơn nhầm TENOQKAY (TDF) thành TENOQKAY và FIBROFINE 145 (Fenofibrate)
-
Kê đơn nhầm STAVACOR (Pravastatin) thành STADOVAS (Amlodipine).
-
Kê đơn nhầm Collyre EYETOBRIN 0.3% (tobramycin 3%) thành TORAXIM 400mg/50ml (Cefuroxim)
-
Kê đơn nhầm LAMONE (Lamivudin 100mg) thành DINARA (Lamivudin 100mg + Tenofovir 300mg)
-
Kê đơn nhầm ATISYRUP (kẽm sulfat 10mg/5ml) thành ATICIZAL (levocetirizin 2,5mg/5ml)
-
Kê đơn nhầm HASPAN ỐNG (Cao khô lá thường xuân) 5ml thành HASPAN CHAI 80ml
-
Kê đơn nhầm CEFPROZIL 250mg thành CEFUROXIM 250mg
• Trùng hoạt chất: 02 trường hợp
-
Kê đơn URSOBIL 300 và URLIV 300: Acid ursodeoxycholic
-
Kê đơn MELOPOWER và CAMLYHEPATINSOF: L - ornithin L - aspartat
Liều:
- Bệnh nhân chẩn đoán rối loạn tiền đình, Rx betahistine 24mg 1viên x 3 lần/ngày
Theo hướng dẫn của NSX, liều dùng của người lớn 1-2 viên/ngày, không được vượt quá 48 mg/ngày. Khuyến cáo BS điều chỉnh liều: 1viên x 2 lần/ngày.
- BN cao 172cm, nặng 90kg, SCr = 20 umol/L (tương đương ClCr = 600ml/phút theo Cockcroft-Gault), cấy BAL (+) Pseudomonas đa nhạy, chỉ định sử dụng Ciprofloxacin.
Bệnh nhân ARC, khuyến cáo liều Ciprofloxacin IV 400mg q8h.
- BN nhiễm nấm Mucor đã điều trị với Amphot đủ 14 ngày, lâm sàng ổn định. Chuyển sang điều trị củng cố với Posaconazol uống 2 muỗng x 2 lần/ngày (≈10 mL ≈ 400 mg), BN gặp tình trạng bị run giật cơ, nghi do không dung nạp Posaconazol
Theo Uptodate, Posaconazol gây tình trạng đau nhược cơ (3-13%), dị cảm ở tay chân (<5%) và có lạnh run (<20%). Khuyến cáo cân nhắc giảm liều chế độ liều 1 muỗng (≈ 5 mL ≈ 200mg) x 3-4 lần/ngày. Đề nghị thực hiện báo cáo ADR.
- BN bị Sốc nhiễm trùng /B20; Viêm phổi. Hiện Rx Tazopelin liều 4,5g q6h. BN nhẹ cân 35kg < 40kg.
Khuyến cáo liều 100mg/kg (tính theo piperacillin) q8h → 4,5g q8h và truyền kéo dài 3-4 giờ để đảm bảo điều trị.
- BN được chẩn đoán: Sốt rét ác tính do P. falciparum thể thiếu máu nặng - TD sốt rét ác tính thể não. Rx Pyramax 3 viên/ngày và Primaquin 01 liều duy nhất → y lệnh 2,5 viên Primaquin 7,5mg, dài ngày.
Theo Quyết định 3377/QĐ-BYT-Hướng dẫn chẩn đoán và điều trị bệnh Sốt rét năm 2023: Đối với người lớn và trẻ ≥ 15 tuổi trở lên bị sốt rét ác tính do P. falciparum → Rx 04 viên Primaquin 7.5mg một liều duy nhất.
- Mogastic (simethicone 80mg) + Grangel (Al(OH)3 600mg, Mg(OH)2 600mg và simethicone 60 mg )
Theo NSX: Mogastic 80mg/viên: 1 viên x 4 lần/ngày (MAX 6 viên một ngày)
Theo NSX: Grangel gói: 2-4 gói/ngày.
Khuyến cáo khi sử dụng 02 chế phẩm này liều Simethicone MAX là 500/ngày (theo DTGQ 2022)
- BN bị Viêm phổi do vi khuẩn nhạy với Oxacillin hoặc MSSA → Rx Oxacillin IV 2g q6h
Khuyến cáo liều Oxacillin (IV) cho Viêm phổi bởi tác nhân nhạy cảm (MSSA) là 2g q4h.
Sử dụng thuốc:
-
Ca 1: BN 34 tuổi, 60kg, 168 cm. Chẩn đoán: TD NT huyết từ vết thương bàn chân => Rx Vancomycin 1000mg/q8h. Kết quả XN: Ctr=5.1 ug/ml, SCr= 60 umol/L (CrCl= 130.38 ml/phút). AUC/MIC ước tính dưới 400 ug*h/ml. Bệnh nhân đang tăng thanh thải và có nguy cơ không đạt AUC/MIC từ 400-600 ngay cả khi liều >4g/ngày.
-
Ca 2: BN nam 38t, 68kg, 167cm. Chẩn đoán:Nhiễm trùng huyết từ da, AIDS --> Rx Vancomcin LD 1750 mg, MD 1000mg q8h → Kết quả XN: Ctr 3,5 ug/ml, CrCl 105,32 ml/P → Hội chẩn DLS đề xuất đo lại Ctr ở liều tiếp theo → Ctr 6 ug/ml, CrCl 107,99 ml/p. Hiện tại BN Rx Vancomycin 3000mg/ngày, nếu tăng tổng liều > 4g/ngày vẫn có nguy cơ không đạt AUC/MIC mục tiêu
Khuyến cáo chuyển Vancomycin sang chế độ truyền liên tục
- Ca 3: BN suy thận chức năng thận 25.57 mL/phút, đang được điều trị với meropenem 1g q8h. Vấn đề: liều meropenem khuyến cáo đối với mức CrCl của bệnh nhân là 1g q12h hoặc 500 mg q8h. Tuy nhiên, BS đồng ý một phần vì lâm sàng chưa cải thiện, BN tiểu tốt nên muốn duy trì liều hiện tại.
Khuyến cáo BN dù có thể tiểu tốt tuy nhiên chức năng thận đã suy và giảm độ thanh thải. Nếu bác sĩ chưa giảm liều thì cân nhắc tiếp tục đo SCr ngày hôm sau nếu Scr vẫn cao thì cần phải giảm liều KS và đánh giá lại bilan nhiễm trùng, các nguyên nhân khác có thể gây tình trạng lâm sàng chưa cải thiện.
- Ca 4: BN Viêm màng não nấm/ Hội chứng thận hư - Suy thận mạn, cushing do thuốc. Scr = 360umol/l, hiện đang sử dụng Ampholip liều 5mg/kg/ngày và FLuconazol 450mg (chỉnh theo chức năng thận). Sau 3 ngày sử dụng tiểu cầu giảm từ 148 → 71 → 61k/ul, hồng cầu giảm nhẹ 4,3 → 3,9 M/ul và Hbg 12,7 → 11,8g/dl.
Nguy cơ giảm tiêu cầu của Amphotericin B theo y văn (uptodate) khoảng 5%, Fluconazol có ghi nhận báo cáo nhưng tỷ lệ rất hiếm gặp. Hiện cân nhắc nguy cơ ADR giảm tiểu cầu nghi do Amphotericin B.
Cân nhắc kỹ giữa lợi ích /nguy cơ, nhận thấy lợi ích của việc điều trị kháng nấm khuyến cáo tiếp tục điều trị Amphotericin B và theo dõi tiểu cầu mỗi ngày.
- Ca 5: BN Bệnh thận mạn CrCl ~ 24 mL/phút Rx Metformin
Metformin CCĐ ở eGFR <30 mL/phút/1,73m2. Cân nhắc đổi sang insulin hoặc linagliptin
- Ca 6: TD nhiễm nấm huyết T.marneffei. Bệnh nhân bị sốc phản vệ với Amphotericin B → Chuyển sang Ampholip. Thời điểm truyền Ampholip và NaCl là cùng thời điểm 13:00.
Khuyến cáo tiêm truyền Ampholip (pha với Glucose 5% nồng độ từ 1-2mg/ml, tốc độ truyền 2,5mg/kg/giờ và lắc nhẹ mỗi 2 giờ nếu truyền dài hơn 2 tiếng). Truyền NaCl 0,5% trước và sau khi tiêm truyền Ampholid, lưu ý dây truyền riêng hoặc rửa giải bằng Glucose trước khi truyền NaCl 0,9% vì có tương kỵ. Đồng thời, nhắc lại kỹ thuật pha truyền Ampholip cho các điều dưỡng.
- Ca 7: Bệnh nhân bị tăng Na+ huyết, hiện sử dụng Imipenem. Hội ý DLS về dung môi pha thuốc phù hợp.
Khuyến cáo Impenem+Cilastatin có thể được pha trong NaCl 0,9%, Glucose 5% nên trong trường hợp này cân nhắc sử dụng Glucose 5%, tuy nhiên lưu ý thời gian bảo quản và truyền thuốc thích hợp do độ bền vững của các chế phẩm Imipnem khác nhau và ngắn hơn khi pha với Glucose.
- Ca 8: BN có xu hướng tăng nhiều hơn Natri máu từ ngày băt đầu Rx fosfomycin IV dinatri. Hội ý DLS.
Theo tờ HDSD sản phẩm Fosmicin dinatri 2g (IV), chế phẩm có chứa 14.5 mEq Na mỗi gam, cần thận trọng khi sử dụng ở các bệnh nhân cần hạn chế Na đưa vào cơ thể như bệnh nhân cao tuổi, cần giảm lượng Na đưa vào cơ thể do suy tim, suy thận, cao huyết áp,...
Hiện chức năng thận 33ml/phút cần giảm liều còn khoảng 75% liều ban đầu chia mỗi 8-12h, tiếp tục theo dõi xu hướng kết quả Na máu và chức năng thận để xử trí.
- Ca 9: Bệnh nhi 43 tháng tuổi, Rx Mg-B6 3 viên/ngày
Theo NSX: Mg-B6 chống chỉ định cho trẻ <12 tuổi
- Ca 10: BN được cấy BAL: Acinetobacter baumannii, kháng Meropenem, nhạy với Ampicillin/sulbactam, nhạy với Colistin → Rx Ampicillin/sulbactam 6g/24h + Colistin 3MUI/12h. BN có sốt trở lại, giảm 3 dòng tế bào máu → Đã hội chẩn BV truyền máu-huyết học. BN đỏ toàn thân, bong vẩy toàn thân, nghi ngờ theo dõi nhiễm trùng huyết do vi khuẩn gram (+)→ Teicoplainin
Teicoplanin có ADR trên hệ máu là giảm bạch cầu trung tính, giảm tiểu cầu và đã từng được ghi nhận tại bệnh viện. Khuyến cáo theo dõi CTM của BN, chú ý vấn đề giảm 3 dòng tế bào.
- Ca 11: BN, 65kg, 168cm, có chẩn đoán: Nhiễm trùng huyết từ viêm mô tế bào cẳng chân, bàn chân (P) do MSSA và S.pyogenes đa nhạy. Đái tháo đường typ 2, gan nhiễm mỡ, suy thượng thận, GERD. BN viêm mô tế bào, điều trị Piperacilin-tazobactam 9N, Vancomycin 11N, vết thương lành chậm, dự kiến điều trị kháng sinh dài ngày
Đề nghị xuống thang kháng sinh, ngưng vancomycin (đã dùng hơn 10 ngày).
Cân nhắc dùng Piperacillin/tazobactam đủ 10-14 ngày tùy theo tình trạng vết thương và hội ý vi sinh thêm nếu cầnCa 12: BN viêm màng não nấm Cryptococcus điều trị giai đoạn củng cố tăng men gan ALT từ 30 210 nghi ngờ do fluconazole.
- Ca 12: Bệnh nhân 42 kg, 160cm. Chẩn đoán: Hoại tử xương hàm trên nghi do nấm đã phẫu thuật. Rx Amphotericin B 50mg (14N) → Voriconazole uống 200 mg x2 lần/ngày. Hai ngày sau khi dùng Voriconazol có ghi nhận mất ngủ. N7 ghi nhận mất ngủ + ảo giác (nhắm mắt thấy có người đứng quanh nói chuyện) → Giảm liều Voriconazol 100 mg x 2 lần/ngày. BN ngủ ổn hơn, bớt ảo giác.
Voriconazol có ADR gây ảo giác. ADR này phụ thuộc vào nồng độ thuốc, cần hiệu chỉnh liều và ngưng thuốc nếu sau khi giảm liều tác dụng phụ này không giảm. Khuyến cáo đo nồng độ Voriconazol để điều chỉnh.
- Ca 13: BN sốc nhiễm trùng - TD sốc độc tố, cấy sang thương S. pyogenes, Staphylococcus argenteus, Staphylococcus, chưa có KSĐ, đang Rx Meropenem + Linezolide + Clindamycin + Levofloxacin.
BN nặng, theo dõi sốc NT đang dùng Meropenem 4N + Linezolide 4N + Levofloxacin 4N + Clindamycin 3N nghi sốc độc tố. Đề nghị ngưng Clindamycin vì Linezolid có thể bao đươc tác dụng kháng độc tố của vi khuẩn Gram (+), đồng thời giảm áp lực nhiều thuốc cho BN trong khi đợi KQ KSĐ.
- Ca 14: Một số chế phẩm Silymarin cần lưu ý CCĐ:
LIVOSIL, HERGAMIN CCĐ trẻ < 18 tuổi (Theo NSX).
EBLAMIN CCĐ trẻ < 12 tuổi (Theo NSX)
Khuyến cáo đổi thuốc HEPA NIC EXTRA hoặc LIVEMARIN vì NSX không có CCĐ cho trẻ < 18 tuổi.
- Ca 15: BN sơ sinh 12 ngày tuổi, 3.7kg. Chẩn đoán: Uốn ván sơ sinh. Đang Rx Acetylcystein PO để điều trị triệu chứng đàm nhớt.
Theo DTQG, Uptodate và NSX chống chỉ định cho TE < 2 tuổi đối với chỉ định tiêu đàm nhày, và không có chế độ liều phù hơp đối với trẻ < 2 tuổi. Đề nghị đổi thuốc khác có tác dụng tương tự và dùng được cho trẻ < 2 tuổi là Bromhexin. Và nếu sử dụng Acetylcystein thì lưu ý vấn đề BHYT.
- Ca 16: BN nhi được chẩn đoán: Cơn tăng huyết áp cấp cứu --> Nifedipin Retard 20mg 0.5 viên x 2 lần/ngày do bé được nuôi ăn, uống qua sonde dạ dày, phải nghiền nát thuốc
Đây là VIÊN NÉN BAO PHIM TÁC DỤNG KÉO DÀI, khuyến cáo của NSX uống nguyên viên, không được nhai, bẻ hoặc nghiền do đó BS theo dõi sát hiệu quả kiểm soát huyết áp và cân nhắc đổi sang thuốc khác.
- Ca 17: BN Chẩn đoán: Nhiễm giun lươn + Nhiễm giun đũa chó Toxocara / nhiễm trùng tiểu / rối loạn giấc ngủ → kê đơn có ZYX (levocetirizin 5mg) 1 viên x 3 lần/ngày, ANTICLOR (Dexchlorpheniramine 2mg/5ml) 1 ống x 2 lần/ngày → sử dụng VỪA TĂNG LIỀU VỪA PHỐI HỢP 02 thuốc antihistamin.
Đề xuất lựa chọn 1 trong 2 cách: tăng liều hoặc phối hợp theo HDĐT của BV.
- Ca 18: BN được chẩn đoán: ĐTĐ typ 2, VGSV B mạn (HBeAg âm) → Rx Galvus (Vildagliptin 50mg). Kết quả xét nghiệm: AST/ALT 379/193 → 298/204 → 68/96 (ngày 26/08)
Thông tin thuốc: Vildagliptin không khuyến cáo dùng cho BN suy gan, men gan tăng trên 2,5 lần ULN, kể cả bệnh nhân có ALT hoặc AST trước điều trị > 2,5 lần ULN (theo NSX). Men gan đang có xu hướng giảm, tuy nhiên xét nghiệm ngày 26/8 cho giá trị ALT > 2.5ULN → khuyến cáo đo lại men gan.
- Ca 19: BN T/d Nhiễm trùng huyết từ viêm phổi (XQ có tổn thương phổi) → Rx Ceftriaxone 1g x 2 viên q24h (2 ngày), Azithromycin 500 mg x 1 viên q24h → BC máu không tăng, BN đừ, sốt cao, ghi nhận TC có dấu hiệu giảm 141 → 98k/ul → Rx Tazopelin 4,5g q6h. BN bị nổi sẩn da từ tay, cổ, bụng → Truyền chậm TZP và theo dõi sát: ghi nhận nốt hồng ban nổi nhiều hơn khi sốt → Imipenem 500 q6h (3N). Đến N3, ghi nhận hồng ban xuất hiện rải rác, tăng sau mỗi lần truyền Imipenem. Hiện tại BN còn sốt cao liên tục + suy hô hấp tiến triển + XQuang phổi tổn thương tăng thêm. Hội chẩn đề nghị đổi Meropenem.
Khai thác tiền sử BN kỹ, chuyển đổi kháng sinh trong cùng nhóm nếu có dị ứng chưa phù hợp. Tham khảo các loại kháng sinh có nguy cơ dị ứng chéo và hướng xử trí chuyển đổi kháng sinh tại Bản tin DLS Quí 1-2020.
- Ca 20: BN bị nhiễm giun lươn + nhiễm Toxocara canis (giun đũa chó)/ Viêm dạ dày trào ngược thực quản → Rx WINNER (Itoprid 50mg) và MODOM (Domperidon 10mg).
02 thuốc này điều trị triệu chứng tương tự. Đề nghị cân nhắc sử dụng 01 thuốc.
Tương tác thuốc:
BS lưu ý khi có cảnh báo mức độ 5 và có thể chủ động liên hệ DLS hội ý về việc sử dụng chung vì các CẢNH BÁO MỨC ĐỘ 5 LÀ CHỐNG CHỈ ĐỊNH theo Quyết định 5948/QĐ-BYT.

Khuyến cáo Hội đồng thuốc và điều trị - Ban Quản lý sử dụng kháng sinh – Khoa Dược
_ Ban hành Danh mục thuốc chống nhầm lẫn - LASA 2023
_ Ban hành Hướng dẫn pha và bảo quản thuốc tiêm tại Bệnh viện – 2023
Thông tin chi tiết đã gửi bản giấy cho tất các các khoa lâm sàng và cập nhật trên http://emed.bvbnd.vn/.
4. CHUYÊN ĐỀ: TIẾP CẬN THEO DÕI NỒNG ĐỘ THUỐC TRONG MÁU (TDM) ĐỐI VỚI LINEZOLID, VORICONAZOL VÀ VALPROAT ACID:
Viện Pasteur TP. Hồ Chí Minh đã thực hiện đo nồng độ thuốc: LINEZOLID, VORICONAZOL và VALPROAT ACID. Bệnh viện Bệnh Nhiệt đới là bệnh viện tuyến đầu về truyền nhiễm, điều trị các bệnh lý nhiễm trùng do vi khuẩn, nấm và viêm màng não mủ do đó sử dụng khá nhiều 03 loại thuốc này. Dựa vào thực tế yêu cầu lâm sàng, Khoa Dược đã tiến hành xây dựng và triển khai hoạt động TDM Linezolid, Voriconazol và Valproat acid nhằm tăng cường hỗ trợ bác sĩ điều trị, đảm bảo an toàn và sử dụng thuốc hợp lý cho người bệnh sau khi được thông qua bởi Hội đồng thuốc và điều trị của Bệnh viện.
4.1 Linezolid



4.2 Voriconazol


4.3 VALPROIC ACID (VPA):



ThS. DS. Nguyễn Quang Vinh, DS. Mai Phương, DS. Trần Bảo Trâm
TÀI LIỆU THAM KHẢO
-
Enrique Bandín Vilar, A Review of Population Pharmacokinetic Analyses of Linezolid.
-
Lexicomp.
-
Bin Lin, Expert consensus statement on therapeutic drug monitoring and individualization of linezolid.
-
Federico Pea, A 10-Year Experience of Therapeutic Drug Monitoring (TDM) of Linezolid in a Hospital-wide Population of Patients Receiving Conventional Dosing: Is there Enough Evidence for Suggesting TDM in the Majority of Patients?
-
DI & ADR, Giám sát nồng độ thuốc trong huyết thanh ở bệnh nhân nặng với các thuốc kháng sinh, kháng nấm và kháng virus.
-
Medicine – Antimicrobial Therapeutic Drug Monitoring – Guideline . V1.0 Effective: May 2023 Review: June 2025.
-
Bộ Y Tế. Hướng dẫn chẩn đoán và điều trị nhiễm nấm xâm lấn, Ban hành kèm theo Quyết định số 3429/QĐ-BYT, ngày 14 tháng 7 năm 2021.
-
Theuretzbacher, U., Ihle, F. & Derendorf, H. Pharmacokinetic/Pharmacodynamic Profile of Voriconazole. Clin Pharmacokinet 45, 649–663 (2006).
-
H. Ruth Ashbee and others, Therapeutic drug monitoring (TDM) of antifungal agents: guidelines from the British Society for Medical Mycology, Journal of Antimicrobial Chemotherapy, Volume 69, Issue 5, May 2014, Pages 1162–1176.
-
Takesue Y, Hanai Y, Oda K, et al. Clinical Practice Guideline for the Therapeutic Drug Monitoring of Voriconazole in Non-Asian and Asian Adult Patients: Consensus Review by the Japanese Society of Chemotherapy and the Japanese Society of Therapeutic Drug Monitoring. Clin Ther. 2022;44(12):1604-1623. doi:10.1016/j.clinthera.2022.10.005.
-
Paul M., B. Winter’s Basic Clinical Pharmacokinetics, Sixth edition.
-
Applied Clinical Pharmacokinetics, second edition.
-
Clinical Pharmacokinetics.
-
Tseng, Y.-J.; Huang, S.-Y.; Kuo, C.-H.; Wang, C.-Y.; Wang, K.-C.; Wu, C.-C. Safety Range of Free Valproic Acid Serum Concentration in Adult Patients. PLoS ONE 2020, 15 (9), e0238201. https://doi.org/10.1371/journal.pone.0238201.
-
Unbound and Uncharted - Therapeutic Drug Monitoring of Free Valproic Acid in ICU Patients. https://www.neurowiserx.com/2023/05/unbound-and-uncharted-therapeutic-drug.html (accessed 2023-09-24).
-
Maat, M. M. R.; van Leeuwen, H. J.; Edelbroek, P. M. High Unbound Fraction of Valproic Acid in a Hypoalbuminemic Critically Ill Patient on Renal Replacement Therapy. Ann. Pharmacother. 2011, 45 (3), e18. https://doi.org/10.1345/aph.1P308.
-
Free Valproic Acid Assay (Reference — 2013.03.006) – Notice of Assessment.
-
VALPG - Overview: Valproic Acid, Free and Total, Serum. https://www.mayocliniclabs.com/test-catalog/overview/37067#Clinical-and-Interpretive (accessed 2023-08-05).
-
Valproate: Drug information - UpToDate. https://www.uptodate.com/contents/valproate-drug-information?search=axit%20valproic&source=panel_search_result&selectedTitle=1~148&usage_type=panel&kp_tab=drug_general&display_rank=1 (accessed 2023-09-24).
-
Valproic acid poisoning - UpToDate. https://www.uptodate.com/contents/valproic-acid-poisoning?search=acid%20valproic&source=search_result&selectedTitle=2~148&usage_type=default&display_rank=1#H2 (accessed 2023-08-05).