- GHI CHÚ DÀNH CHO CÁC PHÁC ĐỒ KHÁNG SINH
- HƯỚNG DẪN SỬ DỤNG KHÁNG SINH TRẺ EM
- HƯỚNG DẪN SỬ DỤNG KHÁNG SINH NGƯỜI LỚN
- HƯỚNG DẪN LỰA CHỌN KHÁNG SINH CHO VI KHUẨN ĐA KHÁNG SAU KHI CÓ KẾT QUẢ KHÁNG SINH ĐỒ
GHI CHÚ DÀNH CHO CÁC PHÁC ĐỒ KHÁNG SINH
-
Các phác đồ trị liệu kháng sinh được xây dựng trên cơ sở mức độ nhạy cảm của các chủng vi khuẩn gây bệnh thường gặp nhất cho các loại bệnh: nhiễm khuẩn huyết, nhiễm khuẩn hô hấp, nhiễm khuẩn ổ bụng, nhiễm khuẩn đường tiết niệu, dịch báng và nhiễm khuẩn da – mô mềm; với các chủng có cỡ mẫu nhỏ, cần đánh giá tính nhạy cảm với kháng sinh một cách thận trọng.
-
Kháng sinh không có vai trò thay thế cho việc tuân thủ các nguyên tắc Kiểm soát nhiễm khuẩn, Kỹ thuật ngoại khoa…
-
Trường hợp nghi ngờ nhiễm nấm xâm lấn trên những bệnh nhân dùng kháng sinh phổ rộng kéo dài, sốt kéo dài có giảm bạch cầu hạt, các trường hợp ghép tủy, ghép tạng đặc, bệnh nhân suy giảm miễn dịch …, đánh giá theo chỉ số CI (candida index) và cho chỉ định nuôi cấy nấm, hội chẩn để quyết định điều trị kháng nấm sớm.
-
Các loại kháng sinh trong hướng dẫn được xếp theo thứ tự ưu tiên theo mức độ nhạy cảm. Cần ghi chú lý do nếu không sử dụng theo thứ tự.
HƯỚNG DẪN SỬ DỤNG KHÁNG SINH TRẺ EM
ĐIỀU TRỊ VIÊM PHỔI
DỮ LIỆU VI SINH
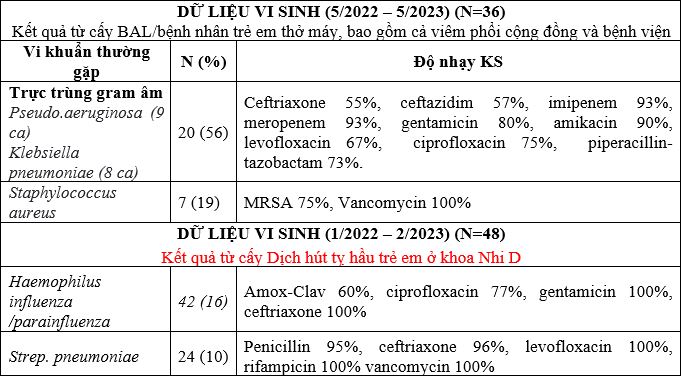
ĐIỀU TRỊ KHỞI ĐẦU
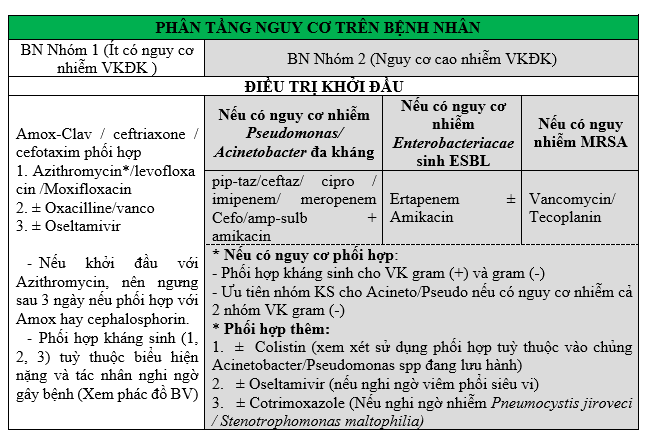
ĐIỀU TRỊ NHIỄM KHUẨN HUYẾT
DỮ LIỆU VI SINH

ĐIỀU TRỊ KHỞI ĐẦU
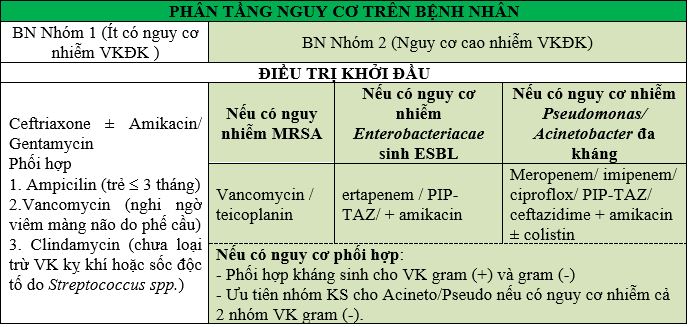
ĐIỀU TRỊ NHIỄM KHUẨN DA VÀ MÔ MỀM
DỮ LIỆU VI SINH

ĐIỀU TRỊ KHỞI ĐẦU

ĐIỀU TRỊ NHIỄM KHUẨN TIẾT NIỆU
DỮ LIỆU VI SINH

ĐIỀU TRỊ KHỞI ĐẦU

HƯỚNG DẪN SỬ DỤNG KHÁNG SINH NGƯỜI LỚN
ĐIỀU TRỊ VIÊM PHỔI
DỮ LIỆU VI SINH
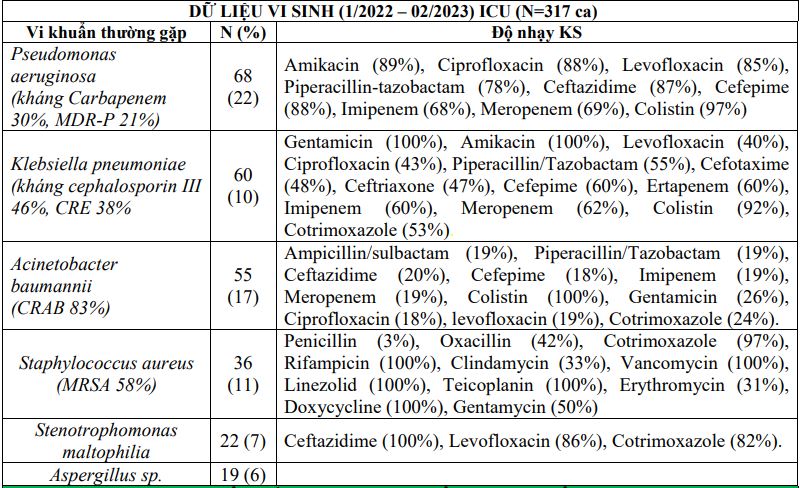
ĐIỀU TRỊ KHỞI ĐẦU

ĐIỀU TRỊ NHIỄM KHUẨN DA VÀ MÔ MỀM
DỮ LIỆU VI SINH

ĐIỀU TRỊ KHỞI ĐẦU

ĐIỀU TRỊ NHIỄM KHUẨN TIẾT NIỆU
DỮ LIỆU VI SINH
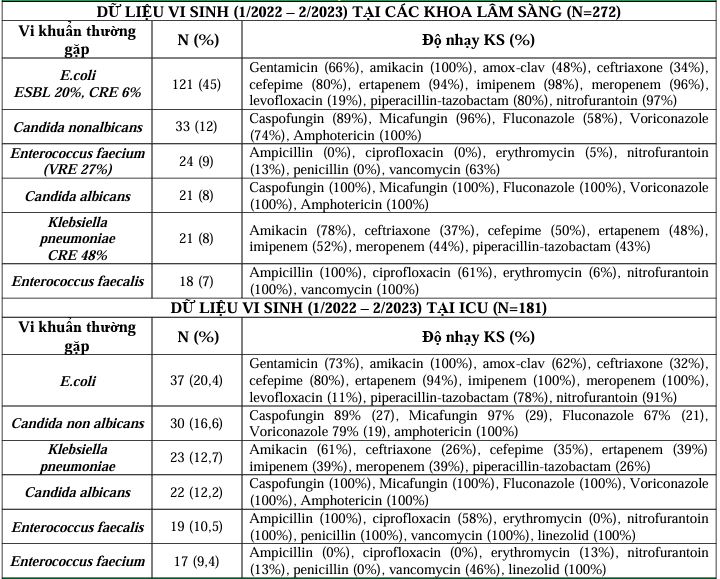
ĐIỀU TRỊ KHỞI ĐẦU
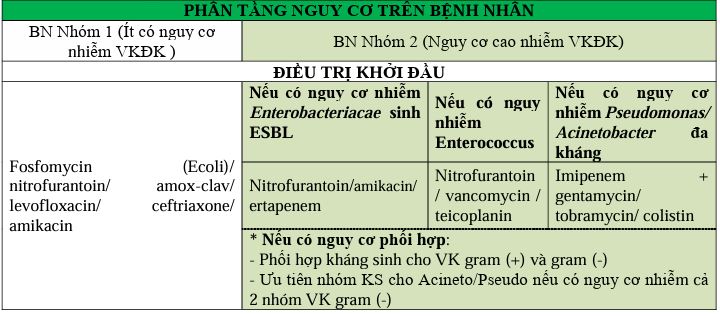
ĐIỀU TRỊ NHIỄM KHUẨN DỊCH BÁNG
DỮ LIỆU VI SINH
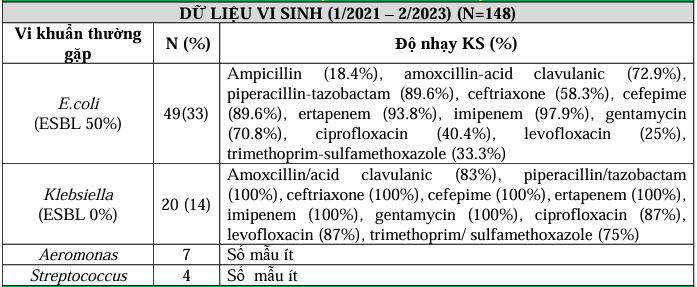
ĐIỀU TRỊ KHỞI ĐẦU

ĐIỀU TRỊ NHIỄM KHUẨN HUYẾT
DỮ LIỆU VI SINH

ĐIỀU TRỊ KHỞI ĐẦU

HƯỚNG DẪN LỰA CHỌN KHÁNG SINH CHO VI KHUẨN ĐA KHÁNG SAU KHI CÓ KẾT QUẢ KHÁNG SINH ĐỒ
Khuyến cáo điều trị kháng sinh kinh nghiệm (KSKN) không được đề cập trong hướng dẫn này. Lựa chọn KSKN cần dựa trên đa yếu tố: mức độ nặng của nhiễm trùng, ổ nhiễm trùng, cơ địa bệnh nhân, dữ liệu quần thể vi sinh tại khoa phòng và độ nhạy cảm của quần thể vi sinh nơi đó. KSKN sẽ được điều chỉnh sau khi có kết quả định danh tác nhân và kháng sinh đồ (KSĐ). Hướng dẫn này tập trung vào lựa chọn kháng sinh (KS) sau khi có kết quả KSĐ.
Chú thích:
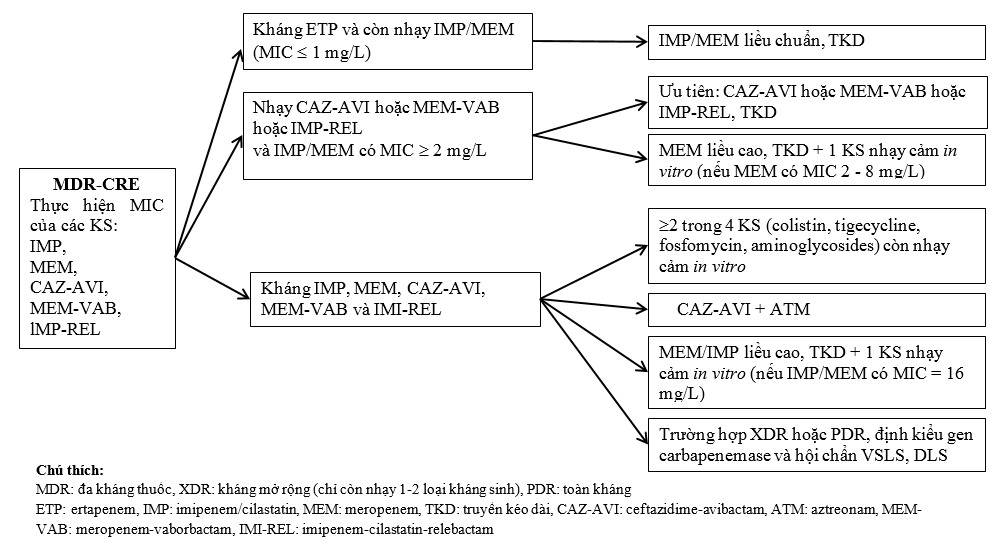
Meropenem liều cao: 2g mỗi 8 giờ truyền tĩnh mạch kéo dài. Imipenem liều cao: 1g mỗi 8 giờ truyền tĩnh mạch kéo dài. Tigecyclin: liều tải 200mg, duy trì 100mg mỗi 12 giờ truyền tĩnh mạch(2,11,12,13,14).
Fosfomycin: 24g/ngày chia 3-4 lần, truyền tĩnh mạch kéo dài(10,15). Truyền kéo dài (TKD) kháng sinh: Liều đầu tiên cần được truyền nhanh trong 30-60 phút.
-
KS nhóm beta-lactam (imipenem, meropenem, ceftazidime-avibactam, meropenem-vaborbactam, imipenem-relebactam): pha với natri chloride 0,9%, TKD >= 3-4 giờ.
-
Fosfomycin: pha với glucose 5%, TKD >= 3-4 giờ.
1. Trực khuẩn Gram âm đường ruột đề kháng Carbapenem (CRE):
a. Bệnh nhân nhiễm trùng nặng hoặc ổ nhiễm trùng nguy cơ cao
Nhiễm trùng nặng: sepsis hoặc sốc nhiễm trùng(2).
Ổ nhiễm trùng nguy cơ cao: ổ nhiễm trùng không phải nhiễm trùng tiểu dưới và nhiễm trùng đường mật đã kiểm soát ổ nhiễm trùng(2).

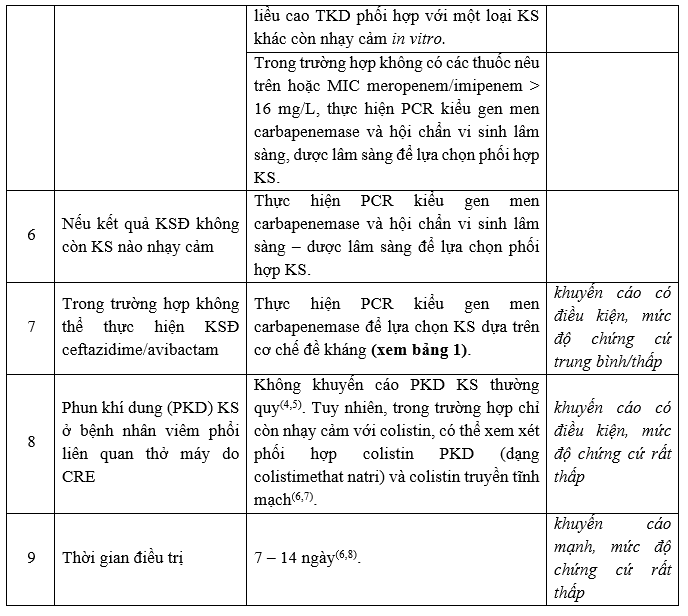
b. Nhiễm trùng tiểu dưới hoặc nhiễm trùng đường mật đã kiểm soát ổ nhiễm trùng


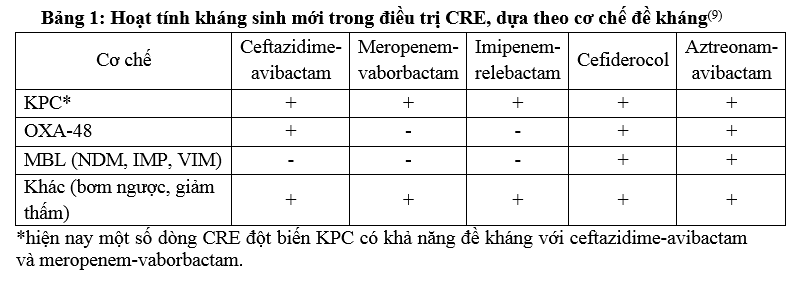
Lưu đồ hướng dẫn lựa chọn kháng sinh cho bệnh nhân nhiễm trùng nặng hoặc ổ nhiễm trùng nguy cơ cao do CRE.
2. Pseudomonas aeruginosa kháng thuốc khó trị (DTR - P. aeruginosa)
a. Định nghĩa: P. aeruginosa không nhạy cảm với tất cả các kháng sinh sau: piperacillin -tazobactam, ceftazidim, cefepim, aztreonam, meropenem, imipenem-cilastatin, ciprofloxacin và levofloxacin (IDSA 2022)
b. Lựa chọn kháng sinh: Kháng sinh được lựa chọn đơn trị liệu:
-
Ưu tiên theo thứ tự: Ceftolozane-tazobactam, ceftazidime-avibactam (nếu đã dùng 1 trong 2 loại này thì không nên dùng tiếp loại còn lại nếu không đáp ứng hay khi cần thay đổi KS).
-
Thuốc thay thế: cefiderocol, imipenem-cilastatin-relebactam, meropenem-vaborbactam.
-
Polymyxins (Colistin) là lựa chọn cuối nếu không có các thuốc trên.
c. Khuyến cáo khác:
-
Ưu tiên dùng đơn trị liệu (ceftolozane - tazobactam, ceftazidime
-
Avibactam, hoặc imipenem - cilastatin - relebactam), việc phối hợp không còn được khuyến cáo do gia tăng nguy cơ phản ứng có hại.
-
Trong trường hợp đề kháng với nhóm kháng sinh ưu tiên, có thể phối hợp một kháng sinh nhóm aminoglycoside (nếu còn nhạy cảm) với một kháng sinh nhóm ưu tiên (nên chọn kháng sinh có MIC thấp nhất).
-
Nếu aminoglycoside không còn nhạy cảm, có thể cân nhắc phối hợp với polymyxin B.
-
Vai trò của kháng sinh đường khí dung trong điều trị nhiễm khuẩn hô hấp do DTR - P. aeruginosa không được khuyến cáo thường quy do còn thiếu dữ liệu lâm sàng.
d. Liều thuốc:
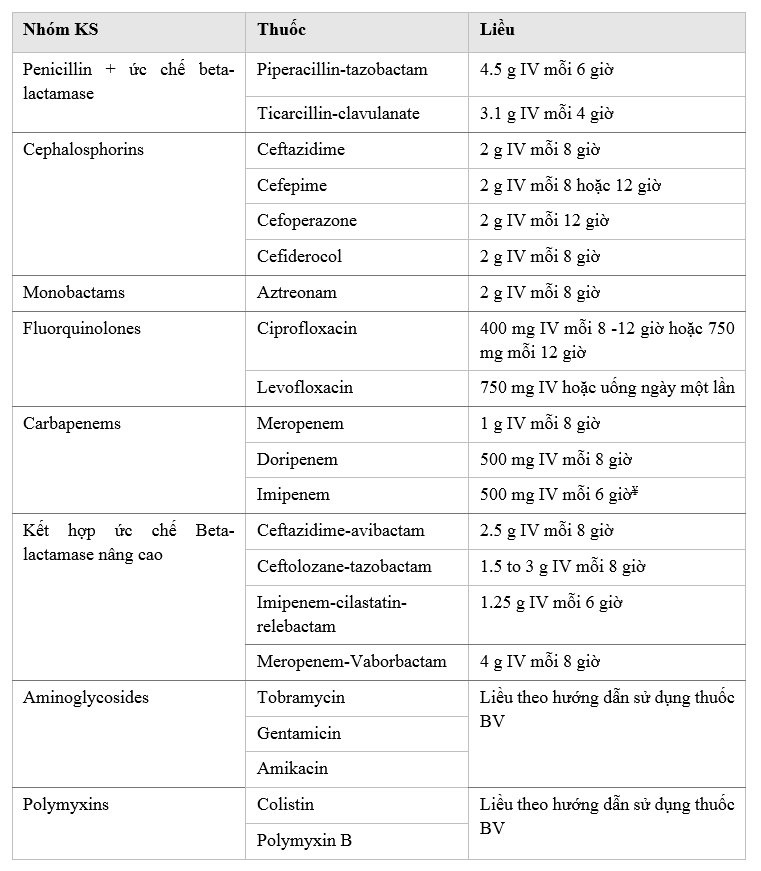
e. Lưu đồ hướng dẫn sử dụng KS cho Pseudomonas aeruginosa kháng thuốc khó trị

3. Acinetobacter baumannii đa kháng
a. Định nghĩa: không nhạy cảm với ít nhất 1 KS trong và trên 3 nhóm KS khác nhau thuộc lớp kháng sinh chọn lựa hàng đầu cho Acinetobacter baumannii như:
-
Ceftazidime hay cefepime, piperacillin-tazobactam hay Ticarcilline-Clavulanic acid, ampicillin-sulbactam, carbapenems (meropenem, imipenem-cilastatin, Doripenem), và fluoroquinolones (ciprofloxacin, Levofloxacin).
-
Aminoglycosides.
-
Trimethoprim-sulfamethoxazole.
b. Lựa chọn kháng sinh:
Nếu chỉ nhiễm Acinetobacter baumannii kháng carbapenem (CRAB)
-
Nhiễm trùng nhẹ: chọn đơn trị liệu, có thể sử dụng các thuốc còn nhạy cảm trong nhóm kháng sinh lựa chọn hàng đầu, ưu tiên ampicillin-sulbactam, cefoperazon-sulbactam liều cao.
-
Nhiễm trùng trung bình và nặng: phối hợp 2 KS còn nhạy ở các lựa chọn:
Ceftazidim (CAZ)/Cefepim (CEF)/Piperacilline-Tazobactam (PIP-TAZ)/ Imipenem-Cilastin (IMP)/Meropenem (MEM) + FQ/ Aminoglycoside.
Fluoroquinolone + Aminoglycoside.
Thay thế: Ceftazidim/Cefepim/Pip-Tazobactam/ Carbapenem/Fluoroquinolone + Polymyxins/dẫn xuất của tetracycline.
Có thể sử dụng Polymyxins + KS có Sulbactam +/- Meropenem liều cao nếu vi khuẩn đề kháng các kháng sinh trên.
Nếu đề kháng hết nhóm KS hàng đầu (Betalactam, Carbapenem, FQ): - Polymyxins (polymyxin B, colistin) và các dẫn xuất của tetracycline (minocycline, tigecycline, eravacycline)
- Thay thế: phối hợp Cefiderocol khi các lựa chọn khác không hiệu quả.
Nếu đề kháng nhóm KS thứ 2 (polymixins, dẫn xuất tetracyclin): Dẫn xuất của tetracycline (minocycline, tigecycline, Eravacycline) + Aminoglycoside.
c. Một số lưu ý
-
Phối hợp thuốc khi nhiễm trùng mức độ trung bình/nặng hay đa kháng, tuy nhiên vẫn chưa có bằng chứng khoa học rõ ràng ưu thế của đa trị so với đơn trị. Nên dùng đơn trị khi nhiễm trùng nhẹ hay nhiễm trùng huyết thứ phát từ đường tiết niệu.
-
Nếu nhiễm khuẩn tiết niệu thì không nên dùng polymyxin B, minocycline và tigecycline đơn trị liệu.
-
Colistin khí dung nên được xem xét phối hợp nếu viêm phổi nặng, tuy nhiên không nên dùng đại trà vì nguy cơ co thắt phế quản.
-
Đường dùng tiêm kênh tủy hay não thất nếu dùng Colistin ở bệnh nhân viêm màng não mủ.
-
Nếu CRAB: có thể sử dụng các thuốc còn nhạy cảm trong nhóm kháng sinh lựa chọn hàng đầu như Ampicillin-Sulbactam, có thể phối hợp Meropenem liều cao truyền kéo dài > 3 giờ.
d. Liều thuốc:
Liều thuốc cho nhóm thuốc chọn lựa theo kinh nghiệm xem trong bảng hướng dẫn liều KS. Liều thuốc cho nhóm KS lựa chọn cho Acinetobacter baumanni đa kháng:
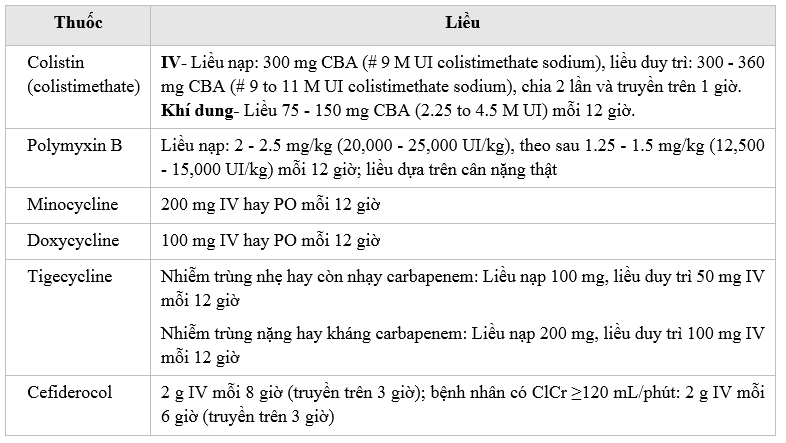
e.Lưu đồ hướng dẫn sử dụng KS cho Acinetobacter baumannii đa kháng:

4. Stenotrophomonas maltophilia
a. Lựa chọn kháng sinh:
Nhiễm trùng nhẹ và có miễn dịch bình thường: chọn đơn trị liệu: - Trimethoprim-sulfamethoxazole hay Minocycline hay Levofloxacin.
-
Nếu kháng thuốc: Tigecycline hay cefiderocol. Nhiễm trùng trung bình và nặng hoặc có suy giảm miễn dịch: chọn đa trị liệu:
-
Trimethoprim-sulfamethoxazole + minocycline/Levofloxacin/cefiderocol
-
Phối hợp các thuốc Minocycline/tigecycline + Levofloxacin/cefiderocol tuỳ thuộc nhạy cảm KS và tình hình thực tế.
b. Một số lưu ý
-
Có thể phối hợp ceftazidime-avibactam và aztreonam nếu các lựa chọn trên không phù hợp.
-
Không dùng ceftazidim điều trị S. maltophilia vì đề kháng tự nhiên.
Tài liệu tham khảo:
-
_Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America Antimicrobial-Resistant Treatment Guidance: Gram-Negative Bacterial Infections. Infectious Diseases Society of America 2022; Version 1.1. Available at https://www.idsociety.org/practice-guideline/amr-guidance/_.
-
Paul M, Carrara E, Retamar P, Tängdén T, Bitterman R, Bonomo RA, de Waele J, Daikos GL, Akova M, Harbarth S, Pulcini C, Garnacho-Montero J, Seme K, Tumbarello M, Lindemann PC, Gandra S, Yu Y, Bassetti M, Mouton JW, Tacconelli E, Rodríguez-Baño J. European Society of Clinical Microbiology and Infectious Diseases (ESCMID) guidelines for the treatment of infections caused by multidrug-resistant Gram-negative bacilli (endorsed by European society of intensive care medicine). Clin Microbiol Infect. 2022 Apr;28(4):521-547. doi: 10.1016/j.cmi.2021.11.025. Epub 2021 Dec 16. PMID: 34923128.
-
Hooton TM, Bradley SF, Cardenas DD, Colgan R, Geerlings SE, Rice JC, et al. Diagnosis, prevention, and treatment of catheter‐associated urinary tract infection in adults: 2009 International Clinical Practice Guidelines from the Infectious Diseases Society of America. Clin Infect Dis 2010;50:625‐63.
-
Kollef MH, Ricard JD, Roux D, Francois B, Ischaki E, Rozgonyi Z, Boulain T, Ivanyi Z, János G, Garot D, Koura F, Zakynthinos E, Dimopoulos G, Torres A, Danker W, Montgomery AB. A Randomized Trial of the Amikacin Fosfomycin Inhalation System for the Adjunctive Therapy of Gram-Negative Ventilator-Associated Pneumonia: IASIS Trial. Chest. 2017 Jun;151(6):1239-1246. doi: 10.1016/j.chest.2016.11.026. Epub 2016 Nov 24. PMID: 27890714.
-
Niederman MS, Alder J, Bassetti M, Boateng F, Cao B, Corkery K, Dhand R, Kaye KS, Lawatscheck R, McLeroth P, Nicolau DP, Wang C, Wood GC, Wunderink RG, Chastre J. Inhaled amikacin adjunctive to intravenous standard-of-care antibiotics in mechanically ventilated patients with Gram-negative pneumonia (INHALE): a double-blind, randomised, placebo-controlled, phase 3, superiority trial. Lancet Infect Dis. 2020 Mar;20(3):330-340. doi: 10.1016/S1473-3099(19)30574-2. Epub 2019 Dec 19. PMID: 31866328.
-
_Andre C. Kalil, Mark L. Metersky, Michael Klompas, John Muscedere, Daniel A. Sweeney, Lucy B. Palmer, Lena M. Napolitano, Naomi P. O'Grady, John G. Bartlett, Jordi Carratalà, Ali A. El Solh, Santiago Ewig, Paul D. Fey, Thomas M. File, Jr, Marcos I. Restrepo, Jason A. Roberts, Grant W. Waterer, Peggy Cruse, Shandra L. Knight, Jan L. Brozek, Management of Adults With Hospital-acquired and Ventilator-associated Pneumonia: 2016 Clinical Practice Guidelines by the Infectious Diseases Society of America and the American Thoracic Society, Clinical Infectious Diseases, Volume 63, Issue 5, 1 September 2016, Pages e61–e111, https://doi.org/10.1093/cid/ciw353_
-
Bao XL, Tao T, Tang N, Wang YZ, Liao XQ, Huang LL, Ji JJ, Chen X. Efficacy and safety of adjunctive nebulized colistin sulfate for multidrug-resistant Gram-negative bacteria pneumonia: a retrospective comparative cohort study. Ann Palliat Med. 2022 Sep;11(9):2939-2951. doi: 10.21037/apm-22-984. PMID: 36217623.
-
Sy CL, Chen PY, Cheng CW, Huang LJ, Wang CH, Chang TH, Chang YC, Chang CJ, Hii IM, Hsu YL, Hu YL, Hung PL, Kuo CY, Lin PC, Liu PY, Lo CL, Lo SH, Ting PJ, Tseng CF, Wang HW, Yang CH, Lee SS, Chen YS, Liu YC, Wang FD. Recommendations and guidelines for the treatment of infections due to multidrug resistant organisms. J Microbiol Immunol Infect. 2022 Jun;55(3):359-386. doi: 10.1016/j.jmii.2022.02.001. Epub 2022 Mar 16. PMID: 35370082.
-
_Vidal-Cortés, P.; Martin-Loeches, I.; Rodríguez, A.; Bou, G.; Cantón, R.; Diaz, E.; De la Fuente, C.; Torre-Cisneros, J.; Nuvials, F.X.; Salavert, M.; Aguilar, G.; Nieto, M.; Ramírez, P.; Borges, M.; Soriano, C.; Ferrer, R.; Maseda, E.; Zaragoza, R. Current Positioning against Severe Infections Due to Klebsiella pneumoniae in Hospitalized Adults. Antibiotics 2022, 11, 1160. https://doi.org/10.3390/antibiotics11091160_
-
Ruiz Ramos J, Salavert Lletí M. Fosfomycin in infections caused by multidrug-resistant Gram-negative pathogens. Rev Esp Quimioter. 2019 May;32 Suppl 1(Suppl 1):45-54. PMID: 31131592; PMCID: PMC6555168.
-
Zha L, Pan L, Guo J, French N, Villanueva EV, Tefsen B. Effectiveness and Safety of High Dose Tigecycline for the Treatment of Severe Infections: A Systematic Review and Meta-Analysis. Adv Ther. 2020 Mar;37(3):1049-1064. doi: 10.1007/s12325-020-01235-y. Epub 2020 Jan 31. PMID: 32006240; PMCID: PMC7223407.
-
Leng B, Yan G, Wang C, Shen C, Zhang W, Wang W. Dose optimisation based on pharmacokinetic/pharmacodynamic target of tigecycline. J Glob Antimicrob Resist. 2021 Jun;25:315-322. doi: 10.1016/j.jgar.2021.04.006. Epub 2021 May 4. PMID: 33957288.
-
_Geng, Ting-Ting MM; Xu, Xin MM; Huang, Man MD*. High-dose tigecycline for the treatment of nosocomial carbapenem-resistant Klebsiella pneumoniae bloodstream infections: A retrospective cohort study. Medicine: February 2018 - Volume 97 - Issue 8 - p e9961. doi: 10.1097/MD.0000000000009961_
-
Chen Z, Shi X. Adverse events of high-dose tigecycline in the treatment of ventilator-associated pneumonia due to multidrug-resistant pathogens. Medicine (Baltimore). 2018 Sep;97(38):e12467. doi: 10.1097/MD.0000000000012467. PMID: 30235740; PMCID: PMC6160260.
-
Antonello RM, Di Bella S, Maraolo AE, Luzzati R. Fosfomycin in continuous or prolonged infusion for systemic bacterial infections: a systematic review of its dosing regimen proposal from in vitro, in vivo and clinical studies. Eur J Clin Microbiol Infect Dis. 2021 Jun;40(6):1117-1126. doi: 10.1007/s10096-021-04181-x. Epub 2021 Feb 18. PMID: 33604721; PMCID: PMC8139892.
-
Bassetti M, Graziano E, Berruti M, Giacobbe DR. The role of fosfomycin for multidrug-resistant gram-negative infections. Curr Opin Infect Dis. 2019 Dec;32(6):617-625. doi: 10.1097/QCO.0000000000000597. PMID: 31567411.
-
_Infectious Diseases Society of America Guidance on the Treatment of AmpC β-lactamase-Producing Enterobacterales, Carbapenem-Resistant Acinetobacter baumannii, and Stenotrophomonas maltophilia Infections. https://www.idsociety.org/practice-guideline/amr-guidance-2.0/_.
-
_Infectious Diseases Society of America 2022 Guidance on the Treatment of Extended-Spectrum β-lactamase Producing Enterobacterales (ESBL-E), Carbapenem-Resistant Enterobacterales (CRE), and Pseudomonas aeruginosa with Difficult-to-Treat Resistance (DTR-P. aeruginosa). https://www.idsociety.org/practice-guideline/amr-guidance/_
-
Zeina A Kanafani, Souha Kanj . Acinetobacter infection: Treatment and prevention. Uptodate Oct 2022
-
Souha S Kan. Principles of antimicrobial therapy of Pseudomonas aeruginosa infections. Uptodate Aug 2022
-
Sarah S Lewis, Aimee Zaas. Stenotrophomonas maltophilia. Uptodate Oct 2022