- 1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
- 2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
- 3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 1-2021
- 4. CHUYÊN ĐỀ: ECMO - KỸ THUẬT MỚI ĐẦY TRIỂN VỌNG VÀ NHỮNG THÁCH THỨC TRONG SỬ DỤNG THUỐC.
- 4.1. Tổng quan về ECMO [1, 12, 15]
- 4.2. Ảnh hưởng của quá trình ECMO trên PK/PD của thuốc [1, 2, 4, 5, 6, 7, 8, 9, 10, 13]
- 4.2.1. Yếu tố đặc tính của hệ thống ECMO [2, 4, 5, 6, 7, 8, 9]
- 4.2.2. Yếu tố đặc tính của thuốc [2, 3, 4, 5, 6, 7, 8, 9, 13]
- 4.2.3. Yếu tố tình trạng sinh lý bệnh của người bệnh [1, 3, 5, 10]
- 4.3. Chế độ liều hiệu chỉnh của một số thuốc thường sử dụng trong quá trình ECMO [3, 10, 11, 14]
1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
Quý 1-2021 ghi nhận có 30 báo cáo ADR xảy ra ở 13 khoa. So với Quý 4-2021 (39 báo cáo), số lượng báo cáo ADR Quý 1-2021 (30 báo cáo) giảm nhưng khá tương đồng với cùng kỳ năm 2020 (Quý 1-2020 có 28 báo cáo). Tăng cường báo cáo phản ứng có hại của thuốc, đặc biệt tại các khoa CCNL (thực tế lâm sàng có xuất hiện ADR tuy nhiên chưa nhận được báo cáo từ khoa).
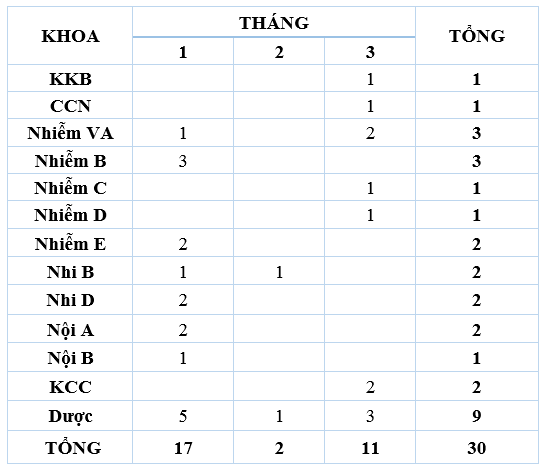
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
không có
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 1-2021
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 255 HSBA nội trú và 834 toa thuốc ngoại trú (gần tương đương so với Quý 4-2020 là 266 HSBA, 833 toa thuốc) tăng so với cùng kỳ năm 2020. Tuy nhiên, đơn vị dược lâm sàng thực hiện 358 trường hợp hội ý/hội chẩn với các khoa lâm sàng trong quá trình điều trị tăng so với Quý 4/202020 (234 TH). Chủ yếu là hội chẩn về liều kháng sinh (vancomycin 107TH, aminoglycosid 7TH, colistin 5TH), phối hợp kháng sinh và tư vấn về nguy cơ tác dụng bất lợi của thuốc,…và can thiệp trực tiếp khi duyệt nội trú y lệnh của khoa lâm sàng hàng ngày.
Bên cạnh đó, đơn vị dược lâm sàng thực hiện 406 (tăng so với Quý 4/2020 là 311TH) can thiệp trong lúc giám sát 1447 HSBA/toa thuốc của bác sỹ (khoảng 28%). Trong đó, có 92% trường hợp được thực hiện kịp thời chủ yếu là các can thiệp chỉnh liều và thông tin thuốc (giảm so với quý 4-2020 (97%); cần tăng cường hoạt động đi buồng và kiểm HSBA tại khoa lâm sàng. Trong Quý 1/2021, sự thống nhất ý kiến giữa dược lâm sàng và bác sĩ điều trị vẫn duy trì 99%, có 03 trường hợp đồng ý một phần về liều thuốc.
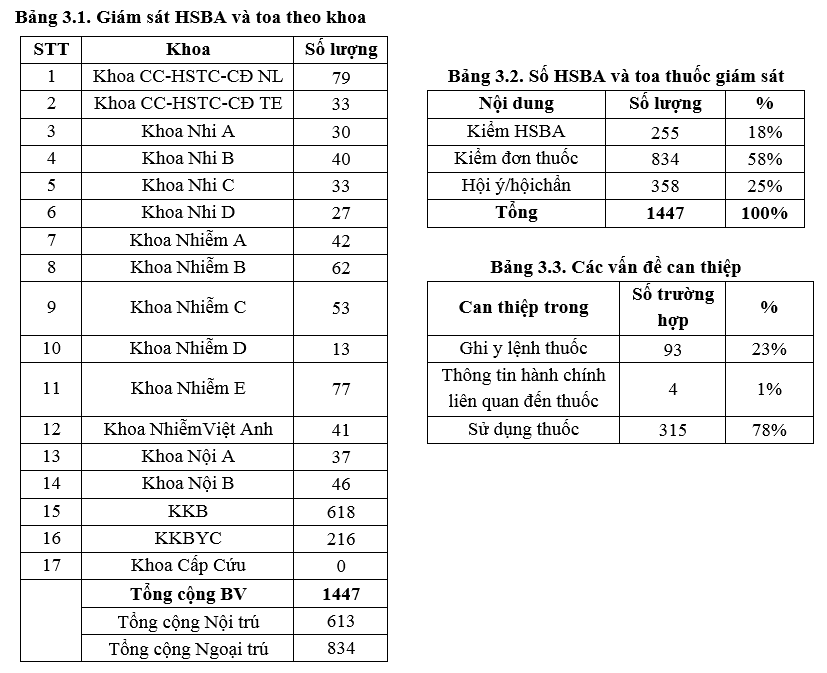
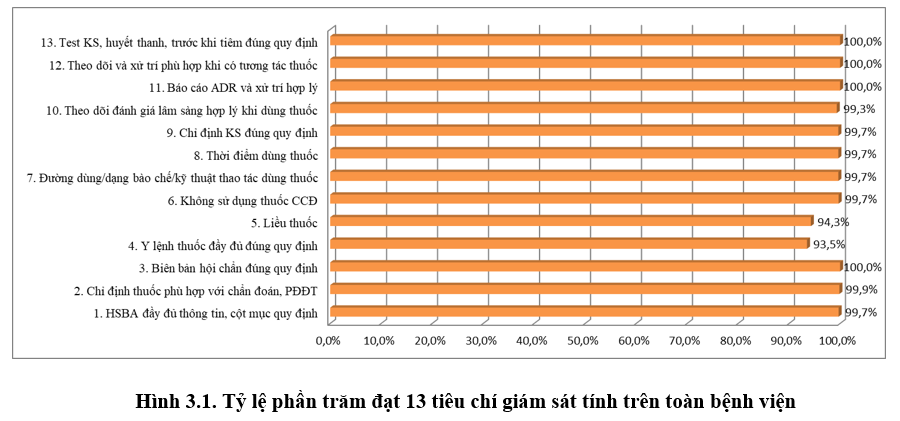
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
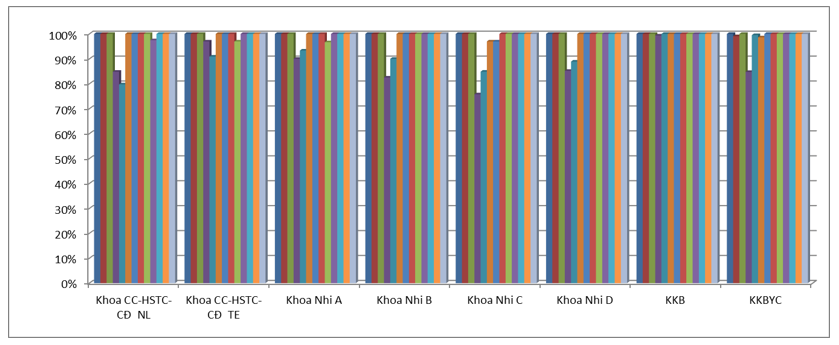
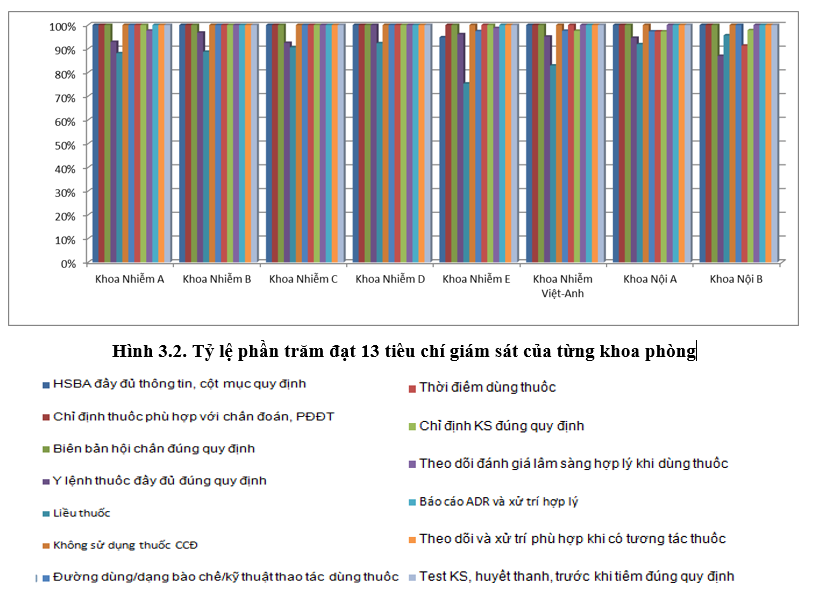
Toàn bệnh viện đạt 13 tiêu chí về sử dụng thuốc > 93% (Quý 4/2020 là 92%).
Tiêu chí liều thuốc và y lệnh đầy đủ ở một số khoa Nhi và Nội-Nhiễm người lớn có tăng dao động khoảng 75-85%, cải thiện nhiều so với Quý 4/2020. Các khoa thuộc Khối Nhi thực hiện tốt các khuyến cáo về liều thuốc được cảnh báo từ Quý 4-2020, tuy nhiên vẫn cần lưu ý liều một số thuốc mới cho đối tượng trẻ em tùy theo tuổi và cân nặng; các thông tin chống chỉ định về độ tuổi và PCNT. Đồng thời, các bác sĩ khi nạp y lệnh trên HIS cần chú ý để tránh trùng hoặc sai y lệnh, sai ngày giờ dùng thuốc
3.3. Khuyến cáo dược lâm sàng:
Quy chế kê đơn:
-
Nhập sai số lượng (KKBYC: 12 đơn thuốc; KKB: 4 đơn thuốc; CCNL, Nhiễm B, C, E; Nhi B, Nội B). Sai tên thuốc (KKB: 7 đơn thuốc, KKBYC: 4 đơn thuốc, CCTE, Nội B). Sai hàm lượng (KKBYC: 6 đơn thuốc), sai liều (KKBYC: 3 đơn thuốc, Nội A, Nội B). Trùng y lệnh (CCNL, Nhiễm A và C, Nội B, Khoa Nhi). Sai ngày/giờ dùng thuốc (Nhi B)
-
Cần ghi rõ chẩn đoán theo mã ICD tương ứng với thuốc chỉ định (đặc biệt: Thuốc PPIs, Vitamin B1 liều cao, Lovenox liều điều trị,…)
-
Kê đơn thuốc trùng các hoạt chất sau: (KKBYC) Lưu ý khi đánh máy và kê toa: Zyx (Levocetirizin 5mg) và Halez (Levocetirizin 5mg)
-
Lưu ý đánh số thứ tự, ngày dùng thuốc đúng quy định gây nghiện (CCNL). Ký rõ họ tên khi sửa y lệnh (CCNL, …).
-
Alpha chymotrypsin: Chỉ định: sưng, phù nề sau chấn thương, bỏng. Vì vậy việc sử dụng cho các chỉ định khác như viêm họng… KHÔNG được BHYT chi trả.
Liều:
- Khuyến cáo NSX Sovalimus 0.1%: Chống chỉ định TE < 15 tuổi
-> Sử dụng Sovalimus 0.03% (Tacrolimus 0.03%) cho trẻ < 15 tuổi
- Khuyến cáo chế phẩm KHÔNG sử dụng cho trẻ < 6 tuổi (Theo NSX)
• Zidocin (Metronidazol 125mg + Spiramycin 75.000 IU)
• Calcical (calci glycerophosphat 0.456g+magnesi gluconat 0.426g)
- BN 22 tuổi, ∆: viêm phổi, cấy BAL (+) MSSA. Rx: Oxacillin IV 2g x 4 lần/ngày.
-> Liều Oxacillin cho MSSA trong áp xe não, viêm xương, viêm phổi, NTH: Oxacillin IV 2g x 6 lần/ngày (Uptodate).
- BN 38 tuổi, ∆: Herpes môi. Rx: Aciclovir PO 800mg x 2 lần /ngày
-> Liều Aciclovir khuyến cáo HSV da niêm: 200mg x 4 - 5 lần/ngày hoặc 400 mg q8 – 12h
- Liều khuyến cáo Cotrim điều trị Stenotrophomonas maltophila ->
15 mg/kg/ngày chia 3 lần (tương ứng 2 viên x3 lần/ngày) (Uptodate).
-
Fostervita: 1 viên/ngày
-
Fexofenadin 180mg: 1 viên/ngày
-
Bioflora 100mg: Người lớn và trẻ em: 2 gói mỗi ngày, chia làm 2 lần
Nystatin:
• Nhiễm nấm Candida đường ruột, thực quản: 100.000 - 500.000 UI q6h
• Nhiễm nấm Candida niêm mạc miệng:
Trẻ sơ sinh: 100.000 UI q6h hoặc 50.000 UI mỗi bên miệng q6h
Trẻ nhũ nhi: 200.000 UI q6h hoặc 100.000 UI mỗi bên miệng q6h
Trẻ em: 400.000-600.000 UI q6h
Racecadotril: TE trên 3 tháng tuổi, liều: 1.5 mg/kg x 3 lần/ngày. Max 7 ngày.
• Trẻ < 9kg: 10 mg/lần x 3 lần/ngày
• Trẻ 9-13kg: 20 mg/lần x 3 lần/ngày
• Trẻ 13 - 27kg: 30 mg/lần x 3 lần/ngày
• Trẻ > 27kg: 60 mg/lần x 3 lần/ngày.
• NL: Bắt đầu với 100 mg, có thể lên tới 3 lần/ngày.
Notired và Fatig
• Trẻ em 6 - 15 tuổi: 1 viên hoặc ống/ngày
• Người lớn: 2 - 3 viên hoặc ống/ngày
Decolic gói (Trimebutin 24mg). Liều khuyến cáo NSX
• Người lớn: 3 gói/lần, ngày 3 lần.
• Trẻ em từ 5 tuổi trở lên: 2 gói/lần, ngày 3 lần.
• Trẻ em dưới 5 tuổi: 4,8 mg/kg/ngày, chia làm 3 lần .
Kẽm gluconat (BOSUZINC)
• Bổ sung kẽm: 1/2 - 1 gói/lần x 1 - 2 lần/ngày
• Điều trị thiếu kẽm: 1 gói /lần x 2 lần/ngày. Nên giảm liều khi triệu chứng cải thiện.
Các chỉ định khác không phải là tiêu chảy nhiễm trùng khuyến cáo sử dụng liều 0.5-1 mg/kg/ngày. Liều kẽm nguyên tố theo tuổi:
• TE 4-8 tuổi: 5mg ( ~ 35mg kẽm gluconat)
• TE 9-13 tuổi: 8mg ( ~ 56mg kẽm gluconat)
NL và TE từ 14 tuổi: 11mg ( ~ 77mg kẽm gluconat)
Sử dụng thuốc kháng Histamin H1 cho PNCT:
-
Theo DTQG 2018 Chlorpheniramine: Chỉ dùng cho người mang thai khi thật cần thiết. Dùng thuốc trong 3 tháng cuối của thai kỳ có thể dẫn đến những phản ứng nghiêm trọng (như cơn động kinh) ở trẻ sơ sinh.
-
Theo khuyến cáo Uptodate, Drug during Prenancy and Lactation; Drug in Prenancy and Lactation : Chlorpheniramine, Loratidin, Cetirizine có thể sử dụng cho PNCT nếu có chỉ định.
• Theo Uptodate: Kháng Histamin H1 thế hệ 2 được cân nhắc trước. (do thế hệ 1 có thể ảnh hưởng đến hô hấp và an thần trẻ mới sinh).
• Theo Drug during Prenancy and Lactation; Drug in Prenancy and Lactation: Kháng Histamin H1 thế hệ 1 được cân nhắc trước. (có thể thay thế bằng Loratidin và Cetirizin ngoại trừ tam cá nguyệt thứ 1).
-> BN thai 35 tuần, chẩn đoán Thủy đậu, cân nhắc Loratidin hoặc Cetirizin
LASA
-
Anticlor 2mg (Dexchlorpheniramin) Liều chuẩn: 2mg/lần. Tránh nhầm lẫn với Chlorpheniramin 4mg.
-
Pulmicort 500MCG/2ML 0,5mg/2ml hàm lượng budesonide là 0,5mg/ống.
-
Pulmicort 0,5mg/ml; ống 2ml hàm lượng budesonide là 1mg/ống.
-
Clindamycin – Hamehl 150mg/ml, ống 4ml HÀM LƯỢNG 600MG/ỐNG
Cách pha và đường dùng
- Methylprenisolon Sopharma: Thuốc theo kết quả thầu SYT 2020 (không có ống nước pha tiêm kèm theo như trong tờ HDSD của thuốc).
Hoàn nguyên: Methylprednisolon 40 mg + 1 ml nước cất pha tiêm
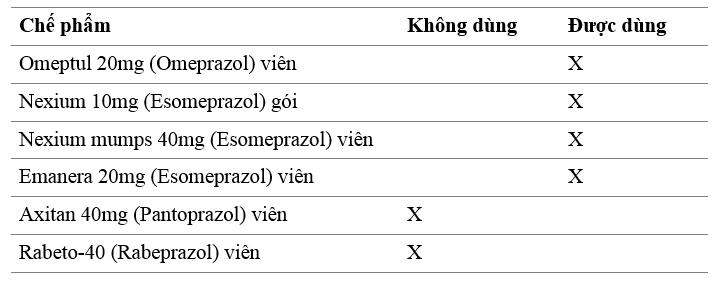
- Các chế phẩm thuốc PPI có tại bệnh viên dung được qua sonde dạ dày:
Tương tác thuốc:
-
Trong Quý 1-2021, số can thiệp các nguy cơ tương tác thuốc giảm nhiều so với cùng kỳ năm 2020, do số lượng bệnh giảm và các pDDI lặp lại khá nhiều, các bác sĩ đã có những điều chỉnh trên lâm sàng (nhưng hệ thống chỉ ghi nhận pDDI) 240 TH/1193 pDDIs, chiếm 20%, và can thiệp chính trên pDDI mức 4-5; chủ yếu là tư vấn và hướng dẫn người bệnh ngoại trú, điều chỉnh y lệnh khi duyệt toa nội trú (giảm so với Quý 4/2020 là gần 30%).
-
Các pDDI mức độ 5 là 7 ca: có tăng so với Quý 4-2020 và đã được cảnh báo + can thiệp. Chưa thấy tác dụng nguy cơ xảy ra thực trên người bệnh. Tuy nhiên, cần tích cực giám sát can thiệp để giảm các pDDI này trong thời gian tới.

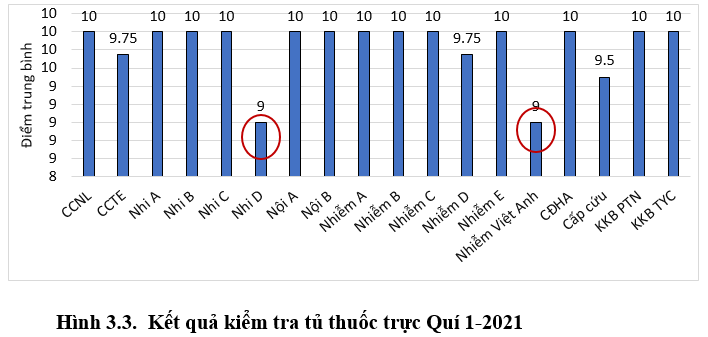
Báo cáo kiểm tra Tủ thuốc trực và đề xuất:
-
Cập nhật nhãn thuốc mới (ghi đúng tên thuốc, nồng độ-hàm lượng).
-
Thuốc viên lẻ không còn nguyên vỉ lưu ý khi cắt thuốc chừa lại phần số lô-HSD / bổ sung nhãn phụ ghi rõ thông tin số lô-HSD.
-
Ưu tiên sử dụng các thuốc có hạn dùng đến ngày 30/09/2021.
-
Cập nhật số lượng - số lô - HSD Thuốc gây nghiện - thuốc hướng thần giữa thực tế và phần mềm FPT.
-
Theo dõi và ghi nhận tO tủ thuốc trực / tủ lạnh, độ ẩm tủ thuốc trực ký tên đầy đủ người thực hiện và người kiểm tra (tránh để tình trạng tủ lạnh bị đóng tuyết).
4. CHUYÊN ĐỀ: ECMO - KỸ THUẬT MỚI ĐẦY TRIỂN VỌNG VÀ NHỮNG THÁCH THỨC TRONG SỬ DỤNG THUỐC.
4.1. Tổng quan về ECMO [1, 12, 15]
ECMO – Extracopereal Membrane Oxygenation được hiểu là kỹ thuật hỗ trợ tim phổi nhân tạo tạm thời (trung bình từ 1-30 ngày) bằng hệ thống máy thực hiện oxy hóa ở màng ngoài cơ thể. Đây là phương pháp sử dụng tuần hoàn và trao đổi oxy ngoài cơ thể nhằm hỗ trợ chức năng sống ở những trường hợp đe dọa tính mạng, suy tuần hoàn hoặc suy hô hấp nặng, như tổn thương phổi nặng do nhiễm trùng, hoặc sốc tim sau nhồi máu cơ tim cấp [1, 12]. Hiện còn được gọi là ECLS (Extracorporeal Life Support).

ECMO được coi là một tiến bộ khoa học trong thập kỷ 90. Khởi đầu từ 1930, khi JH Gibbon chế tạo được máy tim phổi nhân tạo và áp dụng lần đầu tiên ở ca mổ tim vào năm 1953. Đến năm 1956, GHA Clowes Jr. chế tạo được màng trao đổi oxy, và sau đó là sự phát triển chất liệu màng Silicone của K Kammermeyer vào năm 1957, từ đó mở ra nhiều triển vọng cho ECMO. Và đánh dấu bằng ca ECMO đầu tiên thành công ở người lớn do JD Hill thực hiện năm 1972 và ca trẻ sơ sinh đầu tiên ECMO thành công được báo cáo năm 1976 bởi Bartlette và công sự. Năm 1989, tổ chức ELSO (The Extracorporeal Life Support Organization) ra đời, các trung tâm ECMO bắt đầu phát triển trên toàn thế giới từ năm 1990 là 83 trung tâm với 1644 ca ECMO, thống kê năm 2016 là 305 trung tâm với 7.368 ca ECMO; và tính tới tháng 7 năm 2016 có hơn 78.000 ca ECMO được tiến hành, trong đó hơn 29.000 ca trẻ sơ sinh suy hô hấp với tỷ lệ hồi phục là 74%, 7552 ca trẻ em và 10.601 ca người lớn với chẩn đoán suy hô hấp nặng, tỷ lệ hồi phục khoảng 58%; các ca còn lại tỷ lệ hồi phục giao động từ 40-50% [12]. Điều này chứng tỏ ECMO chính là cứu cánh của những bệnh cảnh nguy kịch hiện nay cũng như trong tương lai.

Nguyên lý hoạt động chính của ECMO là thực hiện vòng tuần hoàn ngoài cơ thể bằng cách hút máu chảy ra khỏi cơ thể với tốc độ dòng ổn định, tiến hành trao đổi khí O2 và CO2, sau đó bơm máu chứa O2 vào cơ thể. Khi bệnh nhân dần cải thiện sẽ giảm bớt tốc độ dòng ECMO và để tim phổi của bệnh nhân làm việc từ từ trở lại.
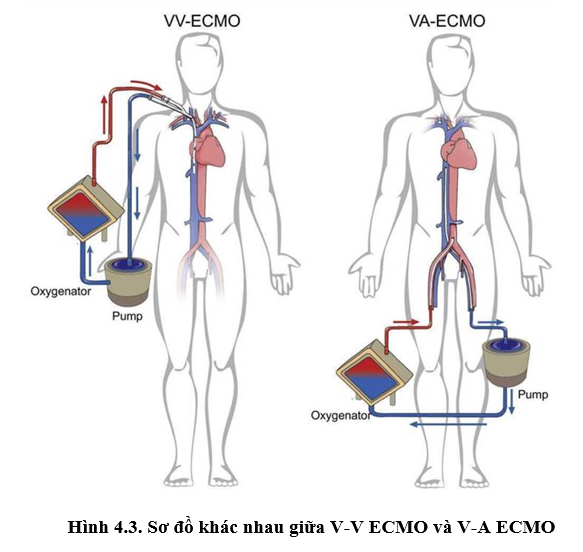
Hai loại ECMO chính:
• V – V ECMO: Lấy máu ra từ tĩnh mạch và trả máu về tĩnh mạch, sau khi trao đổi O¬2 và CO2 qua một màng trao đổi khí ngoài cơ thể, chủ yếu để hỗ trợ phổi.
• V – A ECMO: Lấy máu ra từ tĩnh mạch và trả máu về động mạch, chủ yếu để hỗ trợ cả tim và phổi.
Mục tiêu của ECMO:
-
Đảm bảo cho cơ thể bệnh nhân có đủ oxy
-
ECMO không chữa lành bệnh tim hoặc phổi nhưng giúp BN vượt qua nguy kịch, đồng thời kết hợp chữa trị nguyên nhân chờ thời gian tim phổi hồi phục.
-
Giảm bớt hỗ trợ máy thở để giảm nguy cơ tổn thương do máy thở.
-
Giảm nguy cơ sử dụng các thuốc trợ tim.
Khoa học y sinh ngày càng phát triển đã giúp kỹ thuật ECMO ngày càng hoàn thiện và tương đối dễ tiếp cận hơn. Do đó, số ca thực hiện ECMO tăng mỗi năm tạo những hiểu biết mới về các biển đổi của sinh lý trong quá trình ECMO ảnh hưởng lên dược động học (PK) và dược lực học (PD) của thuốc. Đây chính là thách thức lớn của nhà điều trị vì những thay đổi này mang tính cá thể cao và rất khó dự đoán, ước tính nhằm có những chiến lược điều trị tương ứng đảm bảo sự tối ưu của liệu pháp điều trị bằng thuốc trong quá trình ECMO. Trong phạm vi của chuyên đề, chúng tôi tóm tắt các hiểu biết còn hạn hẹp về ảnh hưởng của ECMO lên PK/PD của các thuốc thường sử dụng trên bệnh nhân nặng ICU để phần nào cung cấp những khuyến cáo hữu ích cho các bác sĩ tối ưu điều trị.
4.2. Ảnh hưởng của quá trình ECMO trên PK/PD của thuốc [1, 2, 4, 5, 6, 7, 8, 9, 10, 13]
Máy ECMO là một hệ thống khá phức tạp gồm ống dẫn máu, màng trao đổi oxy, bơm máu, bộ trao đổi nhiệt. Và để duy trì hệ thống hoạt động cần có dung dịch mồi (circuit priming), heparin chống đông máu,... Đây là quá trình mở rộng vòng tuần hoàn và thực hiện trao đổi khí ngoài cơ thể bằng các công cụ nhân tạo vì vậy tác động đáng kể đến việc thuốc lưu hành trong máu đặc biệt là nồng độ thuốc đảm bảo điều trị. Với hàng ngàn ca ECMO, các nhà khoa học đã dần định hình được các yếu tố quan trọng tác động lên PK của các thuốc thường sử dụng như thuốc an thần, giảm đau, thuốc kháng sinh, kháng nấm.
4.2.1. Yếu tố đặc tính của hệ thống ECMO [2, 4, 5, 6, 7, 8, 9]
Việc thuốc bị mất tại hệ thống ECMO là kết quả tất yếu. Lượng thuốc mất rất khó xác định do sự tương tác đa dạng giữa các đặc tính của chất liệu tạo hệ thống ECMO và các loại thuốc sử dụng.
Ví dụ: nếu sử dụng máu làm dung dịch mồi thì thuốc sẽ bị giữ tại hệ thống ECMO nhiều hơn so với dung dịch tinh thể; màng trao đổi oxy có thể làm mất các phân tử thân dầu kích thước nhỏ hoặc ống dẫn bằng PVC sẽ hấp phụ nhiều hơn các chất liệu khác.
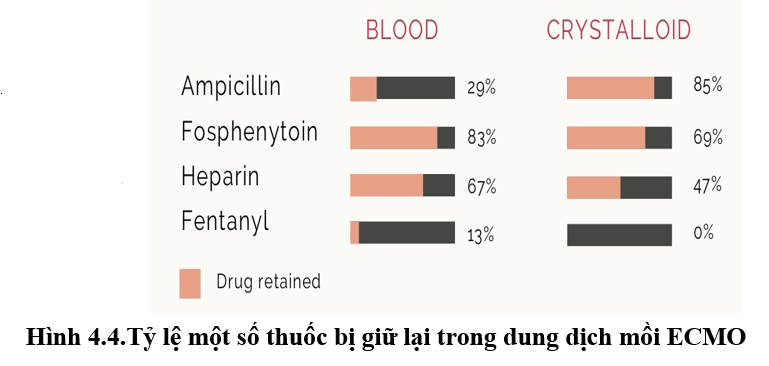
Loại màng trao đổi oxy, chất liệu hệ thống ống dẫn máu và dung dịch mồi (circuit priming) có ái lực hấp phụ khác nhau đối với các loại thuốc khác nhau. Kết quả thuốc bị gắn kết, tách cô lập tại hệ thống ECMO và dẫn đến thể tích phân bố của thuốc (Vd) có thể tăng, làm nồng độ thuốc giảm dưới mức trị liệu. Mặc khác, tình trạng này cũng làm cho hệ thống ECMO có thể trở thành một kho tích trữ thuốc và tái phân bố thuốc vào hệ thống tuần hoàn của bệnh nhân và dẫn đến kéo dài tác dụng của thuốc, thậm chí gây nguy cơ độc tính. Do đó, thời gian sử dụng của hệ thống màng và ống dẫn cũng là yếu tố tác động đến lượng thuốc bị gắn vào hệ thống.

4.2.2. Yếu tố đặc tính của thuốc [2, 3, 4, 5, 6, 7, 8, 9, 13]
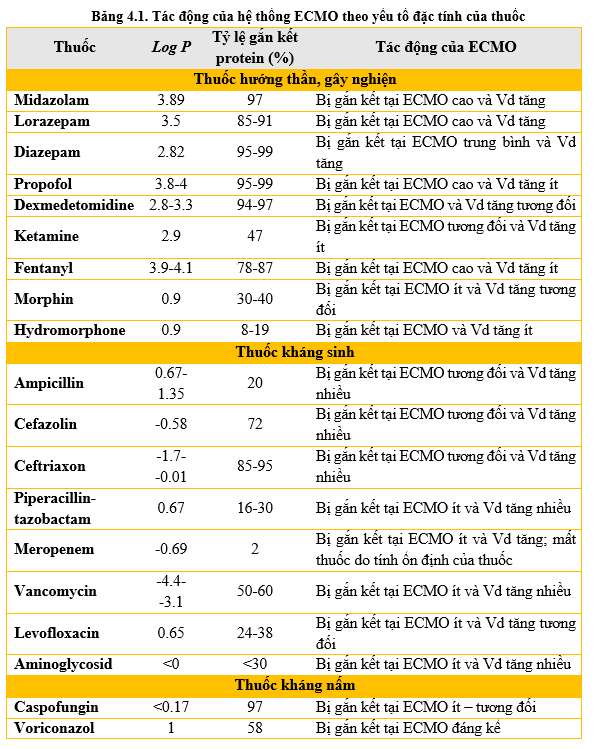
Đặc tính của thuốc ảnh hưởng khá nhiều đến việc gắn kết thuốc vào hệ thống ECMO bao gồm tỷ lệ gắn protein huyết tương, hệ số dầu-nước (Log P), kích thước phân tử và khả năng ion hóa. Ví dụ: Những thuốc thân dầu Log P lớn có ái lực cao gắn vào ống dẫn PVC của hệ thống ECMO; thuốc có tỷ lệ gắn protein huyết tương càng cao thì càng có khả năng bị cô lập tại hệ ECMO. Các yếu tố này cộng hưởng với nhau và tương tác với các đặc tính của hệ thống ECMO được thể hiện cụ thể một số thuốc theo Bảng 4.1
4.2.3. Yếu tố tình trạng sinh lý bệnh của người bệnh [1, 3, 5, 10]
Tình trạng lâm sàng của người bệnh khi thực hiện ECMO thường khá nặng do đó tạo những thay đổi về dược động học đặc thù riêng của từng cá thể. Hình tóm tắt các vấn đề trọng tâm cần đặc biệt lưu ý khi người bệnh nặng tiến hành ECMO
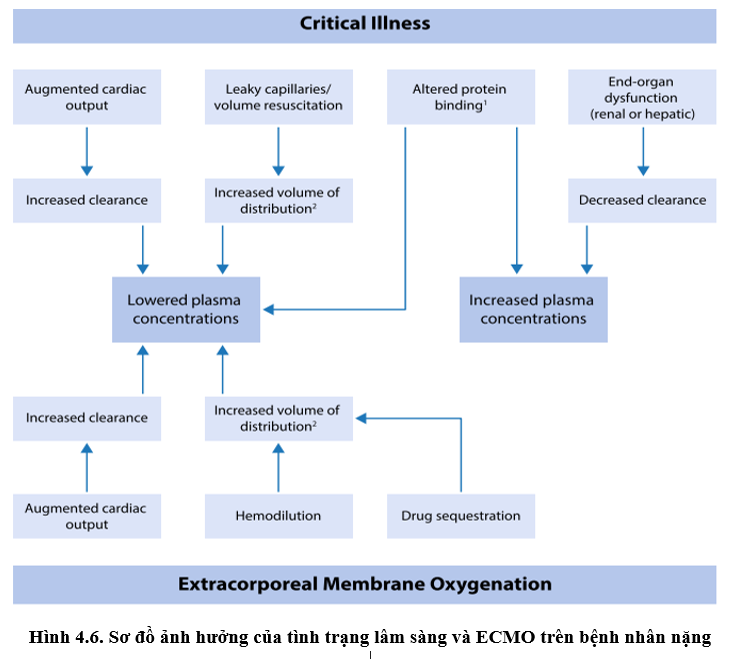
Như vậy, trạng thái dược động học của người bệnh chính là kết quả cộng hưởng của nhiều yếu tố và chủ yếu là tác động lên thể tích phân bố (Vd), độ thanh thải của thuốc (Cl). Hệ quả là ảnh hưởng trực tiếp hoặc gián tiếp thay đổi nồng độ thuốc điều trị. Mỗi thuốc khác nhau trên những cá thể người bệnh khác nhau sẽ tạo sự thay đổi rất đa dạng và khó lường. Vì vậy, những nghiên cứu trên bệnh nhân ECMO giúp tạo nền tảng hiểu biết cơ bản về dược động học trong quá trình ECMO và giúp định hướng điều chỉnh liều thuốc tương thích để tránh thất bại cũng như độc tính trong trị liệu (Bảng 4.2)
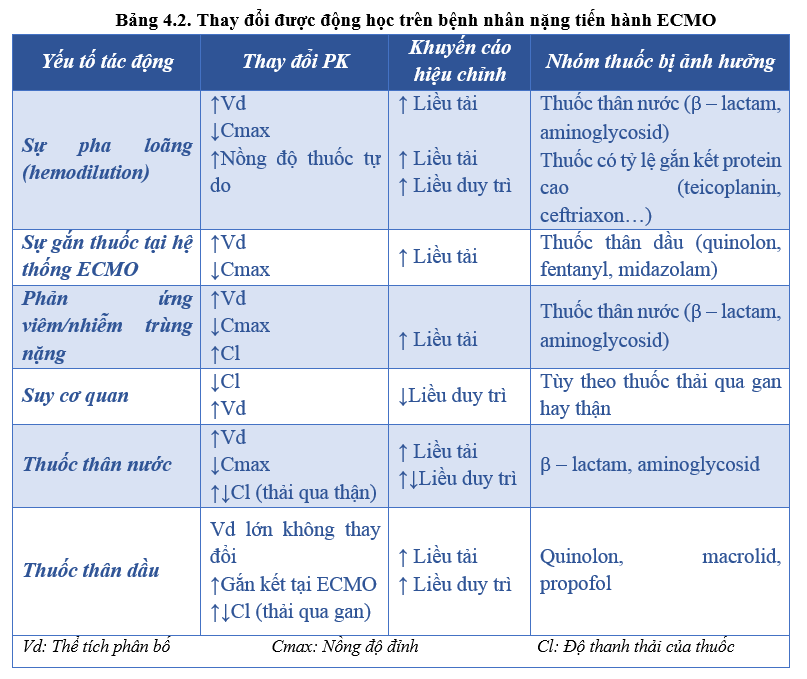
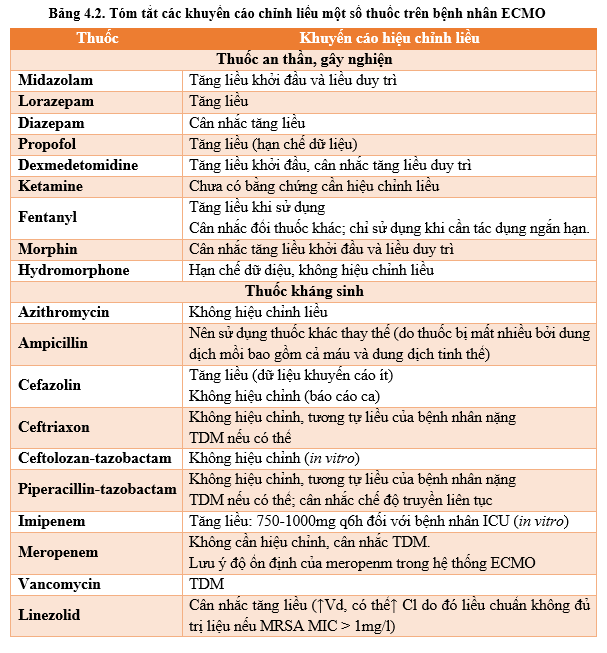
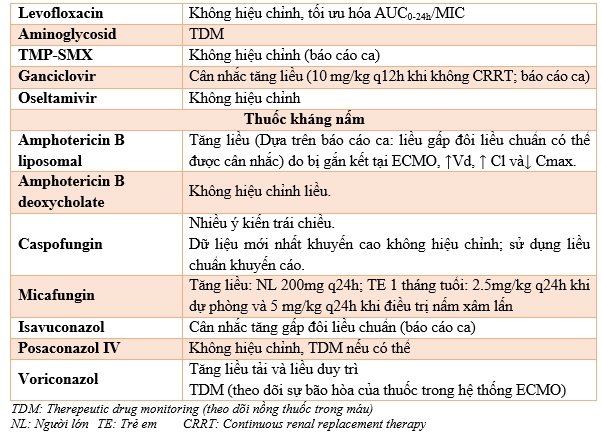
4.3. Chế độ liều hiệu chỉnh của một số thuốc thường sử dụng trong quá trình ECMO [3, 10, 11, 14]
ECMO đang trở thành một kỹ thuật can thiệp y khoa quan trọng. Nó như một biện pháp cứu mạng của nhiều trường hợp nguy cấp, đặc biệt là trong giai đoạn dịch bệnh COVID-19. Bệnh viện Bệnh Nhiệt Đới bắt đầu tiến hành kỹ thuật này từ khi điều trị bệnh nhân COVID-19 số 91 với sự hỗ trợ của Bệnh viện Chợ Rẫy và cũng đang dần hoàn thiện về cơ sở vật chất, kỹ thuật, đào tạo cán bộ y tế để có thể tự thực hiện ECMO cho người bệnh.
Ca ECMO đầu tiên tại bệnh viện đã mở ra nhiều cơ hội cứu sống người bệnh nhưng cũng cho thấy nhiều thách thức mà nhà điều trị phải xử trí. Một trong những thách thức đó chính là đảm bảo sử dụng thuốc an toàn và hiệu quả trong quá trình ECMO. Qua những kiến thức nền tảng đã trình bày ở phần trên, chúng ta có thể tóm tắt một số vấn đề trọng điểm như sau:
-
Thuốc có thể bị mất do gắn kết vào hệ thống ECMO và điều này có khả năng cao đối với các thuốc có đặc tính thân dầu và tỷ lệ gắn kết protein huyết tương cao.
-
Việc dẫn máu ra ngoài cơ thể làm tăng thể tích tuần hoàn khá lớn và có khả năng ảnh hưởng nhiều đến các thuốc có tính thân nước và Vd thấp do đó về nguyên lý cơ bản có thể làm giảm nồng độ thuốc trong máu.
-
Tình trạng lâm sàng nặng của từng cá thể người bệnh cũng ảnh hưởng khá lớn đến dược động học và sự giao thoa đồng thời với các yếu tố tác động của hệ thống ECMO tạo nên kết cục thay đổi chủ yếu về Vd, Cl và nồng độ thuốc trong máu -> thay đổi an toàn cũng như hiệu quả điều trị.
Những biến đổi về PK/PD của thuốc trên người bệnh ECMO khá đa dạng, khó dự đoán và chưa có các nghiên cứu phân tích đánh giá hệ thống mà đa phần là các báo cáo ca riêng lẻ. Tuy nhiên, với xu hướng điều trị theo chứng cứ y học và sự quan tâm ngày càng tăng về ECMO trong hai thập niên vừa qua của các nhà nghiên cứu đã mở ra bước đầu cho các khuyến cáo điều chỉnh liều nhằm tối ưu hóa trị liệu trên người bệnh. Và qua chuyên đề này, chúng tôi đã tóm tắt các khuyến cáo hướng dẫn liều một số thuốc thường sử dụng trong quá trình ECMO nhằm cung cấp cho bác sĩ điều trị những dữ liệu hiện hành có thể áp dụng và góp phần giải quyết các thách thức, khó khăn về sử dụng thuốc ở người bệnh chỉ định ECMO.
Tài liệu tham khảo:
-
Amy L. Dzierba, Darryl Abrams, and Daniel Brodie. Medicating patients during extracorporeal membrane oxygenation: the evidence is building. Critical Care (2017) 21:66.
-
Ami G. Shah et al. Medication Complications in Extracorporeal Membrane Medication Complications in Extracorporeal Membrane Oxygenation. Thomas Jefferson University 2017.
-
_Cheng V, Abdul-Aziz M, Roberts J, Shekar K. Optimising drug dosing in patients receiving extracorporeal membrane oxygenation. J Thorac Dis. 2018;10 (Suppl 5): S629-S641. https://www.ncbi.nlm.nih.gov/pubmed/29732181_.
-
_Cheng V, Abdul-Aziz M, Roberts J, Shekar K. Overcoming barriers to optimal drug dosing during ECMO in critically ill adult patients. Expert Opin Drug Metab Toxicol. 2019;15(2):103-112. https://www.ncbi.nlm.nih.gov/pubmed/30582435_.
-
_Dagan, J Klein, C Gruenwald, D Bohn, G Barker, G Koren, Preliminary studies of the effects of extracorporeal membrane oxygenator on the disposition of common pediatric drugs. Ther Drug Monit. 1993 Aug;15(4):263-6. https://pubmed.ncbi.nlm.nih.gov/8236359_
-
Drugs in Patients on Extracorporeal Membrane Oxygenation: A Review of the Current Literature. Clinical Therapeutics/Volume 38, Number 9, 2016.
-
_Dzierba A, Abrams D, Brodie D. Medicating patients during extracorporeal membrane oxygenation: the evidence is building. Crit Care. 2017;21(1):66. https://www.ncbi.nlm.nih.gov/pubmed/28320466_.
-
S_hekar K, Fraser J, Smith M, Roberts J. Pharmacokinetic changes in patients receiving extracorporeal membrane oxygenation. J Crit Care. 2012;27(6):741.e9-18. https://www.ncbi.nlm.nih.gov/pubmed/22520488_.
-
_Ha M, Sieg A. Evaluation of Altered Drug Pharmacokinetics in Critically Ill Adults Receiving Extracorporeal Membrane Oxygenation. Pharmacotherapy. 2017;37(2):221-235. https://www.ncbi.nlm.nih.gov/pubmed/27931091._
-
Jennifer Sherwin, MD; Travis Heath, PharmD; and Kevin Watt, MD. Pharmacokinetics and Dosing of Anti-infective
-
Kaitlin Branick , Matthew J Taylor , Matthew W Trump , Geoffrey C Wall, Apparent interference with extracorporeal membrane oxygenation by liposomal amphotericin B in a patient with disseminated blastomycosis receiving continuous renal replacement therapy. Am J Health Syst Pharm. 2019 May 17;76(11):810-813.
-
_Mehta T, Sallehuddin A, John J. The journey of pediatric ECMO, Qatar. Medical Journal, 4th Annual ELSO-SWAC Conference Proceedings 2017:4 http://dx.doi.org/10.5339/qmj.2017.swacelso.4_
-
Ayesha Ather, PharmD, BCPS. College of Pharmacy, Adjunct Assistant Professor, University of Kentucky. Pharmacotherapy Management in Patients with Extracorporeal Membrane Oxygenation.
-
Sanford guide Update 2021.
-
ThS.BS. Mai Văn Cường. Bệnh viện Bạch Mai. Kỹ thuật ECMO trong cấp cứu và hồi sức tim mạch.