1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
Quý 4-2022 ghi nhận có 39 báo cáo ADR xảy ra ở 11 khoa (theo bảng). Trong đó, ngoài nhà thuốc ngoại trú 11 ca, Nhi B 7 ca và Nhi D 5 ca. So với quý trước, số lượng báo cáo ADR Quý 4-2022 tương đương quý trước do tiếp tục ghi nhận thêm các ca ADR nghi ngờ liên quan ceftriaxone và amphoterincin B. Các khoa lâm sàng tiếp tục tăng cường giám sát, theo dõi, xử trí và báo cáo tác dụng phụ không mong muốn của thuốc (đặc biệt chú ý các phản ứng có liên quan đến ceftriaxone, amphoterincin B) gửi về khoa Dược trên phần mềm Ehospital.
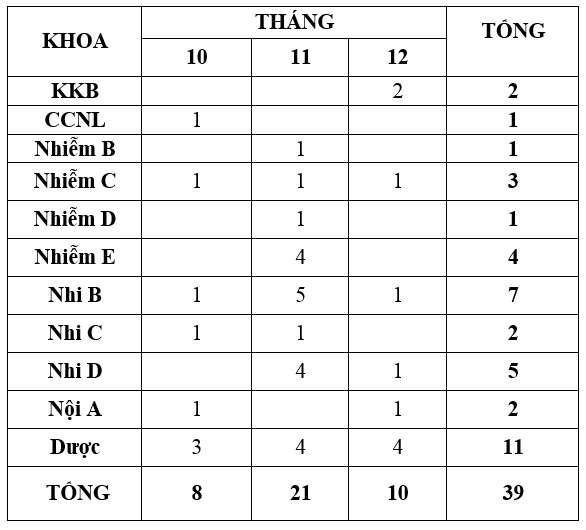
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
Nhi B và Nhi D xuất hiện 07 ca phản ứng phản vệ với chế phẩm Cetrimaz (hoạt chất ceftriaxone) cùng số lô 040722 và nhà sản xuất trong tháng 11. Đồng thời trong quý này ghi nhận 5 ca ADR liên quan Amphot (Amphotericin B) cùng số lô CC138E và nhà sản xuất xảy ra chủ yếu ở Nhiễm E. Khoa dược, P.Quản lý chất lượng, P. Điều dưỡng tiến hành theo dõi và khảo sát các quy trình liên quan. Hiện chưa có ghi nhận bất thường. Tuy nhiên, để đảm bảo an toàn điều trị cho người bệnh, bệnh viện đã đề nghị công ty đổi toàn bộ lô thuốc đồng thời tiếp tục theo dõi chặt chẽ việc sử dụng hai hoạt chất này.
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 4-2022
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 484 TH nội trú (thấp hơn so với quý 3/2022) và 1039 toa thuốc ngoại trú (tăng so với quý 3/2022). Đơn vị dược lâm sàng thực hiện 268 can thiệp dược lâm sàng chiếm 17.6% trong các hoạt động thường quy của DLS. Chủ yếu là các can thiệp hội ý/hội chẩn về thuốc: liều kháng sinh (trong đó có 71 ca Vancomycin, 03 ca AG), phối hợp kháng sinh và tư vấn về nguy cơ tác dụng bất lợi của thuốc,…và can thiệp trực tiếp khi duyệt nội trú y lệnh của khoa lâm sàng hàng ngày.
Trong 268 can thiệp có 76% là can thiệp trong việc sử dụng thuốc và giảm so với Quý 3/2022 vì tình hình số bệnh nhân giảm dần. Trong Quý 4/2022, sự thống nhất ý kiến giữa dược lâm sàng và bác sĩ điều trị tăng so với quý 2/2022: 99.6% so với 90.3 %, có 01 trường hợp đồng ý một phần chủ yếu ở các khoa khám ngoại trú và nhà thuốc bệnh viện và 0 trường hợp không đồng ý. Tỷ lệ can thiệp về “Ghi y lệnh thuốc”; “Thông tin hành chính liên quan đến thuốc” gia tăng trong quý 4/2022 so với quý 3/2022, lần lượt là: 16.0% so với 11.46%; 7.8% so với 2.58%. Một số can thiệp được ghi nhận là: Nhập nhằm số lượng, hàm lượng, dạng bào chế, tên thuốc, trùng cử thuốc do choàng cử, lãnh tổng (dạng chai, lọ siro thể tích lớn) nhưng quên chọn KHÔNG LÃNH ở những ngày dùng thuốc tiếp theo.
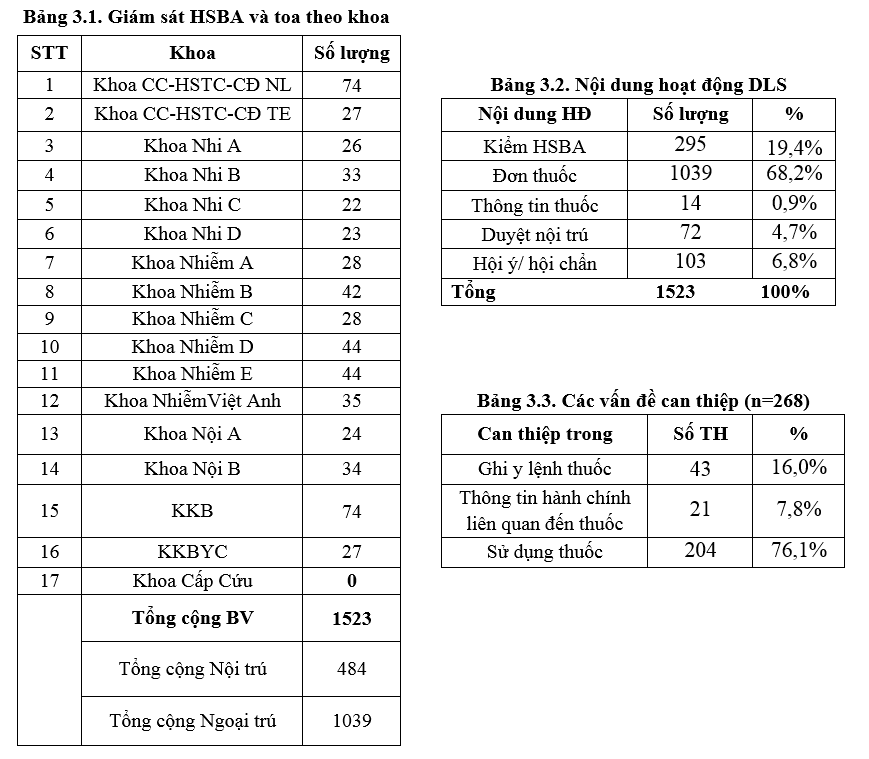
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
Toàn bệnh viện đạt 13 tiêu chí về sử dụng thuốc > 95% (tăng với Quý 3/2022 là 93%).
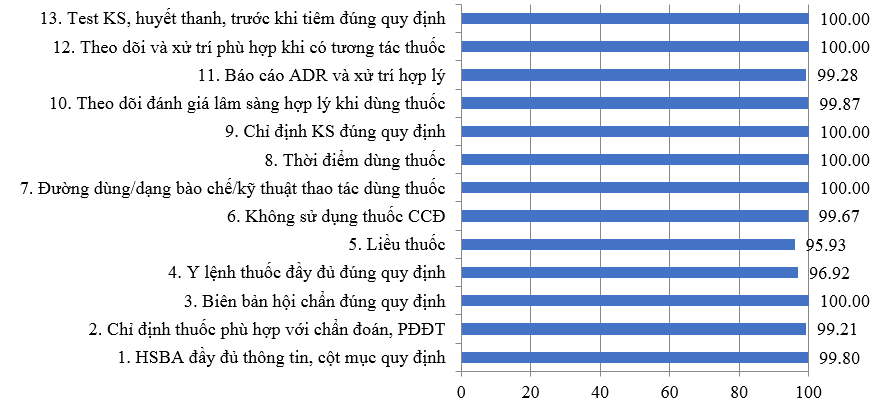
Tiêu chí liều thuốc và y lệnh đầy đủ tăng nhẹ so với Quý 3/2022. Các khoa thuộc Khối Nhi thực hiện các khuyến cáo về liều thuốc được cảnh báo từ Quý 2-3/2022 đã cải thiện khá nhiều nhưng vẫn cần lưu ý liều một số thuốc mới cho đối tượng trẻ em tùy theo tuổi và cân nặng; các thông tin chống chỉ định về độ tuổi và PCNT. Đồng thời, các bác sĩ/điều dưỡng khi nạp y lệnh trên HIS cần chú ý để tránh trùng hoặc sai y lệnh, sai ngày giờ dùng thuốc, ở KKB và KKBYC vẫn còn một số lỗi về đánh máy toa thuốc.
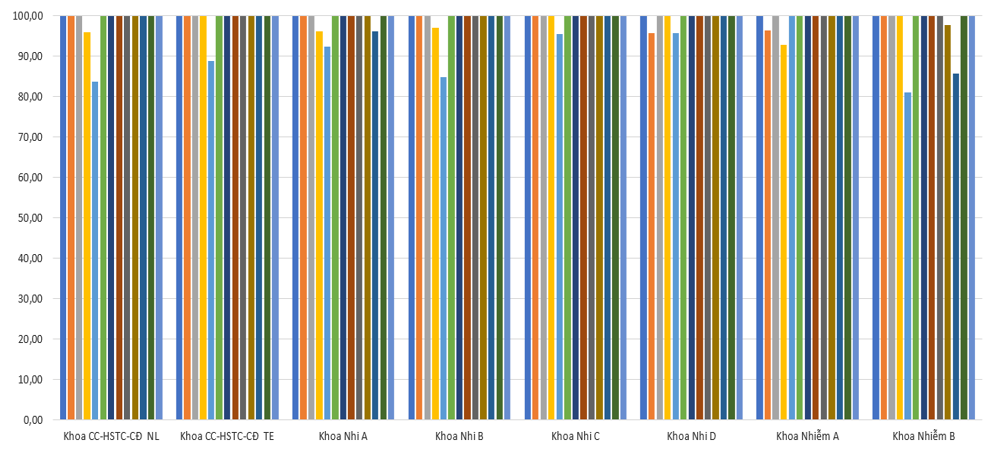

3.2. Khuyến cáo dược lâm sàng:
Quy chế kê đơn:
- Khi nạp y lệnh trùng trên hệ thống HIS hoặc đánh nhầm số lượng, tên thuốc, trùng y lệnh; đặc biệt lưu ý khi choàng cử thuốc. Các sai sót này chưa xảy ra và ngăn chặn kịp thời tuy nhiên số sai sót tăng so với Quý 2/2022. Ví dụ:
-> Nhầm tên thuốc:
Aziphar (azithromycin 200mg/5ml) -> Nhập Aticizal (Levocetirizin 2.5mg/5ml)
Stacytin 200mg (N-acetylcystein 200mg) -> Nhập Stadleucin 500mg (acetyl leucin 500mg)
Azein 250mg: 5 lọ/ngày -> Oresol 5 gói/ngày
Ezenstatin (atorvastatin10mg+ Ezetimib 20mg) -> Nhập Enterobella (Lactobacilus)
Cetimed (cetirizin10mg) -> Nhập Cetigam (vitamin C 200mg/10ml)
ANTI@42 8400USP(Alphachymotrypsin 8400 UI) -> Nhập Anticlor (Dexchlorpheniramin 2mg/5ml)
Etmin 10mg (ebastin 10mg) -> Nhập Eramux 50mg (eprazinon 50mg)
Silymax Complex (Slymarin 70mg) -> Silyhepatis (L-arginin 1000mg/5ml)
Blosatin 20 (ebastin 20mg) -> Nhập Bometan (betamethason 0.5mg/g+ Calcipotriop 50mcg/g)
Atisyrup ( kẽm 10mg) -> Nhập Atisalbu (salbutamol 4mg/10ml)
-> Nhầm hàm lượng:
Langitax 10mg (Rivaroxaban 10 mg) -> Nhập Langitax 20 (Rivaroxaban 20 mg)
Lamivudin 150mg -> Nhập Lamivudin 100mg
Paracetamol 150mg -> Nhập paracetamol 500mg
-> Nhầm số lượng:
Medlon 16 (Methylprednisolon 16mg) 15 viên -> Nhập thành 30 viên
Prednisolon 5mg số lượng 10 viên -> Nhập thành 30 viên
Levofloxacin 500mg số lượng 28 viên -> Nhập 56 viên
Ivermectin 6mg: 1 viên -> Ivermectin 6mg: 2 viên
Op. copan (cao khô lá thường xuân 35mg/5ml) 1 chai -> Nhập 9 chai Op. copan
Ivermectin 6mg: 4 viên -> Nhập 28 viên
Liều:
- BN NTH, VP do vi khuẩn đa kháng CRAB sử dụng liều cao Sulbactam 6-9g q8h theo IDSA 2022 và Uptodate 2022, tuy nhiên sẽ làm tăng liều Ampicillin và Cefoperazol trong chế phẩm phối hợp (do không có chế phẩm đơn chất Sulbactam) và có thể lớn hơn liều khuyến cáo của NSX.
-> Khuyến cáo NSX AMA POWER (1g Ampi + 0.5 g Sulbactam): TỔNG LIỀU Sulbactam ≤ 4g/ngày MAX 8 lọ/ngày chia q6-q8h
-> Khuyến cáo NSX Ampicillin (đơn chất) 1g IV: Liều tối đa Ampicillin 12g/ngày
-> Khuyến cáo cập nhật: Ampi+Sulbactam 9g q8h = 27 g/ngày = 18 g Ampi + 9 g Sulbactam = 6 lọ x 3 lần/ngày
-> Sử dụng Cefoperazon + Sulbactam thay thế lưu ý chức năng gan, nguy cơ rối loạn đông máu
- Bệnh nhân nhiễm nấm Aspergillus mũi xoang đang điều trị duy trì với Voriconazol liều 200mg q12h (CN 47kg). Bệnh nhân tái khám, xét nghiệm lại chức năng gan: AST, ALT ~ 100 UI/L; GGT tăng cao. Lâm sàng bệnh nhân ổn, cải thiện.
-> Voriconazol có liên quan đến việc tăng cao các xét nghiệm chức năng gan và các dấu hiệu lâm sàng của tổn thương gan như vàng da. NSX khuyến cáo với bệnh nhân suy gan:
-> Liều tấn công chuẩn: 400mg q12h; Liều duy trì giảm ½ ở bệnh nhân xơ gan nhẹ - trung bình (Child - Pugh A và B). Chưa có nghiên cứu trên bệnh nhân xơ gan Child-Pugh C.
-> Khuyến cáo chỉnh liều duy trì ở bệnh nhân: 100mg q12h (Giảm 50% liều duy trì tiêu chuẩn). Tái khám lại sau 2 tuần + đánh giá lại chức năng gan, đáp ứng lâm sàng.
- Bệnh nhân PCP đang điều trị phác đồ thay thế: Clindamycin + Primaquin. Nhập Clindamycin 300mg/2ml, ống 2ml, nhập 01 ống q8h.
-> Chế phẩm hiện có tại khoa Dược là: Clindamycin 300mg/2ml, ống 2ml -> Liều điều trị VP PCP là 600mg q8h -> Cần nhập 02 ống q8h. Lưu ý phân biệt với Clindamycin 150mg/ml, ống 4ml (01 ống = 600 mg)
- Bệnh nhân cấy dịch rửa phế quản (+) Pseudomonas aeruginosa đa kháng chỉ nhạy colistin -> Muốn bổ sung thêm dạng khí dung
-> Theo Hướng dẫn sử dụng kháng sinh 2022 (BV BNĐ) khuyến cáo có thể phối hợp colistin phun khí dung như một liệu pháp bổ sung thêm đối với trực trùng gram âm đa kháng với liều 2-4 MIU/12h
-
Khuyến cáo lưu ý cách ghi liều các chế phẩm đa liều cho bệnh Nhi trên Ehos: Hoastex, Flabivi, Desloratadin.
-
Bệnh 71t, 48kg, 150 cm. Chẩn đoán: Nhiễm nấm Aspergillus mũi xoang; Suy hô hấp hiện ổn. Bệnh nhân đã được điều trị trên 2 tháng với Voriconazol. Men gan GGT tăng 396 456 u/l. AST, ALT trong giới hạn bình thường. Vấn đề: TD tác dụng phụ của Vorionazole, hiện lâm sàng ổn. IBW = 45 kg. Theo khuyến cáo NXS, Uptodate về việc hiệu chỉnh liều ở bệnh nhân suy gan.
-> Bác sĩ đánh giá bệnh nhân đáp ứng lâm sàng tốt + theo dõi tác dụng phụ của Voriconazol lên chức năng gan.
-> Khuyến cáo giảm liều Voriconazol duy trì: 100mg q12h + Đánh giá đáp ứng lâm sàng điều trị và đánh giá lại chức năng gan sau 1-2 tuần điều trị.
Sử dụng thuốc:
- Bệnh nhân nam, 55kg, 167cm. Chẩn đoán: Melioidosis thể nhiễm trùng huyết, thể áp xe đa cơ quan (tuyến mang tai, lách, màng não, phổi, tuyến tiền liệt); TD áp xe ngoài màng cứng (T); TD Dị ứng da do cotrim; Đái tháo đường type 2; TD tổn thương thận cấp cải thiện. Rx Meropenem 2g q8h + Cotrim 960mg x 2 viên q8h (N31). Vấn đề: BN tăng Eosinophil máu, ngứa 2 cẳng chân lúc có lúc không, không sang thương da. Esoinophil: 0.08 0.26 0.72 1.05 1.92 (ngày 26/12).
-> Các thuốc đang sử dụng cho bệnh nhân có ghi nhận tăng Eosin:
-
Meropenem: Mức độ ít gặp
-
Cotrim: Mức độ hiếm gặp
-> Chưa loại trừ nguyên nhân tăng Eosin do thuốc đang sử dụng. Khuyến cáo: Ngưng 1 trong 2 thuốc (Meropenem hoặc Cotrim) theo đánh giá đáp ứng lâm sàng hiện tại. Theo dõi CBC để đánh giá loại trừ/xác định nguyên nhân do thuốc đang sử dụng + Báo cáo ADR. Theo dõi, đánh giá chức năng/mức độ tổn thương các cơ quan
- Bệnh nhân 14t, 74kg, 160cm. Chẩn đoán: Sốc sốt xuất huyết Dengue N7. Đang Rx Vancomycin 1.5g q8h (1.5g pha trong 300 mL NaCl 0.9% = 900 ml/ngày), Imipenem/Cilastatin 500mg q6h (500mg pha trong 100 mL NaCl 0.9% = 400 ml/ngày). Tổng lượng dung môi đưa vào = 1300 ml/ngày. Vấn đề: Giai đoạn tái hấp thu, thể tích tuần hoàn cao có nguy cơ phù phổi. Dịch truyền kháng sinh # 1300 ml/ngày, có 2 thời điểm kháng sinh truyền cùng giờ (08h và 23h).
-> Khuyến cáo có thể giảm thể tích dung môi/dịch pha kháng sinh như sau: Vancommycin 1.5g pha trong 200 mL (nồng độ Vancomycin truyền là 7.5 mg/mL, nồng độ tối đa cho phép khi truyền tĩnh mạch ngoại biên là 10mg/mL, truyền tĩnh mạch trung tâm là 20mg/mL) Giảm 300 mL dung môi/ngày. Imipenem/Cilastatin 500mg pha trong 60 mL dung môi -> Giảm 160 ml/ngày
-> Tổng thể tích dịch giảm được là: 460 ml/ngày (giảm ~ 35% thể tích dung môi pha kháng sinh). Lưu ý về độ tan khi pha cô đặc hơn (tăng thời gian đảo trộn/lắc) + giảm tốc độ truyền (kéo dài thời gian truyền).
-> Bác sĩ đánh giá nguy cơ quá tải dịch, cân bằng xuất nhập Hội chẩn DLS khi cần thiết pha thuốc hạn chế dung môi
- Bệnh nhân đặt sonde tiểu, cấy nước tiểu (+) Proteus mirabilis kháng carbapenem. Chỉ nhạy Tigecycline. Rx Tigecyclin LD 100mg, MD 50mg q12h. Theo khuyến cáo NSX, Tigecyclin (Tigacyl) chỉ có chỉ định trong những trường hợp sau: Nhiễm trùng da và cấu trúc da có biến chứng, Nhiễm trùng ổ bụng có biến chứng. GIỚI HẠN chỉ định: KHÔNG chỉ định cho nhiễm trùng bàn chân đái tháo đường; Viêm phổi bệnh viện, viêm phổi thở máy do các nghiên cứu đến hiện tại đều cho thấy không hiệu quả Về mặt dược động học: 59% Tigecyclin thải trừ qua gan/mật dưới dạng không biến đổi; 33% qua nước tiểu dạng nguyên vẹn/liên hợp
-> Không chuyến cáo chỉ định Tigecyclin cho Nhiễm trùng tiểu do Proteus mirabilis. Bác sĩ đồng ý 1 phần, tạm thời trì hoãn điều trị, thay sonde tiểu mới, hội chẩn chuyên khoa tiết niệu. Ngày hôm sau, bệnh nhân sốt, tầm soát nguyên nhân không loại trừ nhiễm trùng tiểu -> Rx Tigecyclin: Lưu ý điều kiện thanh toán BHYT + Đáp ứng lâm sàng
- Bệnh nhân được chẩn đoán nhiễm nấm Talaromyces marneffei huyết và Bệnh nhân được chẩn đoán nhiễm nấm Mucor tuyến mang tai -> Rx Amphotericin B (Amphot). Bệnh nhân bị sốt, lạnh run khi truyền. Bác sĩ đổi sang chế phẩm Amphotericin B phức hợp lipid
-> Phản ứng chung khi truyền Amphotericin B: Rét run và sốt, đau đầu, đau cơ hoặc khớp xảy ra với mức độ: Thường gặp (ADR 1/100)
-> Cách xử trí ADR: Dùng liều tăng dần như HD NSX; Để giảm phản ứng sốt, rét run, có thể Rx thuốc hạ sốt (paracetamol, ibuprofen) và kháng histamin trước khi truyền tĩnh mạch Amphotericin B (NSX, Uptodate)
-> Việc đổi sang chế phẩm Ampholip lưu ý tư vấn thân nhân/bệnh nhân về liệu trình và chi phí điều trị (vấn đề thanh toán BHYT) và ADR: sốt, rét run khi truyền vẫn được nghi nhận khi truyền Ampholip phức hợp lipid
- Bệnh nhân Nhi có tiền sử sốt cao co giật, ho ít có thể siro thuốc HOASTEX không?
-> Theo NSX, chế phẩm siro HOASTEX chống chỉ định cho TE có tiền sử động kinh hoặc co giật do sốt cao -> Không khuyến cáo sử dụng. Thay thế thuốc ho khác.
- Bệnh nhân 9t , chẩn đoán: Mề đay , kê đơn Thymomodulin 80mg
-> Thymomodulin 80mg CCĐ cho TE < 12 tuổi (NSX) -> Thay thế thuốc khác nếu cần thiết
- Bệnh nhân dị ứng chưa rõ dị nguyên -> Rx 2 thuốc Antihistamin H1 cùng thế hệ 2
-> Theo phác đồ BV: Chỉ được phối hợp 2 kháng histatmin H1 khác thế hệ -> Thay desloratadin/Levocertirizin bằng 1 thuốc kháng histamin H1 thế hệ 1 (ví dụ: Chlopheniramin)
- Rx Oseltamivir cho PNCT
-> Oseltamivir là tác nhân kháng virus được cân nhắc để điều trị bệnh nhân cúm cho PN mang thai vì đây là tác nhân có kinh nghiệm lâm sàng lớn nhất. Dữ liệu về sự an toàn của oseltamivir trong thời kỳ mang thai còn hạn chế, đặc biệt là trong ba tháng đầu; tuy nhiên, lợi ích của việc điều trị sớm dường như lớn hơn nguy cơ tiềm ẩn.
-> Kết quả nghiên cứu cho thấy tỷ lệ sinh non, dị tật bẩm sinh và điểm Apgar thấp tương tự nhau giữa nhóm nhóm PNCT có sử dụng (nhóm bệnh) so với nhóm PNCT không sử dụng (nhóm chứng) chất ức chế (neuraminidase)
-> Liều khuyến cáo như liều người lớn trưởng thành: 75 mg q12h, Rx 5 ngày.
Tương tác thuốc:
BS lưu ý khi có cảnh báo mức độ 5 và có thể chủ động liên hệ DLS hội ý về việc sử dụng chung vì các CẢNH BÁO MỨC ĐỘ 5 LÀ CHỐNG CHỈ ĐỊNH theo Quyết định Bộ Y tế ra 5948/QĐ-BYT về việc ban hành Danh mục tương tác thuốc chống chỉ định trong thực hành lâm sàng tại các cơ sở khám bệnh, chữa bệnh.

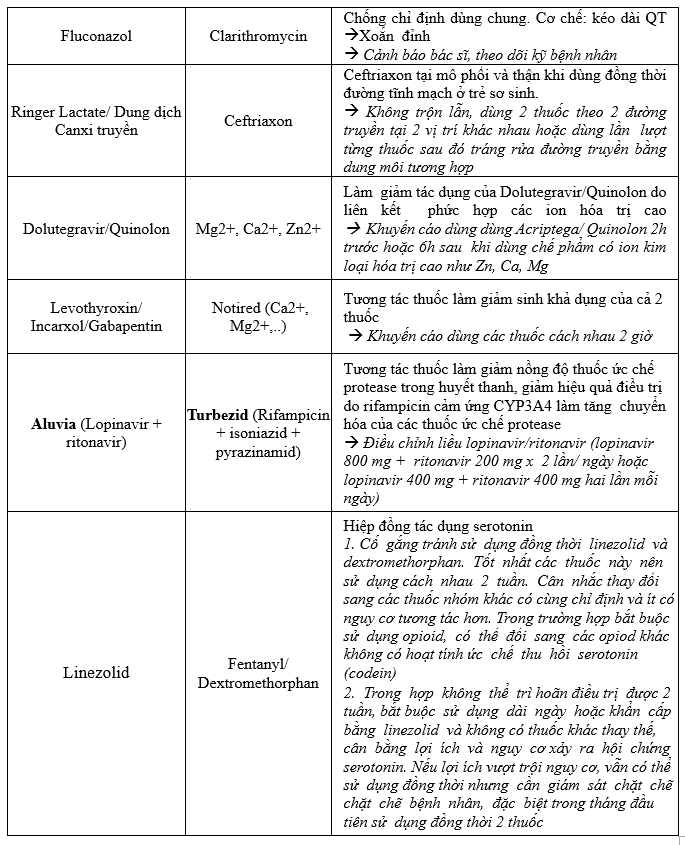
Khuyến cáo Hội đồng thuốc và điều trị:
(1) Quý 2/2022, cơ quan BHYT cảnh báo việc chỉ định không phù hợp với các thuốc
-
Các thuốc chống chỉ định cho trẻ em: Thuốc Notired eff Strawberry: CCĐ TE <6 tuổi; Levofloxacin: CCĐ TE<18 tuổi
-
Các thuốc chỉ định không đúng tờ hướng dẫn sử dụng đã được đăng ký:
Plavix 75mg,
Langitax 10 (Rivaroxaban)
Encorate Chrono 500 (Valproat),
Atorvastatin 20
Cofidec (celecoxib) 200mg,
Grangel
Dacolfort (Diosmin-hesperidin),
Lyrica (Pregabalin 75mg)
Givet-4 (Monterlukast),
Jimenez (TDF) 300mg
SaVi Gabapentin,
- Các thuốc sử dụng khi có Chống chỉ định theo tờ hướng dẫn sử dụng, như sau: Lipovenoes 10%, Lipidem, Smoflipid 20%, Oliclinomel N4-550 E, Clinoleic 20%, Metsav 850; Metformin Stella 850mg
(2) Quản lý thuốc mua theo yêu cầu đề xuất của khoa lâm sàng theo mẫu phiếu gửi trên Tủ hồ sơ Office online. Lưu ý các khoa lâm sàng ghi đầy đủ nội dung, đặc biệt là tên hoạt chất và hàm lượng.
(3) Việc sử dụng sulbactam liều cao theo khuyến cáo IDSA năm 2022:
IDSA ban hành IDSA Guidance on the Treatment of Antimicrobial-Resistant Gram-Negative Infections: Ver 2.0 có khuyến cáo điều trị Acinetobacter baumanii kháng Carbapenem (CRAB) với Ampicillin + Sulbactam liều cao: 9-12g Sulbactam.
Hiện không có chế phẩm Sulbactam đơn lẻ, khoa dược có 02 chế phẩm dạng phối hợp Ampicillin + Sulbactam (tỷ lệ 2:1) và Cefoperazon + Sulbactam (tỷ lệ 1:1) và Tờ hướng dẫn sử dụng thuốc của 02 chế phẩm này giới hạn liều MAX của Sulbactam là 4g và liều MAX Ampicillin, Cefoperazon là 12g.
-> Hội đồng khuyến cáo như sau:
Hội chẩn chuyên môn. Có thể cân nhắc liều cao Sulbactam từ 6-9g.
Tư vấn cho người bệnh và thân nhân bệnh nhân về điều trị kháng sinh liều cao.
Theo dõi lâm sàng chặt chẽ về hiệu quả và độ an toàn.
Khuyến cáo ASP: Nếu sử dụng từ 3 KS cần hội ý/hội chẩn với Ban QLSDKS trước khi sử dụng, đặc biệt TH nhiễm khuẩn đa kháng thuốc nên hội ý VSLS.
4. CHUYÊN ĐỀ: CHỨNG CỨ Y HỌC HIỆN ĐẠI VỀ THỜI GIAN SỬ DỤNG VÀ ĐƯỜNG DÙNG KHÁNG SINH
Kháng sinh ra đời từ một thế kỷ trước được coi là một trong những phát minh thành công nhất trong lịch sử y học, là vũ khí mạnh mẽ chống lại nhiễm trùng do vi khuẩn [1]. Cũng như các loại thuốc khác, sử dụng kháng sinh từ lâu đã tồn tại nhiều quan điểm điều trị phổ biến và được xem là tiêu chuẩn trong thực hành lâm sàng. Trong đó, điển hình là hai quan điểm sau [3]:
(1) Duy trì sử dụng kháng sinh ngay cả khi bệnh nhân đã hết triệu chứng, và
(2) Chỉ sử dụng kháng sinh đường tĩnh mạch trong một số hội chứng nhiễm trùng nhất định.
Đáng lưu ý, nền tảng của các quan điểm trên chỉ đến từ các báo cáo ca/ chùm ca từ cả nửa thế kỷ trước và được phóng đại bởi ý kiến từ các chuyên gia. Hai quan điểm này đã bị “lật lại” bởi nhiều nghiên cứu tiến cứu có độ tin cậy cao hơn. Cụ thể, hơn 120 thử nghiệm lâm sàng ngẫu nhiên có đối chứng (Randomized Controlled Trials, RCTs) chứng minh được rút ngắn liệu pháp kháng sinh có hiệu quả tương đương với liệu pháp “truyền thống” trong nhiều loại nhiễm trùng và 21 RCT cho thấy liệu pháp kháng sinh uống ít nhất cũng hiệu quả như đường tĩnh mạch (IV) trong điều trị viêm tủy xương, nhiễm trùng máu và viêm nội tâm mạc [3]. Các bằng chứng này dẫn đến sự chuyển dịch về quan điểm điều trị của các nhà lâm sàng hiện đại, và sự ra đời của hai nguyên tắc điều trị mới, đó là: “Shorter is better” và “Oral is the new IV”.
Tuy nhiên, hiện tại hai nguyên tắc mới này vẫn chưa được áp dụng tại nhiều cơ sở thực hành. Theo ý kiến từ y học hiện đại, đã đến lúc để thay đổi các quan điểm này trong thực hành điều trị bệnh truyền nhiễm để tiến tới kỷ nguyên y học chứng cứ (evidence based medicine) [3, 6].
Bài viết xin được tổng hợp các y văn hiện đại về sự thay đổi của hai quan điểm điều trị truyền thống trên, đi từ bối cảnh lịch sử cho tới các bằng chứng mới đáng tin cậy hơn. [14].
4.1. Nguyên tắc hiện đại về thời gian sử dụng kháng sinh “Shorter is better”
Theo Bộ Y tế Việt Nam (2015), “độ dài đợt điều trị phụ thuộc vào tình trạng nhiễm khuẩn, vị trí nhiễm khuẩn và sức đề kháng của người bệnh” [19].
Nguyên tắc “Shorter is better” trong sử dụng kháng sinh đề cập đến việc rút ngắn số ngày trong một đợt kháng sinh mà không làm tăng nguy cơ thất bại điều trị. Khi nguyên tắc này được thực hiện một cách an toàn, nó có thể mang lại lợi ích như giảm nguy cơ gây hại của kháng sinh, bao gồm biến cố có hại (ví dụ: suy gan, thận..), tình trạng bội nhiễm (superinfection, ví dụ nhiễm Clostridium dificile) và đề kháng kháng sinh [1][12]. Bên cạnh đó, việc rút ngắn thời gian điều trị hợp lý giúp giảm nguy cơ sai sót trong sử dụng kháng sinh [10], giảm chi phí điều trị và tăng tuân thủ dùng thuốc ở BN [19].
Thông thường, các nhà lâm sàng có khuynh hướng tiếp tục đợt điều trị kháng sinh ngay cả khi các triệu chứng nhiễm trùng đã được giải quyết, với mục đích hạn chế nhiễm trùng tái phát và phát triển đề kháng thuốc nhưng chưa có bằng chứng nào ủng hộ niềm tin trên. Ngược lại, thực tế đã ghi nhận nhiều trường hợp kháng thuốc do dùng kháng sinh kéo dài, làm tăng phơi nhiễm kháng sinh với vi khuẩn và tăng áp lực chọn lọc dòng vi khuẩn kháng thuốc [3, 6, 12]. Nhiều triệu chứng của nhiễm trùng có thể đến từ đáp ứng viêm của cơ thể đối với vi khuẩn, hơn là do sự hiện diện của vi khuẩn sống. Do đó, sự kéo dài của triệu chứng trong một vài ngày không đồng nghĩa với việc vẫn còn vi khuẩn [15]. Theo bác sĩ Rice, rút ngắn đợt điều trị kháng sinh là một trong những phương án khả thi nhất để làm giảm áp lực chọn lọc kháng sinh. Điều này mang lại lợi ích cho cả BN được chỉ định kháng sinh phù hợp lẫn các trường hợp điều trị quá mức (ví dụ sử dụng kháng sinh phổ rộng hoặc phối hợp kháng sinh không cần thiết) [12].
4.1.1. Tổng hợp bằng chứng
Vào năm 2021, Hiệp hội bác sĩ Hoa Kỳ (American College of Physicians, ACP) đã nhấn mạnh sự không cần thiết của sử dụng kháng sinh dài ngày và đưa ra lời khuyên thực hành lâm sàng (the best practice advice) về rút ngắn thời gian điều trị trong bốn loại nhiễm trùng thường gặp, bao gồm: viêm phế quản với đợt bùng phát bệnh phổi tắc nghẽn mạn tính (COPD), viêm phổi cộng đồng, nhiễm trùng tiểu và nhiễm trùng da, mô mềm (Bảng 1) [6].

Vào năm 2022, một số tác giả đã tóm lược về kết quả của hơn 120 RCT so sánh hiệu quả giữa việc rút ngắn liệu pháp kháng sinh và liệu trình truyền thống trong 17 loại nhiễm trùng (Bảng 2) [3, 14]. Để có thể áp dụng phù hợp trong thực hành lâm sàng, các chuyên gia y tế nên truy cập vào các nghiên cứu gốc và phiên giải cẩn thận về đối tượng BN, ưu nhược điểm của từng nghiên cứu.
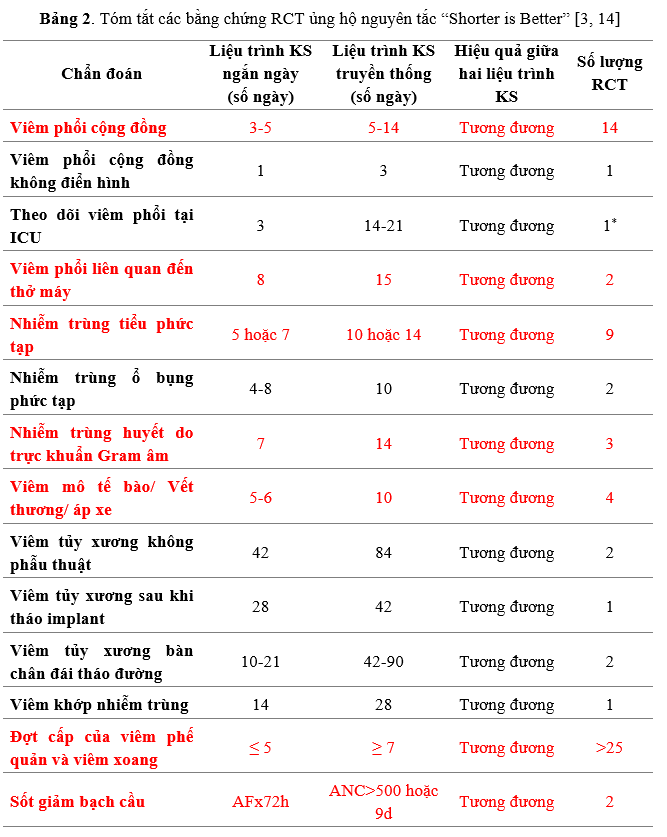

Từ bảng 1 và bảng 2 có thể thấy, việc rút ngắn thời gian dùng kháng sinh có thể áp dụng cho nhiều loại nhiễm trùng (bao gồm cả nhiễm trùng không biến chứng, có biến chứng và cấp tính), trên cả BN ngoại trú, nội trú, miễn dịch đầy đủ hoặc suy giảm miễn dịch [5]. Ngoài khía cạnh tương đương về hiệu quả, các RCT cũng chứng minh được tính an toàn của liệu pháp kháng sinh ngắn ngày.
Bên cạnh các RCT, các bằng chứng thế giới thực (real-world evidence) cũng ủng hộ nguyên tắc “Shorter is better”. Ví dụ một nghiên cứu hồi cứu trên 1488 hồ sơ bệnh án của BN nội trú cho thấy điều trị kháng sinh sau 10 ngày làm tăng 3% nguy cơ biến cố có hại của thuốc, phổ biến nhất là bất thường trên tiêu hóa (42%), trên thận (24%) và huyết học (15%) [7, 18]. Gần đây, một nghiên cứu quan sát được thực hiện trên hơn 1000 BN nội trú ≥ 18 tuổi tại 24 bệnh viện tại Hoa Kỳ nhằm xác định thời gian điều trị kháng sinh tối ưu đối với nhiễm trùng tiểu biến chứng. Tiêu chí chính đánh giá là tỷ lệ tái phát nhiễm trùng trong vòng 30 ngày sau khi kết thúc điều trị. Kết quả cho thấy không có sự khác biệt về tỷ lệ tái phát giữa nhóm dùng kháng sinh 10 ngày (46%) và nhóm dùng 14 ngày (54%). Đáng chú ý, tỷ lệ tái phát ở nhóm dùng kháng sinh 7 ngày là 37% so với 63% ở nhóm dùng 14 ngày (95% CI: 1,4 – 4,6) [8]
4.1.2. Ngoại lệ của nguyên tắc “Shorter is better”
Mặc dù rút ngắn liệu trình kháng sinh có nhiều lợi ích, nhưng không phải trường hợp nào cũng phù hợp để áp dụng. Hiệp hội bác sĩ Hoa Kỳ (ACP) đã lưu ý các khuyến cáo thực hành (Bảng 1) có thể không thích hợp cho BN có giải phẫu phức tạp (ví dụ giãn phế quản) hoặc có tiền sử nhiễm vi khuẩn kháng thuốc gần đây [6]. Ngoài ra, việc rút ngắn liệu trình kháng sinh không hiệu quả bằng liệu trình “truyền thống” trong nhiễm trùng khớp nhân tạo còn lưu thiết bị (retention of the device), viêm tai giữa ở trẻ dưới 2 tuổi, và trong điều trị viêm phổi mạn do Aspergillus (Bảng 3) [3, 14].
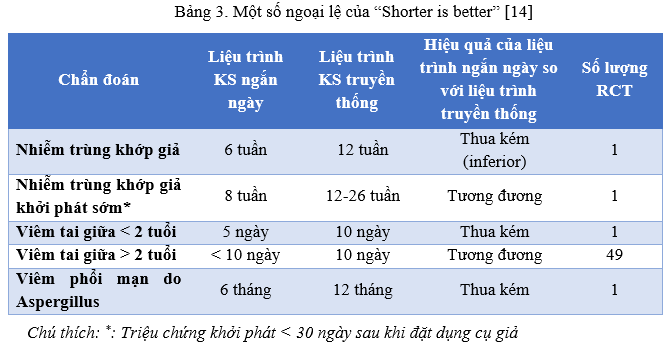
Các trường hợp cần kéo dài đợt điều trị kháng sinh thường liên quan đến tình trạng bệnh lý phức tạp, ví dụ: nhiễm khuẩn huyết Staphylococcus aureus và Pseudomonas, tình trạng bệnh nguy kịch với nguyên nhân phức tạp, nguồn nhiễm trùng chưa được kiểm soát đầy đủ [4, 7].
Tóm lại, mục tiêu quan trọng là cần cá thể hóa thời gian điều trị kháng sinh theo đáp ứng của từng BN. Với các loại nhiễm trùng mà nguyên tắc “Shorter is better” được chứng minh đồng nhất qua nhiều nghiên cứu, các bác sĩ nên được khuyến khích ngưng kháng sinh cho bệnh nhân ngay khi các triệu chứng nhiễm trùng đã được giải quyết [15]. Đối với các loại nhiễm trùng chưa xác định được thời gian điều trị tối ưu, cần thêm các nghiên cứu được thiết kế tốt để đề xuất phương pháp thích hợp [1].
4.2. Nguyên tắc hiện đại về đường dùng kháng sinh “Oral is the new IV”
4.2.1. Tổng quan về lịch sử
Đối với một số loại nhiễm trùng như viêm tủy xương, nhiễm trùng huyết và viêm nội tâm mạc nhiễm khuẩn, quan điểm chỉ dùng kháng sinh tĩnh mạch trong cả liệu trình điều trị đã tồn tại một thời gian dài.
Theo Davar và cộng sự, niềm tin này đến từ các báo cáo chùm ca từ những năm 1950-1960 (với viêm tủy xương) và 1940-1950 (với viêm nội tâm mạc). Cụ thể, trong điều trị viêm tủy xương, kháng sinh đường uống bị tác giả phủ định về hiệu quả ngay cả khi chưa được thử nghiệm trên BN [25]. Các báo cáo ca viêm nội tâm mạc ghi nhận tỷ lệ chữa khỏi của các kháng sinh đường uống (sulfanilamide, erythromycin, tetracycline) chỉ < 30%, thấp hơn nhiều so với tỷ lệ > 75% của kháng sinh penicillin IV. Tuy nhiên cần lưu ý là các kháng sinh đường uống trên vốn là các kháng sinh cũ với đặc tính dược động ít phân bố trong máu, dẫn đến không đạt đủ nồng độ mục tiêu trong máu so với nồng độ ức chế tối thiểu (MIC) của vi khuẩn. Do đó, việc áp dụng các nghiên cứu cũ, không được kiểm soát (uncontrolled) vào thực hành lâm sàng hiện đại không thực sự phù hợp, đặc biệt khi ngày nay đã có nhiều kháng sinh đường uống mới hơn với sinh khả dụng cao và đủ khả năng đạt được nồng độ mục tiêu trong máu [3, 16, 25].
4.2.2. Tóm tắt các bằng chứng hiện đại
Nguyên tắc “Oral is the new IV” nhằm chỉ ra liệu pháp đường uống hoặc chuyển đổi sang uống cũng có hiệu quả tương đương hoặc có thể vượt trội hơn so với đường dùng tiêm tĩnh mạch.
Nguyên tắc trên đang được khẳng định theo các dữ liệu được tích lũy dần. Một tổng quan hệ thống được xuất bản năm 2021 đã phân tích 21 RCT so sánh giữa liệu pháp chỉ dùng kháng sinh tiêm tĩnh mạch và liệu pháp chuyển đổi sang kháng sinh uống đối với ba loại nhiễm trùng viêm tủy xương, nhiễm trùng huyết và viêm nội tâm mạc nhiễm khuẩn. Về hiệu quả lâm sàng, không có sự khác biệt giữa hai liệu pháp trên. Về tính an toàn, liệu pháp chuyển đổi qua uống giúp làm giảm tần suất các biến cố liên quan đến catheter và thời gian nằm viện. Đặc biệt, không có RCT đơn lẻ nào cho thấy điều ngược lại (Bảng 4). Từ đó, tác giả đề xuất ưu tiên chuyển đổi sang kháng sinh uống trong ba loại nhiễm trùng trên đối với BN thích hợp [24].
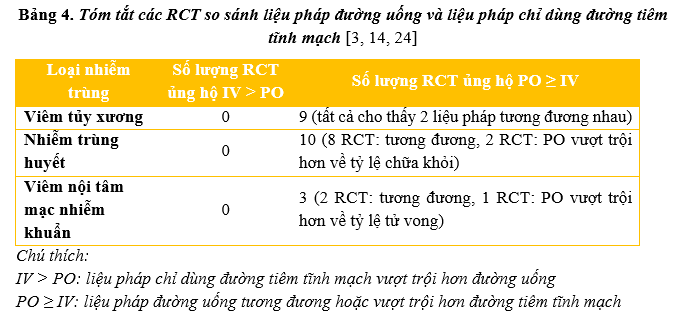
Ngoài ba loại nhiễm trùng trên, tính tương đương về hiệu quả giữa đường uống và đường tĩnh mạch cũng được thể hiện ở một số loại nhiễm trùng khác, ví dụ như viêm phổi ở người lớn (4 RCT) [2, 9, 11, 13, 23], sốt giảm bạch cầu ở BN ung thư [22], viêm thận cấp ở trẻ em [9, 17].
Về mặt lợi ích, kháng sinh đường uống giúp tránh được nguy cơ gây hại của kháng sinh tĩnh mạch như biến cố tiêu chảy, viêm mạch, huyết khối, tổn thương thoát mạch tại vị trí tiêm, nhiễm trùng cục bộ hoặc thậm chí nhiễm trùng huyết [9]. Ngoài ra, kháng sinh đường uống thường có giá thành rẻ, tính tiện lợi cao và có thể giúp tăng tuân thủ điều trị ở BN [19].
Sinh khả dụng (hay phần trăm thuốc vào đến hệ tuần hoàn) là một thông số dược động học thường được nhắc đến đối với kháng sinh đường uống. Theo Bộ Y tế, sinh khả dụng từ 50% trở lên được coi là tốt. Các kháng sinh có sinh khả dụng trên 80% được coi là hấp thu tương tự như đường tiêm tĩnh mạch và hoàn toàn có thể cân nhắc trong điều trị nối tiếp đường tiêm tĩnh mạch (Bảng 5) [19, 21].
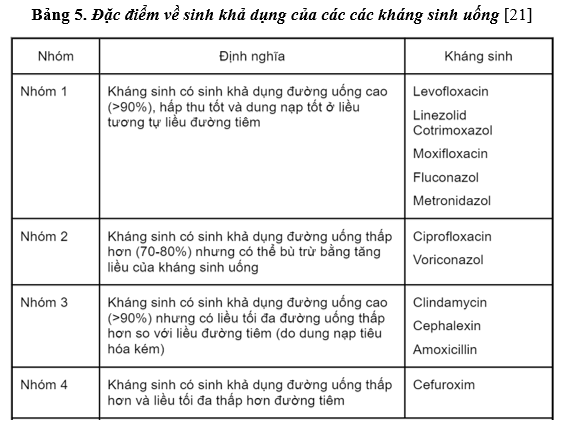
Bộ Y tế cũng khuyến cáo nên lựa chọn các kháng sinh đường uống ở hầu hết trường hợp nhiễm trùng, ngoại trừ BN bị giảm khả năng hấp thu qua đường tiêu hóa (do bệnh lý đường tiêu hóa, khó nuốt, nôn, tắc ruột...) hoặc một số nhiễm trùng nặng, cấp tính cần đạt nhanh nồng độ thuốc trong máu. Bên cạnh đó, khi cần phải sử dụng đường tiêm tĩnh mạch, cần đánh giá thường xuyên các yếu tố để xem xét chuyển đổi sang đường uống ngay khi có thể. Các kháng sinh đường uống có sinh khả dụng cao và ít bị ảnh hưởng bởi thức ăn được ưu tiên để chuyển đổi. Ban quản lý sử dụng kháng sinh cần đảm bảo rằng tất cả các nhân viên y tế liên quan đều được đào tạo, tập huấn để biết cách thức thực hiện được việc chuyển đổi kháng sinh từ đường tiêm sang đường uống trong thực hành lâm sàng. Hướng dẫn khuyến khích sự hợp tác của nhóm chuyên trách bao gồm các bác sĩ và dược sĩ lâm sàng – vốn là chuyên gia về dược động học của thuốc, giúp tư vấn về liều dùng khi chuyển đổi… [19, 21].
Tổng hợp lại, liệu pháp đường uống hoặc chuyển đổi sang đường uống nên được cân nhắc trong viêm tủy xương, nhiễm trùng huyết, và viêm nội tâm mạc nhiễm khuẩn cũng như một số loại nhiễm trùng khác ở bệnh nhân thỏa các điều kiện sau [3, 16, 19, 20]:
-
BN ổn định về lâm sàng và huyết động, và
-
Đường uống không bị hạn chế (không có các tình trạng như nôn, tiêu chảy nặng, rối loạn nuốt, mất ý thức..) và BN có thể hấp thu được thuốc uống, và
-
Nguồn nhiễm khuẩn đã được kiểm soát bằng các thủ thuật nếu cần thiết, (hoặc đã sạch khuẩn trong máu), và
-
Có sẵn kháng sinh đường uống phù hợp theo các phác đồ điều trị và nhạy cảm với tác nhân vi khuẩn gây bệnh/ có phổ trùng với kháng sinh tĩnh mạch, và
-
BN không đang nhiễm các loại nhiễm trùng cấp tính, cần thiết đạt nhanh nồng độ đỉnh trong máu.
Bộ Y tế có hướng dẫn cụ thể việc chuyển đổi sang đường uống tại Quyết định số 5631/QĐ-BYT về việc ban hành tài liệu “Hướng dẫn thực hiện quản lý sử dụng kháng sinh trong bệnh viện”.
Kết luận:
Nhiều quan điểm điều trị phổ biến hiện tại chỉ đơn giản dựa trên các báo cáo ca không được kiểm soát từ hơn hàng chục năm trước và không phù hợp thực hành lâm sàng theo y học chứng cứ. Để tối ưu hóa trong điều trị bệnh nhân, nhân viên y tế cần liên tục cập nhật, đánh giá lại những điều đã biết cũng như thay đổi cách tiếp cận trong thực hành lâm sàng. Dĩ nhiên, tất cả các bằng chứng trên không thể khẳng định rằng việc rút ngắn thời gian sử dụng kháng sinh và phác đồ đường uống/chuyển đổi sang đường uống sẽ phù hợp cho mọi BN cũng như tất cả loại nhiễm trùng. Tuy nhiên, các nghiên cứu này đã xác định được [3]:
-
Tính hiệu quả tương đương của việc rút ngắn thời gian dùng kháng sinh so với chuẩn mực thông thường trong một số loại nhiễm trùng nhất định và
-
Kháng sinh đường uống là một cân nhắc hợp lý để điều trị nối tiếp đường tiêm tĩnh mạch trong viêm mô tế bào, nhiễm trùng huyết, và viêm nội tâm mạc.
Nếu bệnh nhân không cải thiện với kháng sinh thích hợp, thay vì chỉ tập trung quy trách nhiệm cho đường uống hoặc mặc định kéo dài thời gian dùng kháng sinh, trước hết, các nhà lâm sàng nên đánh giá các yếu tố khác như: việc kiểm soát nguồn nhiễm trùng, liều lượng thuốc, sự tuân thủ điều trị của bệnh nhân...
TÀI LIỆU THAM KHẢO
-
Aminov Rustam I %J Frontiers in microbiology (2010), "A brief history of the antibiotic era: lessons learned and challenges for the future", 1, pp. 134.
-
Castro-Guardiola Antoni, Viejo-Rodríguez Alfonso-Luís, Armengou-Arxé Arola, et al. (2001), "Efficacy and safety of oral and early-switch therapy for community-acquired pneumonia: a randomized controlled trial", 111(5), pp. 367-374.
-
Davar Kusha, Clark Devin, Centor Robert M, et al., "Can the Future of ID Escape the Inertial Dogma of Its Past?: The Exemplars of Shorter Is Better and Oral Is the New IV," in Open Forum Infectious Diseases, 2022.
-
Havey Thomas C, Fowler Robert A, Pinto Ruxandra, et al. (2013), "Duration of antibiotic therapy for critically ill patients with bloodstream infections: A retrospective cohort study", 24(3), pp. 129-137.
-
Imlay Hannah, Spellberg Brad %J Transplant Infectious Disease (2022), "Shorter is better: The case for short antibiotic courses for common infections in solid organ transplant recipients", 24(5), pp. e13896.
-
Lee Rachael A, Centor Robert M, Humphrey Linda L, et al. (2021), "Appropriate use of short-course antibiotics in common infections: best practice advice from the American College of Physicians", 174(6), pp. 822-827.
-
Maximos Mira. (2020). Shorter Is Better With Antibiotics: Lessons & Resources. Available: https://www.idstewardship.com/shorter-better-antibiotics-lessons-resources/, truy cập ngày 19/01/2023
-
McAteer John, Lee Jae Hyoung, Cosgrove Sara E, et al. (2023), "Defining the Optimal Duration of Therapy for Hospitalized Patients with Complicated Urinary Tract Infections and Associated Bacteremia", Clinical Infectious Diseases.
-
Morgenstern Justin (2019), "Magical thinking in modern medicine: IV antibiotics for cellulitis".
-
Nguyen Lam V, Pham Lien TT, Bui Anh L, et al., "Appropriate Antibiotic Use and Associated Factors in Vietnamese Outpatients," in Healthcare, 2021, p. 693.
-
Oosterheert Jan Jelrik, Bonten Marc JM, Schneider Margriet ME, et al. (2006), "Effectiveness of early switch from intravenous to oral antibiotics in severe community acquired pneumonia: multicentre randomised trial", 333(7580), pp. 1193.
-
Rice Louis B %J Clinical infectious diseases (2008), "The Maxwell Finland Lecture: for the duration—rational antibiotic administration in an era of antimicrobial resistance and Clostridium difficile", 46(4), pp. 491-496.
-
Siegel Robert E, Halpern Neil A, Almenoff Peter L, et al. (1996), "A prospective randomized study of inpatient IV antibiotics for community-acquired pneumonia: the optimal duration of therapy", 110(4), pp. 965-971.
-
Spellberg Brad. (2023, 16/1). Available: https://www.bradspellberg.com/, truy cập ngày 19/01/2023.
-
Spellberg Brad %J Journal of hospital medicine (2018), "The maturing antibiotic mantra:“shorter is still better”", 13(5), pp. 361.362.
-
Spellberg Brad, Chambers Henry F, Musher Daniel M, et al. (2020), "Evaluation of a paradigm shift from intravenous antibiotics to oral step-down therapy for the treatment of infective endocarditis: a narrative review", 180(5), pp. 769-777.
-
Strohmeier Yvonne, Hodson Elisabeth M, Willis Narelle S, et al. (2014), "Antibiotics for acute pyelonephritis in children", (7).
-
Tamma Pranita D, Avdic Edina, Li David X, et al. (2017), "Association of adverse events with antibiotic use in hospitalized patients", 177(9), pp. 1308-1315.
-
Bộ Y tế (2015), "Quyết định 708/QĐ-BYT của Bộ Y tế về việc ban hành Tài liệu chuyên môn Hướng dẫn sử dụng kháng sinh".
-
Bộ Y tế (2016), "THỰC HIỆN QUẢN LÝ SỬ DỤNG KHÁNG SINH TRONG BỆNH VIỆN (Ban hành kèm theo Quyết định số 772/QĐ-BYT ngày 04 tháng 3 năm 2016)".
-
Bộ Y tế (2020), "THỰC HIỆN QUẢN LÝ SỬ DỤNG KHÁNG SINH TRONG BỆNH VIỆN (Ban hành kèm theo Quyết định số 5631 ngày 31 tháng 12 năm 2020)".
-
Vidal Liat, Paul Mical, Eliakim‐Raz Noa, et al. (2013), "Oral versus intravenous antibiotic treatment for febrile neutropenia in cancer patients", (10).
-
Vogel Friedrich, Lode Harmut %J Journal of Antimicrobial Chemotherapy (1991), "The use of oral temafloxacin compared with a parenteral cephalosporin in hospitalized patients with pneumonia", 28(suppl_C), pp. 81-86
-
Wald-Dickler Noah, Holtom Paul D, Phillips Matthew C, et al. (2022), "Oral Is the New IV. Challenging Decades of Blood and Bone Infection Dogma: A Systematic Review", 135(3), pp. 369-379. e1.
-
Waldvogel Francis A, Medoff Gerald, Swartz Morton N %J New England Journal of Medicine (1970), "Osteomyelitis: a review of clinical features, therapeutic considerations and unusual aspects", 282(5), pp. 260-266.