- 1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
- 2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
- 3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 2-2023
- 4. CHUYÊN ĐỀ: CHIẾN LƯỢC ĐIỀU TRỊ COVID-19 TRONG TÌNH HÌNH MỚI:
1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
Quý 2-2023 ghi nhận có 27 báo cáo ADR xảy ra ở 12 khoa (theo bảng). Trong đó, khoa Dược báo cáo nhiều nhất với 10 ca, hầu hết là các trường hợp ngoại trú. So với quý trước, báo cáo ADR Quý 2-2023 tăng cả về số khoa và số ca báo cáo. Các khoa lâm sàng tiếp tục tăng cường giám sát, theo dõi, xử trí và báo cáo tác dụng phụ không mong muốn của thuốc gửi về khoa Dược trên phần mềm Ehospital.
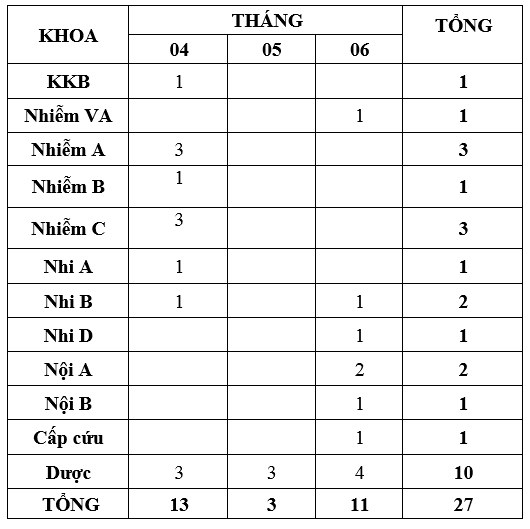
B. Phản hồi các khoa lâm sàng về chất lượng thuốc: Không có
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 2-2023
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 430 TH nội trú (giảm nhẹ so với quý 1/2023) và 755 toa thuốc ngoại trú (tăng nhẹ so với quý 1/2023) do tình hình bệnh giảm. Đơn vị dược lâm sàng thực hiện 199 can thiệp dược lâm sàng chiếm 16.7% trong các hoạt động thường quy của DLS (giàm so so với Quý 1/2023 là 19.4%). Chủ yếu là các can thiệp hội ý/hội chẩn về thuốc: liều kháng sinh (trong đó có 48 ca vancomycin, tỷ lệ sử dụng vancomycin giảm dần và tăng dần số ca sử dụng linezolide), phối hợp kháng sinh và tư vấn về nguy cơ tác dụng bất lợi của thuốc,…và can thiệp trực tiếp khi duyệt nội trú y lệnh hàng ngày.
Trong 199 can thiệp có 81.9% là can thiệp trong việc sử dụng thuốc và tăng so với với Quý 1/2023 vì tình hình số bệnh nhân giảm dần. Trong Quý 2/2023, sự thống nhất ý kiến giữa dược lâm sàng và bác sĩ điều trị tương tự với quý 1/2023: 99.5 %, có 01 trường hợp không đồng ý chủ yếu ở các khoa khám ngoại trú và nhà thuốc bệnh viện.
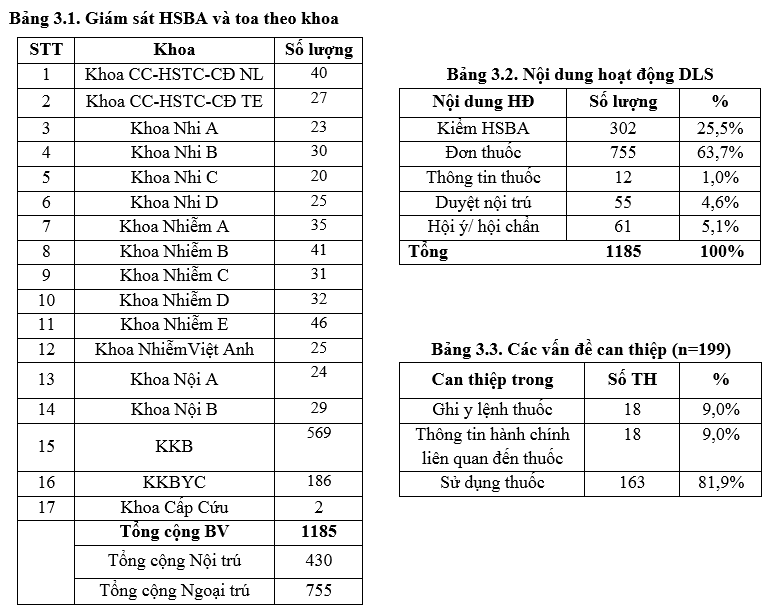
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
Toàn bệnh viện đạt 13 tiêu chí về sử dụng thuốc > 95% (tăng nhẹ so với Quí 1/2023 là 94%).

Tiêu chí liều thuốc và y lệnh đầy đủ tăng nhẹ so với Quý 4/2022. Các khoa thuộc Khối Nhi thực hiện các khuyến cáo về liều thuốc được cảnh báo tuy có cải thiện nhưng vẫn cần lưu ý liều một số thuốc mới cho đối tượng trẻ em tùy theo tuổi và cân nặng; khoa Nhiễm Việt Anh, A và E cần lưu ý hơn về liều thuốc do tình trạng bệnh nặng kèm thay đổi chức năng gan, thận. Đồng thời, các bác sĩ/điều dưỡng khi nạp y lệnh trên HIS cần chú ý để tránh trùng hoặc sai y lệnh, sai ngày giờ dùng thuốc, ở KKB và KKBYC vẫn còn một số lỗi về đánh máy
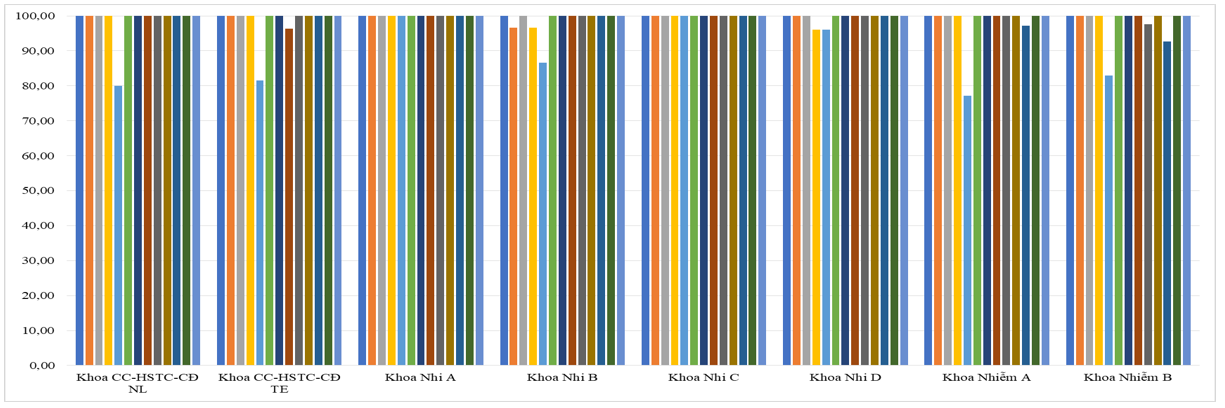

3.2. Khuyến cáo dược lâm sàng:
Quy chế kê đơn:
Khi nạp y lệnh trùng trên hệ thống HIS hoặc đánh nhầm số lượng, tên thuốc, trùng y lệnh; đặc biệt lưu ý khi choàng cử thuốc. Các sai sót này chưa xảy ra và ngăn chặn kịp thời tuy nhiên vẫn còn sai sót trong Quý 1/2023.
Ví dụ:
• Sai hàm lượng: 08 trường hợp
• Sai số lượng: 07 trường hợp
• Sai tên thuốc: 05 trường hợp
-
Sai tên thuốc: Bs kê đơn VASMETIN (acrivastin 8mg) -> Nhập VASTEC 35 MR (Trimetazidin 35mg)
-
Kê đơn MEYERBASTIN 10mg(ebastin 10mg) -> Nhập Meyersucral (sucralfat 1g)
-
Kê đơn CHYMORICH 8400IU (Alphachymotrysin 8400IU) -> CEFURICH 500mg (Cefuroxim 500mg)
-
Kê đơn FIBROFIN 145 (fenofibrat 145mg) -> Nhập FIBYHE-200 (Ibuprofen 200mg)
-
Kê đơn ANTICLOR (dexchlorpheniramin 2mg) -> Nhập ATIRIN 20 (Ebastin 20mg)
• Sai dạng bào chế: 01 trường hợp
- Kê đơn PARACETAMOL 150mg (gói)- uống Nhập PARACETAMOL 150mg (viên) - đặt hậu môn
Liều:
- BN nhiễm trùng huyết (+) MSSA Rx Oxacilin 2 g q6h
-> Khuyến cáo chỉnh liều Oxacilin thành 2 g q4h cho chỉ định nhiễm trùng huyết
-
BN COVID-19 dự phòng huyết khối Rx Heparin 25.000 UI q12h TDD -> Khuyến cáo liều heparin SC trong dự phòng huyết khối là 5000 UI q8-12h
-
Bệnh nhân Viêm phổi do A.baumanii đa nhạy. Rx Cefoperazone/Sulbactam (1g+1g) 4.5 lọ x 2 lần/ngày, hủy 0.5 lọ mỗi cử, tổng liều: 9g/ngày.
-> Khuyến cáo chế độ liều Cefoperazone/Sulbactam cho V.P do A.baumanii: Liều Sulbactam 6-9 g/ngày chia q8h -> Báo bs điều trị chỉnh lại liều Cefoperazone/Sulbactam: 3 lọ (1g+ 1g) q8h [Biệt dược Sulbactam].
- Bệnh nhân 80kg, cao 175cm. Chẩn đoán: TD nang ấu trùng sán dải heo. Kết quả chụp MRI sọ não thấy u đa vùng trán bên phải, chẩm bên trái bắt thuốc viền, phù não xung quanh. BN hiện đang được kê: Dexamethasone 32mg, Albendazole 400mg x 2 lần/ngày.
-> Theo phác đồ điều trị ấu trùng sán dải heo trên thần kinh trung ương (Uptodate), nếu BN có từ 1-2 nang sán, khuyến cáo phác đồ sử dụng thuốc bao gồm: kháng kí sinh trùng đơn trị Albendazole liều 15 mg/kg/ngày chia làm 2 lần uống cùng với bữa ăn, max 1200mg/ngày, kháng viêm Corticoid liều cao và thuốc chống động kinh.
-> Khuyến cáo chỉnh liều Albendazole thành 600mg x 2 lần/ngày. Theo dõi vấn đề viêm não/phù não, nếu có phù tiến triển, cân nhắc ngưng điều trị kháng kí sinh trùng.
- BN nam 38 tuổi, 50 kg, 155 cm. CĐ: viêm não siêu vi chưa loại trừ HSV. Rx Acyclovir IV 250 mg q8h.
-> Khuyến cáo liều điều tị Viêm não do HSV là Acyclovir IV 10 mg/kg q8h -> BN 50 kg nên cần tăng liều thuốc lên thành 500mg q8h.
Sử dụng thuốc:
-
Ca 1: BN (68 kg, 170 cm) Rx Vancomycin N6 1,25 g (5g/ngày) q6h. C đáy = 11.6. BN vẫn cấy máu ra MRSA, số lượng ổ áp xe tăng
-
Ca 2: Bệnh nhân 16t, 90 kg, 175cm, BMI = 29.4 kg/m^2. Chẩn đoán: Nhiễm trùng huyết từ áp xe mô mềm vùng cẳng tay P do Cầu trùng Gram dương đứng chùm; TD Viêm khớp háng T. TD Viêm xương cẳng tay P. Cấy máu (+) MRSA. Rx Vancomycin 1g q6h (4g/ngày). SCr 70 -> 65 umol/mL
-> Vấn đề: Kết quả đo nồng độ Vancomycin đáy: Ctrough = 8.7 ug/mL, AUC/MIC ước tính ~ 400 mcg*hr/mL. Lâm sàng đáp ứng chậm, cấy máu lại (+) MRSA, Ctrough < 10 ug/mL.
-> Khuyến cáo chuyển Vancomycin sang chế độ truyền liên tục
- Ca 3: BN 30t, 76kg, 165. Chẩn đoán: TD nhiễm trùng huyết do cầu trùng gram dương đứng riêng đôi chuỗi chưa loại trừ MRSA/ TD viêm nội tâm mạc nhiễm trùng/TD bệnh van tim. Kết quả cấy máu (+) Streptococcus sanguinis (đa nhạy). *Vấn đề: Bác sĩ chẩn DLS về chế độ liều Gentamicin trong điều trị Viêm nội tâm mạc nhiễm trùng (chưa loại trừ)
-> Khuyến cáo liều: Ampicillin 2g q4h + Gentamicin chế độ truyền thống 1 mg/kg q8h (tính theo IBW). Không chuyến cáo AG chế độ liều ODA cho tác dụng đồng vận trong viêm nội tâm mạc do vi khuẩn Gram dương.
- Ca 4: BN 8 tuổi, chẩn đoán chàm da, bs kê đơn BOMETAN (betamethason 0.5mg/g+Calcipotriol 50mcg/g).
-> Theo NSX, thuốc chưa được nghiên cứu hiệu quả và an toàn ở người dưới 18 tuổi
-
Ca 5: BN Bệnh thận mạn CrCl ~ 24 mL/phút Rx Metformin -> Metformin CCĐ ở eGFR <30 mL/phút/1,73 m2. Cân nhắc đổi sang insulin hoặc linagliptin
-
Ca 6: BN COVID-19 thở O2 mũi Rx Molnupiravir + Remdesivir -> Hiện chưa có bằng chứng về việc phối hợp 2 thuốc kháng virus trong điều trị COVID-19 Khuyến cáo ngưng 1 thuốc
-
Ca 7: Bệnh nhân bị nhiễm Aspergillus phế quản kèm bệnh lao - điều trị cả 2 bệnh 3 tháng. Nội soi kiểm tra lại nấm Aspergillus phế quản: Âm tính (Không phát hiện). Lâm sàng đáp ứng tốt, hết các triệu chứng bệnh. Bác sĩ hỏi thời gian điều trị thuốc kháng nấm bao lâu? Có cân nhắc kéo dài thêm?
-> Thời gian điều trị: phụ thuộc vào vị trí nhiễm trùng, bệnh nền của bệnh nhân và đáp ứng với điều trị. Điều trị bằng thuốc kháng nấm thường được tiếp tục cho đến khi tất cả các dấu hiệu và triệu chứng của nhiễm trùng đã được giải quyết và thường lâu hơn ở những bệnh nhân bị suy giảm miễn dịch kéo dài. Các bất thường trên X quang phải ổn định và các dấu hiệu nhiễm trùng đang hoạt động phải biến mất trước khi ngừng điều trị. Thời gian điều trị tối thiểu là 6 đến 12 tuần, nhưng đối với hầu hết bệnh nhân bị ức chế miễn dịch, liệu pháp kháng nấm sẽ tiếp tục trong nhiều tháng hoặc thậm chí nhiều năm trong một số trường hợp.[QUYẾT ĐỊNH 3429/QĐ-BYT]
- Ca 8: Bệnh nhân B20, Rx Amphotret cho Viêm màng não nấm. Bệnh nhân gặp phản vệ độ 3 khi truyền -> Ngưng thuốc, xử lý theo phác đồ phản vệ. Chuyển sang chế phẩm Ampholip. Rx 7N, bệnh nhân không đủ chi phí điều trị tiếp với Ampholip. Bác sĩ tư vấn bệnh nhân và chuyển sang sử dụng lại chế phẩm Amphotret. BS hội ý DLS về các biện pháp dự phòng phản ứng khi tiêm Amphotericin B.
-> Khuyến cáo từ NSX (Amphot, Amphotret), Uptodate về ADR của Amphotericin B khi tiêm truyền:
ADR khi tiêm truyền: Rét run và sốt, đau đầu, đau cơ hoặc khớp ở mức độ thường gặp (>1/100)
Để giảm phản ứng sốt, rét run có thể Rx paracetamol, kháng histamin, NSAID, corticoid, chống nôn để dự phòng trước khi truyền Amphotericin B
Liều test/thăm dò ban đầu: 1 mg Amphotericin B pha trong 20 mL Glucose 5%, truyền trong 20-30 phút. Theo dõi mạch, nhiệt độ, huyết áp mỗi 30 phút trong 2 giờ (không cần điều trị dự phòng với liều test ban đầu)
Bắt đầu với liều điều trị hằng ngày 0.25 mg/kg cân nặng, sau đó nếu bệnh nhân dung nạp tốt tăng dần đến liều điều trị 1mg/kg cân nặng (trường hợp bệnh nhân gặp ADR với liều thăm dò)
Truyền tĩnh mạch chậm trong 2-4h, có thể kéo dài >6h để giảm độc tính khi truyền
- Ca 9: Bệnh nhân nhiễm nấm xâm lấn, cấy máu (+) nấm sợi, chưa có nấm đồ. BS hỏi điều kiện thanh toán theo BHYT thuốc kháng nấm Voriconazol -> Theo thông tư 20/2022, Quỹ BHYT thanh toán 50% Voriconazol uống trong điều trị:
Nhiễm Asperillus xâm lấn
Nhiễm Candida huyết trên bệnh nhân không giảm bạch cầu;
Nhiễm Candida xâm lấn nặng kháng fluconazol;
Điều trị nhiễm nấm nặng gây bởi Scedosporium spp. và Fusarium spp. cho những bệnh nhân không đáp ứng các điều trị khác
- Ca 10: Bệnh nhân 68 kg, 1m72, 31t. Chẩn đoán: Nhiễm trùng huyết S. aureus MRSA. Rx Vancomycin 1g q8h. SCr = 65 umol/L. Kết quả đo kiểm tra nồng độ Vancomycin đáy: Ctrough = 10.5 ug/mL. BS tiếp tục duy trì liều hiện tại tuy nhiên AUC/MIC có thể < 400 mcg*hr/mL.
-> Khuyến cáo: BS hội ý DLS trong các trường hợp Ctr ≈ 10mg/l. Theo IDSA 2020 và quy trình TDM vancomycin 2020 PK/PD mục tiêu của Vancomycin là AUC/MIC 400-600 mcg*hr/mL không phải Ctrough =10-20mg/L. Bác sĩ điều trị liên hệ DLS để ước tính AUC/MIC và hiệu chỉnh liều.
- Ca 11: BN 17 tháng, 15kg, chuẩn đoán: GERD. Rx: Glesoz (Esomeprazol 20mg dạng viên bao tan trong ruột). NSX khuyến cáo nuốt toàn bộ viên, KHÔNG nhai hoặc nghiền nát viên. Dạng uống không phù hợp cho trẻ 1-2 tuổi.
-> Theo DTQG, NSX: Chế phẩm Esomeprazol dạng bao tan trong ruột, không ổn định trong môi trường acid, nên phải uống nguyên viên nang, không nhai/nghiền. Khuyến cáo Bs chuyển sang dùng Nexium mups 10 (Esomeprozol 10mg) dạng gói chứa vi hạt phân tán được trong nước và có chỉ định cho trẻ nhỏ.
- Ca 12: BN viêm màng não nấm Cryptococcus điều trị giai đoạn củng cố tăng men gan ALT từ 30 -> 210 nghi ngờ do fluconazole. -> Fluconazole có thể gây nhiễm độc gan (từ tăng nhẹ và không có triệu chứng transaminase huyết thanh đến suy gan). Tổn thương gan do fluconazole thường tự khỏi mà không cần can thiệp. Sau khi giảm liều hoặc ngừng tổn thương gan thường có thể hồi phục trong vòng ~ 2 tuần nhưng có thể tái phát khi dùng lại. Tổn thương gan ít gặp hơn với fluconazole so với các azole khác.
-> Tăng transaminase gan hoặc phosphatase kiềm tương đối hiếm khi sử dụng fluconazole 400- 800 mg, chỉ có 1-2% có giá trị >5 lần ULN. Cân nhắc giảm liều fluconazole trong giai đoạn củng cố là 400 mg/ngày, theo dõi CN gan
- Ca 13: BN 12 tuổi, kê đơn Tacrolimus 0.1%. Theo NSX và DTQG, Tacrolimus 0.1% chống chỉ định cho trẻ < 15 tuổi
-> Khuyến cáo Bs chuyển sang dùng Tacrolimus 0.03% có chỉ định cho trẻ ≥ 2 tuổi
- Ca 14: Nhiễm nấm Mucor sp. (Cập nhật số liệu trong năm 2022 đến 18/04/2023):
-> Khuyến cáo điều trị Mucormycosis:
GĐ tấn công: Amphotericin B 1mg/kg q24h
GĐ duy trì: Posaconazol PO ít nhất 7 ngày, liều Posaconazol PO, dạng hỗn dịch 400mg q12h (800mg/ngày) (Sandford Guide, Uptodate)
-> Hướng dẫn sử dụng Posaconazol: Lắc đều chai trước khi uống, mỗi lần uống 2 muỗng (~ 10mL ~ 400mg); nên dùng trong bữa ăn/uống lúc no/bữa ăn giàu chất béo để tăng sinh khả dụng. Nếu không dung nạp, chia nhỏ mỗi cử 1 muỗng (5 mL) x 3-4 lần/ngày (NSX khuyến cáo liều có thể từ 600-800mg/ngày).
-> Lưu ý điều kiện thanh toán BHYT khi đổi sang chế phẩm Ampholip.
-> Voriconazol KHÔNG có phổ trên nấm Mucor sp.
Tương tác thuốc:
BS lưu ý khi có cảnh báo mức độ 5 và có thể chủ động liên hệ DLS hội ý về việc sử dụng chung vì các CẢNH BÁO MỨC ĐỘ 5 LÀ CHỐNG CHỈ ĐỊNH theo Quyết định 5948/QĐ-BYT.
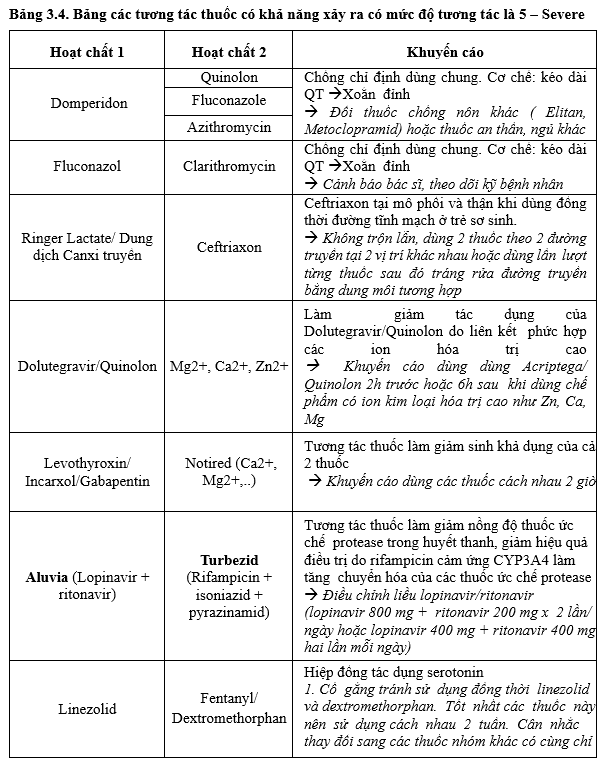
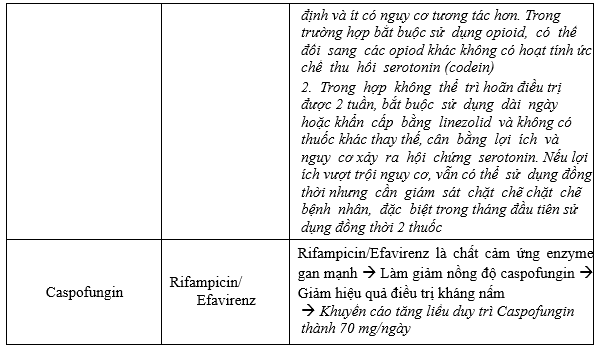
Khuyến cáo Hội đồng thuốc và điều trị - Ban Quản lý sử dụng kháng sinh
Thực hiện lại Quy trình duyệt và cấp phát kháng sinh hạn chế vào ngày 7 sử dụng kháng sinh với các trường hợp sử dụng kháng sinh kéo dài.
4. CHUYÊN ĐỀ: CHIẾN LƯỢC ĐIỀU TRỊ COVID-19 TRONG TÌNH HÌNH MỚI:
Vào ngày 05/05/2023, Tổ chức Y tế Thế giới (World Health Organization, WHO) đã tuyên bố “COVID-19 không còn là tình trạng khẩn cấp toàn cầu và chuyển sang chiến lược phòng ngừa và kiểm soát dài hạn”. Quyết định trên được đưa ra theo xu hướng giảm dần về số ca nhập viện, tử vong do COVID-19 và mức độ miễn dịch cộng đồng ngày càng tăng từ nhiễm trùng và tiêm vaccine COVID-19 [13, 19]. WHO đồng thời nhấn mạnh về tầm quan trọng của việc tiếp tục bảo về đối tượng dễ bị tổn thương nhất (người cao tuổi, người có bệnh nền, người suy giảm miễn dịch, người chưa tiêm vaccin...) – là những đối tượng có nguy cơ cao diễn biến nặng nếu nhiễm bệnh [13, 19].
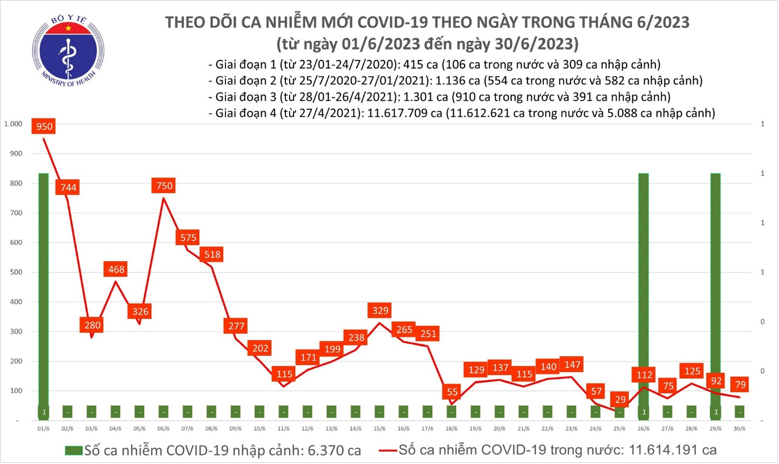
Tại Việt Nam, từ đầu tháng 6, tình hình bệnh nhiễm COVID-19 tăng nhẹ trong cả nước và kịp ứng phó với tình hình này Bộ Y tế đã ban hành Quyết định 2671 “Hướng dẫn chẩn đoán và điều trị COVID-19” ngày 26/6/2023.
Các thuốc điều trị đặc hiệu COVID-19 đã được trình bày trong bản tin dược lâm sàng Quý 1 năm 2022 của Bệnh viện Bệnh Nhiệt đới. Bài viết dưới đây sẽ nhắc lại các nguyên tắc chính trong dùng thuốc điều trị COVID-19 và cập nhật một số thông tin mới về các liệu pháp điều trị.
4.1 Nguyên tắc dùng thuốc điều trị COVID-19
Cơ chế bệnh sinh của COVID-19 được cho là trải qua hai pha: pha virus và pha viêm. Ở pha virus, cơ chế bệnh sinh chủ yếu do sự nhân đôi của virus. Ở pha viêm, cơ chế bệnh sinh do đáp ứng viêm/ điều hòa miễn dịch với nhiễm trùng, có thể dẫn tới tổn thương mô sâu và huyết khối [2, 4]. Đa số bệnh nhân không tiến triển sang pha viêm (mức độ bệnh từ nặng - nguy kịch), ngoại trừ người có yếu tố nguy cơ cao (cao tuổi, chưa tiêm vaccine COVID-19, có bệnh nền...) [16].

Do đó, các liệu pháp tác động trực tiếp trên SARS-CoV-2 (thuốc kháng virus, kháng thể trung hòa virus, huyết tương từ người khỏi bệnh) được cho là có hiệu quả tối ưu vào giai đoạn sớm của bệnh; trong khi các liệu pháp điều hòa miễn dịch, kháng viêm, chống đông có nhiều lợi ích hơn ở giai đoạn sau của bệnh (đặc trưng bởi thiếu oxy máu và rối loạn chức năng nội mô) [2, 4].
Đối với bệnh nhân mức độ nhẹ - trung bình, phần lớn chỉ cần kiểm soát triệu chứng mà không cần các điều trị đặc hiệu. Tuy nhiên, nếu bệnh nhân có các yếu tố nguy cơ cao tiến triển nặng, bệnh nhân nên được điều trị sớm (trong vòng 5-7 ngày kể từ khi khởi phát triệu chứng) bằng các thuốc tác động đặc hiệu trên SARS-CoV-2. Việc lựa chọn các thuốc này phụ thuộc vào nhiều yếu tố [2, 4, 14], bao gồm:
• Hiệu quả lâm sàng (qua các nghiên cứu lâm sàng)
• Tính sẵn có tại cơ sở điều trị
• Nguy cơ tương tác thuốc nghiêm trọng (VD: nirmatrelvir/ritonavir)
• Tính khả thi khi sử dụng đường dùng tĩnh mạch (VD: remdesivir, kháng thể trung hòa)
• Tình trạng mang thai của bệnh nhân (VD: phụ nữ có thai không nên dùng molnupiravir)
• Thời gian kể từ lúc khởi phát triệu chứng (time from symptom onset)
• Hoạt tính in vitro với các biến thể SARS-CoV-2 đang lưu hành
Ở bệnh nhân suy giảm miễn dịch nặng, pha virus có thể kéo dài dẫn đến virus tiến hóa nhanh chóng và hình thành đột biến kháng thuốc. Kéo dài thời gian điều trị hoặc phối hợp thuốc được gợi ý nhằm hạn chế nguy cơ kháng thuốc ở nhóm đối tượng này; tuy nhiên vẫn chưa có bằng chứng về lợi ích của các biện pháp này [2, 4].
4.2 Kháng thể trung hòa virus
Kháng thể trung hòa virus có tác động ức chế virus bằng cách gắn kết với protein gai của SARS-CoV-2, từ đó ngăn chặn virus xâm nhập và tấn công tế bào người. Các thuốc này đã cho thấy lợi ích lâm sàng trong:
• Điều trị bệnh nhân COVID-19 mức độ nhẹ - trung bình có nguy cơ cao tiến triển nặng: bamlanivimab/etesevimab, casirivimab/imdevimab, sotrovimab, và bebtelovimab
• Dự phòng sau phơi nhiễm: bamlanivimab/etesevimab và casirivimab/imdevimab
• Dự phòng trước phơi nhiễm: tixagevimab/cilgavimab [2, 4].
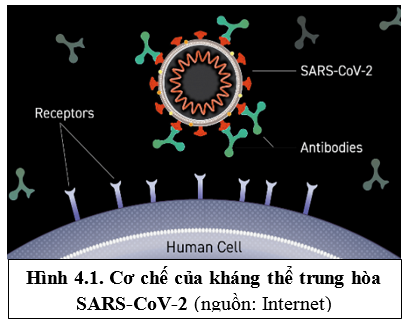
Tuy nhiên, SARS-CoV-2 thường có xu hướng biến đổi, hình thành các biến thể mới và trở nên không còn nhạy cảm với các kháng thể trung hòa hiện có. Cụ thể tại Hoa Kỳ, kết quả in vitro cho thấy các kháng thể trung hòa hiện có đã mất hoặc giảm đáng kể hoạt tính với các biến thể đang lưu hành (các biến thể phụ của Omicron). Do đó hiện nay, Viện Y tế Quốc gia Hoa Kỳ (National Institutes of Health, NIH) và WHO khuyến cáo không sử dụng các kháng thể trung hòa này trong điều trị và dự phòng COVID-19. Ngoài ra, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (Food and Drug Administration, FDA) cũng đã thu hồi cấp phép sử dụng khẩn cấp (Emmergency Use Authorizations, EUA) các kháng thể trung hòa trên [2, 4, 14].
Các kháng thể trung hòa này vẫn có thể được cân nhắc sử dụng ở khu vực địa lý đang lưu hành các biến thể SARS-CoV-2 vẫn còn nhạy cảm với các thuốc này [4].
4.3 Thuốc kháng virus
Hiện nay, nirmatrelvir/ritonavir, remdesivir và molnupiravir là ba thuốc kháng virus được khuyến cáo trong điều trị COVID-19, mức độ nhẹ - trung bình. Trong đó, remdesivir là thuốc duy nhất được khuyến cáo ở bệnh nhân COVID-19 mức độ nặng. Hiện vẫn chưa có khuyến cáo về phối hợp các thuốc kháng virus trong điều trị COVID-19 [2, 4, 14].
Khác với các kháng thể trung hòa, các thuốc kháng virus có nhiều khả năng vẫn giữ được hoạt tính với biến thể Omicron và các biến thể phụ của Omicron [2, 18].
4.3.1. Remdesivir
Tuy bản chất là thuốc kháng virus, remdesivir ban đầu được nghiên cứu và khuyến cáo sử dụng trên bệnh nhân COVID-19 nhập viện, mức độ trung bình – nặng, qua nhiều nghiên cứu như ACTT-1, WHO Solidarity…. Kể từ thử nghiệm PINETREE (2022), remesivir được mở rộng chỉ định trên bệnh nhân COVID-19 ngoại trú mức độ nhẹ-trung bình có nguy cơ cao tiến triển bệnh nặng [2, 4]
PINETREE là một thử nghiệm lâm sàng Pha 3 ngẫu nhiên, mù đôi, có nhóm chứng đánh giá an toàn và hiệu quả của liệu trình Remdesivir tĩnh mạch 3 ngày trên 562 bệnh nhân COVID-19 ngoại trú thỏa các tiêu chí:
• Khởi phát triệu chứng trong vòng 7 ngày
• Chưa tiêm vaccine COVID-19 và
• Có ít nhất 1 yếu tố nguy cơ cao tiến triển bệnh nặng (VD béo phì, đái tháo đường, tăng huyết áp, suy giảm miễn dịch…) hoặc tuổi từ 60 trở lên.
-> Tiêu chí đánh giá chính: nhập viện liên quan đến COVID-19 hoặc tử vong do mọi nguyên nhân trước ngày 28.
-> Kết quả cho thấy remdesivir làm giảm 87% nguy cơ nhập viện so với giả dược (số ca nhập viện do COVID-19 là 2 (0,7%) ở nhóm remdesivir và 15 (5,3%) nhóm giả dược (HR=0,13; 95% CI: 0,03-0,59, p=0,008). Lợi ích về tử vong của remdesivir chưa rõ ràng vì không ghi nhận trường hợp nào tử vong ở cả hai nhóm dùng remdesivir và giả dược. Về an toàn, remdesivir dung nạp khá tốt: biến cố có hại gặp ở 42,3% bệnh nhân dùng remdesivir và 46,3% bệnh nhân dùng giả dược [8].
Trong ba thuốc kháng virus được khuyến cáo trong điều trị COVID-19, remdesivir là thuốc duy nhất dùng đường tiêm truyền tĩnh mạch và bệnh nhân cần được theo dõi chặt trong quá trình truyền thuốc và ít nhất 1 giờ sau khi truyền. Liều dùng ở người lớn bao gồm 1 liều nạp 200 mg vào ngày đầu, sau đó duy trì 100 mg/ngày vào các ngày tiếp theo.

4.3.2 Molnupiravir
Ngày 23/12/2021, FDA Hoa Kỳ cấp phép sử dụng khẩn cấp molnupiravir ở bệnh nhân COVID-19 mức độ nhẹ-trung bình có nguy cơ cao tiến triển bệnh nặng, chủ yếu dựa trên kết quả từ nghiên cứu nền tảng MOVe-OUT (molnupiravir làm giảm 31% nguy cơ nhập viện/ tử vong) [10].
Vào cuối năm 2022, một thử nghiệm lâm sàng ngẫu nhiên có đối chứng (randomized controlled trial, RCT) khác về monulpiravir - thử nghiệm PARONAMIC – được công bố. Tính tới nay, đây là RCT lớn nhất về thuốc kháng virus mới trong điều trị COVID-19. So với MOVe-OUT, PANORAMIC liên quan nhiều hơn với thực hành điều trị hiện tại, với mẫu bệnh nhân có tính đại diện hơn: hầu hết đã được tiêm vaccine COVID-19 và nhiễm biến thể Omicron [2, 5].

Do thực hiện trên mẫu bệnh nhân có miễn dịch cao hơn, tỷ lệ nhập viện hoặc tử vong trong nghiên cứu PANORAMIC thấp hơn nghiên cứu MOVe-OUT. PANORAMIC cho thấy molnupiravir không làm giảm nguy cơ nhập viện/ tử vong vốn đã thấp, nhưng có thể đẩy nhanh thời gian hồi phục (cải thiện triệu chứng) ở bệnh nhân [2]. PANORAMIC là nghiên cứu nhãn mở (bệnh nhân biết họ có được dùng molnupiravir hay không) nên có thể ảnh hưởng đến việc báo cáo triệu chứng của bệnh nhân [2, 5].
4.3.3. Nirmatrelvir/ritonavir
Nirmatrelvir ức chế enzyme 3C-like protease (3CLpro/ Mpro) của SARS-CoV2. Ritonavir ức chế men gan CYP450 phân hủy của Nirmatrelvir do đó kéo dài thời gian tác dụng và tăng nồng độ của Nirmatrelvir. Thuốc được phát triển bời công ty Pfizer và được FDA cấp phép. Thử nghiệm EPIC-HR với n = 2246, trên bệnh nhân COVID-19 ngoại trú mức độ nhẹ-trung bình có nguy cơ cao tiến triển bệnh nặng, ≥ 18 tuổi và khởi phát triệu chứng trong vòng 5 ngày. Kết quả cho thấy giảm nguy cơ nhập viện/tử vong 88% (p < 0,0001) trong vòng 5 ngày khởi phát triệu chứng và 89% trong vòng 3 ngày khởi phát triệu chứng.
Bộ Y tế khuyến có sử dụng Nirmatrelvir/ritonavir như sau:
-
Chỉ định: Người bệnh COVID-19 người lớn và trẻ em từ 12 tuổi trở lên có cân nặng ít nhất 40kg mức độ nhẹ, trung bình và có ít nhất 1 nguy cơ cao tiến triển thành bệnh nặng (bao gồm nhập viện và tử vong). Sử dụng trong vòng 5 ngày kể từ khi khởi phát các triệu chứng hoặc khi có xét nghiệm dương tính.
-
Liều dùng:
-
Mức lọc cầu thận eGFR ≥ 60 mL/phút: 300mg nirmatrelvir (2 viên 150mg) uống đồng thời cùng 100mg ritonavir (1 viên 100 mg), x 2 lần/ngày. Thời gian điều trị: 05 ngày.
-
Mức lọc cầu thận eGFR ≥ 30 đến 60 mL/phút: 150mg nirmatrelvir (1 viên 150mg) uống đồng thời cùng 100mg ritonavir (1 viên 100 mg), x 2 lần/ngày.
-
Nếu eGFR <30mL/min hoặc suy gan nặng (ChildPugh C): không khuyến cáo
-
Chú ý các tương tác thuốc nghiêm trọng hoặc chống chỉ định thông qua ức chế CYP3A4. Không khuyến cáo sử dụng cho người bệnh suy gan nặng, suy thận nặng.
4.3.4. Tổng hợp về thuốc kháng virus
Mặc dù chưa có nghiên cứu so sánh trực tiếp giữa các liệu pháp kháng virus, molnupiravir có vẻ như kém hiệu quả hơn các thuốc khác (bảng 4.4).

Hiện tại, molnupiravir đang được khuyến cáo là liệu pháp thay thế: chỉ sử dụng khi không thể sử dụng được nirmatrelvir-ritonavir và remdesivir [2, 4, 14]. Bằng chứng trên bệnh nhân ít nguy cơ diễn tiến nặng (VD: bệnh nhân đã tiêm vaccine COVID-19) vẫn còn hạn chế (bảng 4). Do đó, ở bệnh nhân mức độ nhẹ-trung bình, điều trị đặc hiệu bao gồm các thuốc kháng virus chỉ nên áp dụng cho đối tượng có nguy cơ cao tiến triển nặng.
Hiện tượng rebound COVID-19: Hiện tượng rebound COVID-19 được ghi nhận sau khi kết thúc đợt điều trị thuốc kháng virus, đặc trưng bởi sự tăng trở lại nồng độ SARS-CoV2 tại dịch hầu họng (dương trở lại của test PCR) và/hoặc xuất hiện lại các triệu chứng. Rebound đã được báo cáo sau khi ngưng molnupiravir và nirmatrelvir/ritonavir, xuất hiện trong khoảng 2-8 ngày sau khi bệnh nhân đã phục hồi lần đầu. Trong nghiên cứu lâm sàng, rebound COVID-19 xuất hiện ở cả bệnh nhân dùng thuốc và bệnh nhân dùng giả dược. Cho tới nay, rebound sau khi ngưng thuốc kháng virus chưa cho thấy có liên quan đến nguy cơ tiến triển thành mức độ bệnh nặng, nhập viện, hoặc tử vong [2]. Trung tâm kiểm soát và phòng ngừa dịch bệnh Hoa Kỳ (CDC) khuyến cáo bệnh nhân xuất hiện rebound cần tuân thủ biện pháp tái cách ly ít nhất 5 ngày và không cần thiết điều trị lại các thuốc kháng virus. Để quản lý hiện tượng rebound, cần có thêm dữ liệu về tần suất, cơ chế, yếu tố nguy cơ cũng như ý nghĩa lâm sàng của hiện tượng này [6, 15].
4.4 Liều của corticosteroids trong điều trị bệnh nhân COVID-19
Corticosteroid đường dùng toàn thân là liệu pháp đầu tiên cho thấy giảm tử vong ở bệnh nhân COVID-19 nhập viện cần bổ sung oxy và đã trở thành điều trị tiêu chuẩn cho nhóm bệnh nhân này [2, 4, 12, 14].
Chế độ liều tối ưu của corticosteoid trong điều trị COVID-19 vẫn chưa rõ ràng. Liều dùng 6mg x 1 lần/ngày dexamethasone trong theo thử nghiệm nền tảng RECOVERY (2020) được lựa chọn dựa theo kinh nghiệm trong điều trị đợt cấp hen và bệnh phổi tắc nghẽn mãn tính (COPD) [3]. Cho tới nay, khuyến cáo của NIH, WHO và Hội bệnh truyền nhiễm Hoa Kỳ (Infectious Disease Society of America, IDSA) về chế độ liều dexamethasone vẫn là 6mg/ngày với mọi mức độ bệnh COVID-19 [2, 4, 14].
Một số nghiên cứu sau đó cho thấy tỷ lệ tử vong giảm hơn nữa khi phối hợp corticosteroid và một thuốc ức chế miễn dịch thứ hai như: chẹn thụ thể interleukin-6 (tocilizumab) hoặc chất ức chế Janus kinase (baricitinib). Do đó, tăng liều corticosteroid đơn thuần - thay vì phối hợp corticosteroid với các thuốc ức chế miễn dịch khác - được gợi ý rằng là một hướng đi giúp tăng lợi ích điều trị và tiết kiệm chi phí, nhất là ở các khu vực có nguồn lực hạn chế.
Đã có các nghiên cứu so sánh các liều khác nhau của corticosteroid ở bệnh nhân COVID-19, với kết quả không nhất quán [2]. Trong đó, hai nghiên cứu lớn nhất là COVID STEROID 2 và RECOVERY (2023).
• COVID STEROID 2 so sánh dexamethasone 12mg/ngày và dexamethasone 6 mg/ngày ở bệnh nhân COVID-19 cần bổ sung O2 ít nhất 10L/phút hoặc thở máy. Mặc dù các kết quả cuối cùng không cho thấy khác biệt có ý nghĩa thống kê giữa hai chế độ liều, phân tích theo phương pháp Bayesian gợi ý liều 12mg/ngày có thể mang lại nhiều lợi ích hơn, nhất là trên bệnh nhân nặng hơn (cần bổ sung mức độ O2 cao hơn) [17].
• RECOVERY (2023) so sánh dexamthasone liều cao (20 mg/ngày x 5 ngày đầu, 10 mg/ngày x 5 ngày) với dexamethasone 6 mg/ngày ở bệnh nhân COVID-19 nhập viện có bằng chứng lâm sàng về giảm Oxy. Phân tích định kỳ trên nhóm bệnh nhân COVID-19 không nguy kịch - không cần bổ sung Oxy hoặc chỉ cần bổ sung liệu pháp Oxy đơn giản - cho thấy dexamethasone liều cao làm tăng 60% nguy cơ tử vong so dexamethasone 6mg/ngày. Vì lý do an toàn, nghiên cứu đã ngưng tuyển bệnh ở nhóm bệnh nhân này. Việc tuyển bệnh ở nhóm cần liệu pháp Oxy không xâm lấn và xâm lấn vẫn tiếp tục [3].
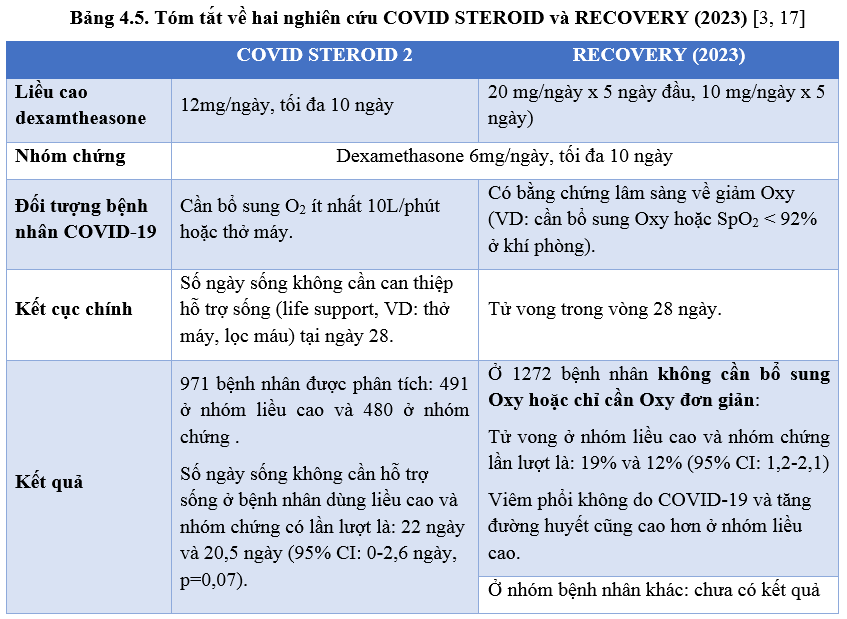
Các phân tích này củng cố thêm giả định về vai trò kháng viêm của dexamethasone trong điều trị COVID-19. Dùng liều cao dexamethasone ở giai đoạn sớm – khi cơ chế bệnh đang ở pha nhân đôi virus – gây hại nhiều hơn lợi vì có thể làm chậm sự thải trừ virus ra khỏi cơ thể.
4.5 Chất ức chế SGLT2 (empagliflozin, dapagliflozin)
Bệnh COVID-19 mức độ nặng đặc trưng bởi viêm và suy đa cơ quan. Nhóm bệnh nhân COVID-19 có hội chứng chuyển hóa (cardiometabolic) - như đái tháo đường type 2, bệnh tim mạch, và bệnh thận - có yếu tố nguy cơ cao tiến triển bệnh nặng, nhập viện và tử vong [16].

Nhiều nghiên cứu lớn đã cho thấy các chất nhóm thuốc ức kênh đồng vận chuyển Natri-glucose-2 (SGLT2i) làm giảm các biến cố tim mạch và thận ở bệnh nhân đái tháo đường type 2, bệnh tim mạch và bệnh thận. Trong trường hợp COVID-19, SGLT2i có thể giảm viêm, cải thiện chức năng nội mạch và tạo môi trường năng lượng kém thuận lợi cho sự phát triển của SARS-CoV-2. Mặc dù vẫn chưa rõ về cơ chế chính xác, các lợi ích trên được tin là có thể giúp ngăn ngừa tổn thương đa cơ quan và cải thiện cơ hội sống sót ở bệnh nhân COVID-19 [9, 11].
Hai thuốc dapagliflozin và empagliflozin được lần lượt nghiên cứu về hiệu quả và an toàn trên bệnh nhân COVID-19 qua hai thử nghiệm DARE-19 và RECOVERY. Hai thử nghiệm lớn này không ủng hộ việc sử dụng dapagliflozin và empagliflozin trong điều trị bệnh nhân COVID-19 nhập viện. Hai thuốc trên được dung nạp khá tốt trong bệnh cấp tính và có thể không cần ngưng nếu có chỉ định phù hợp [9, 11].
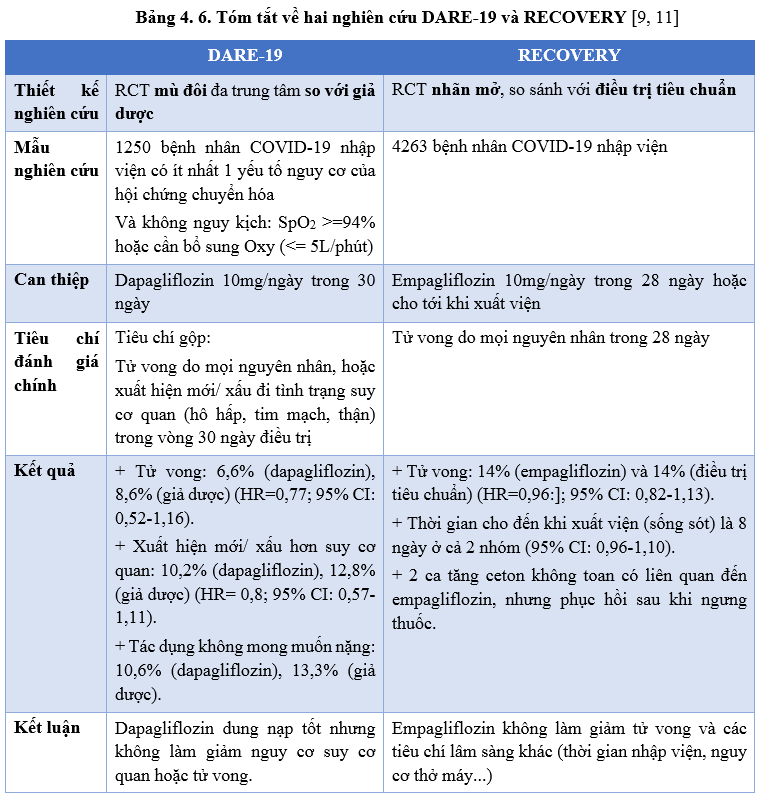
Kể từ chùm ca bệnh COVID-19 đầu tiên tại Vũ Hán (Trung Quốc) cuối năm 2019, kiến thức về COVID-19 - từ cơ chế bệnh sinh đến các liệu pháp điều trị và các bài học trong phòng chống dịch - đã và đang được tích lũy dần. Tuy nhiên hiện vẫn còn nhiều vấn đề cần được nghiên cứu thêm như: vai trò thực sự của các thuốc kháng virus trên bệnh nhân đã tiêm vaccine COVID-19 (tính hiệu quả - kinh tế), hiện tượng rebound sau khi ngưng thuốc kháng virus và hướng xử trí, liều tối ưu của corticosteroid ở bệnh nhân COVID-19 mức độ nặng - nguy kịch, cơ chế và cách xử trí tình trạng COVID-19 kéo dài (long COVID), ý nghĩa lâm sàng nếu đồng nhiễm COVID-19 và cúm mùa... Tại Việt Nam, COVID-19 đang trong giai đoạn chuyển từ bệnh truyền nhiễm nhóm A sang nhóm B; việc nâng cao hiểu biết là cần thiết để xây dựng kế hoạch kiểm soát quản lý bền vững COVID-19 trong tình hình mới [1]. Hướng dẫn điều trị mới cập nhật ngày 26/6/2023 của Bộ Y tế cũng đã kịp thời thay đổi phù hợp với những nghiên cứu và khuyến cáo trên thế giới về thuốc điều trị đặc hiệu COVID-19 đối với thuốc kháng thể đơn dòng kháng virus COVID-19 và favipiravir đã không còn được khuyến cáo; đồng thời bổ sung thuốc ức chế Janus Kinase là Barcitini chỉ định cho người bệnh ≥ 2 tuổi phải thở oxy, NIV, MV hoặc ECMO.
Ngoài ra, tiêm ngừa vaccine COVID-19 vẫn là biện pháp dự phòng hiệu quả và an toàn, giúp giảm nguy cơ mắc bệnh COVID-19, tiến triển bệnh nặng, nhập viện hoặc tử vong. Hiệu quả bảo vệ của vaccine sẽ giảm dần theo thời gian, để đạt được bảo vệ lâu dài, người dân nên tiêm nhắc lại vaccine COVID-19 sau một thời gian tiêm các mũi cơ bản. Người trên 65 tuổi và người suy giảm miễn dịch mức độ trung bình-nặng có thể cần nhiều lần tiêm nhắc lại hơn. Mặc dù vaccine COVID-19 có thể liên quan đến một số phản ứng có hại nặng như: viêm cơ tim (myocarditis), viêm màng ngoài tim (pericarditis), giảm tiểu cầu huyết khối (thrombotic thrombocytopenia), các phản ứng này nhìn chung là hiếm gặp và thường có thể điều trị được hoặc tự giải quyết theo thời gian [7]. Mỗi người dân nên có ý thức cập nhật về tình hình mũi vaccine mới nhất có sẵn tại địa phương và tham vấn thêm ý kiến từ nhân viên y tế để chủ động phòng ngừa cho chính mình và xã hội.
DS. Hà Thị Cẩm Tú
TÀI LIỆU THAM KHẢO
- Bộ trưởng Y tế: 'Xem xét chuyển Covid thành bệnh thông thường cuối tuần này" (cập nhật 30/05/2023). Available: https://vnexpress.net/bo-truong-y-te-xem-xet-chuyen-covid-thanh-benh-thong-thuong-cuoi-tuan-nay-4611209.html, truy cập 09/06/2023.
- National Institutes of Health. Coronavirus Disease 2019 (NIH) Treatment Guidelines (cập nhật 20/04/2023). Available: https://www.covid19treatmentguidelines.nih.gov/, truy cập 09/06/2023.
- Abani Obbina, Abbas Ali, Abbas Fatima, et al. (2023), "Higher dose corticosteroids in patients admitted to hospital with COVID-19 who are hypoxic but not requiring ventilatory support (RECOVERY): a randomised, controlled, open-label, platform trial", 401(10387), pp. 1499-1507.
- America Infectious Diseases Society of, "IDSA Guidelines on the Treatment and Management of Patients with COVID-19," ed: Arlington, VA: Infectious Diseases Society of America. (Updated 2023 May 15), 2023.
- Butler Christopher C, Hobbs FD Richard, Gbinigie Oghenekome A, et al. (2023), "Molnupiravir plus usual care versus usual care alone as early treatment for adults with COVID-19 at increased risk of adverse outcomes (PANORAMIC): an open-label, platform-adaptive randomised controlled trial", 401(10373), pp. 281-293.
- Centers for Disease Control and Prevention (2022), COVID-19 Rebound After Paxlovid Treatment. Available: https://emergency.cdc.gov/han/2022/pdf/CDC_HAN_467.pdf
- Centers for Disease Control and Prevention (2023), "Stay Up to Date with Vaccines",(cập nhật 07/06/2023) available at: https://www.cdc.gov/coronavirus/2019-ncov/vaccines/stay-up-to-date.html
- Gottlieb Robert L, Vaca Carlos E, Paredes Roger, et al. (2022), "Early remdesivir to prevent progression to severe Covid-19 in outpatients", 386(4), pp. 305-315.
- Horby Peter W, Staplin Natalie, Peto Leon, et al. (2023), "Empagliflozin in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial", pp. 2023.04. 13.23288469.
- Jayk Bernal Angélica, Gomes da Silva Monica M, Musungaie Dany B, et al. (2022), "Molnupiravir for oral treatment of Covid-19 in nonhospitalized patients", 386(6), pp. 509-520.
- Kosiborod Mikhail N, Esterline Russell, Furtado Remo HM, et al. (2021), "Dapagliflozin in patients with cardiometabolic risk factors hospitalised with COVID-19 (DARE-19): a randomised, double-blind, placebo-controlled, phase 3 trial", 9(9), pp. 586-594.
- Medicine RECOVERY Collaborative Group %J New England Journal of (2021), "Dexamethasone in hospitalized patients with Covid-19", 384(8), pp. 693-704.
- World Health Organization, "Statement on the fifteenth meeting of the IHR (2005) Emergency Committee on the COVID-19 pandemic," in 2023-05-05) [2023-05-18]. https://www. who. int/news/item/05-05-2023-statement-on-the-fifteenth-meeting-of-the-international-health-regulations, 2023.
- World Health Organization, "Therapeutics and COVID-19: living guideline, 13 January 2023," World Health Organization2023.
- Parums Dinah V %J Medical Science Monitor (2022), "Rebound COVID-19 and cessation of antiviral treatment for SARS-CoV-2 with paxlovid and molnupiravir", 28.
- Centers for Disease Control and Prevention. Underlying Medical Conditions, (cập nhật 15/06/2023). Available: https://www.cdc.gov/coronavirus/2019-ncov/hcp/clinical-care/underlyingconditions.html
- Russell Lene, Uhre Kis Rønn, Lindgaard Ann Louise Syraach, et al. (2021), "Effect of 12 mg vs 6 mg of dexamethasone on the number of days alive without life support in adults with COVID-19 and severe hypoxemia: the COVID STEROID 2 randomized trial", 326(18), pp. 1807-1817.
- Vangeel Laura, Chiu Winston, De Jonghe Steven, et al. (2022), "Remdesivir, Molnupiravir and Nirmatrelvir remain active against SARS-CoV-2 Omicron and other variants of concern", 198, pp. 105252.
- Wise Jacqui, "Covid-19: WHO declares end of global health emergency," ed: British Medical Journal Publishing Group, 2023.