1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
Quý 2-2019 ghi nhận có 18 báo cáo ADR xảy ra ở 8 khoa (theo bảng). Trong đó khoa Nhiễm B (6 ca), Nhiễm A (3 ca), các khoa còn lại có báo cáo nhưng ít, tất cả đều được xử trí kịp thời. Số lượng báo cáo ADR Quý 2-2019 (18 báo cáo) nhiều hơn với Quý 1-2019 (10 báo cáo). Trong Quý 2, khoa Dược thực hiện báo cáo Tổng kết hoạt động ADR và thông tin thuốc năm 2018.
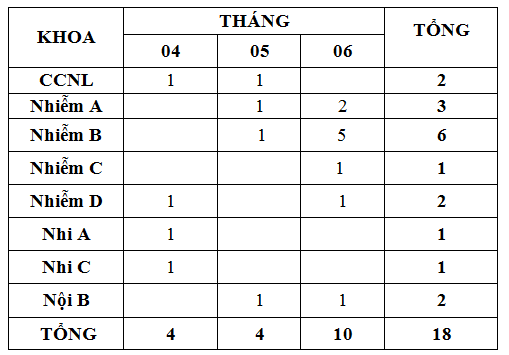
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
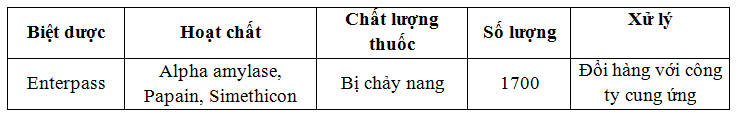
- THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần : THÔNG TIN THUỐC
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 1-2018
1.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 212 HSBA nội trú và 1207 toa thuốc ngoại trú. Ngoài ra, đơn vị dược lâm sàng cũng thực hiện 80 trường hợp hội ý/hội chẩn với các khoa lâm sàng trong quá trình điều trị (36 trường hợp hội ý qua điện thoại được ghi nhận trong sổ). Chủ yếu là hội chẩn về liều kháng sinh (đặc biệt là TDM Vancomycin 48/80 trường hợp, TDM Aminoglycosid 7 ca), phối hợp kháng sinh và tư vấn thông tin thuốc.
Bên cạnh đó, đơn vị dược lâm sàng thực hiện 278/1463 (khoảng 19% < 30% của Quý 1-2019) can thiệp trong quá trình điều trị thuốc để kịp thời hỗ trợ công tác điều trị của bác sỹ. Trong 278 can thiệp, có 254 ( 91% < 97% so với Quý 2-2019) trường hợp được thực hiện kịp thời (chỉnh liều và cảnh báo tương tác thuốc). Quý 2-2019, ghi nhận các can thiệp của dược lâm sàng đều được sự thống nhất ý kiến của bác sỹ.
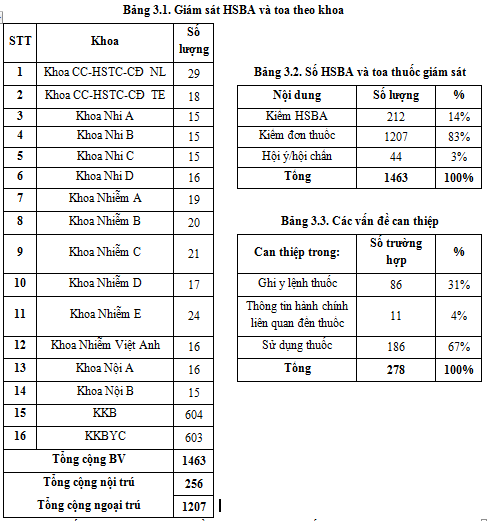
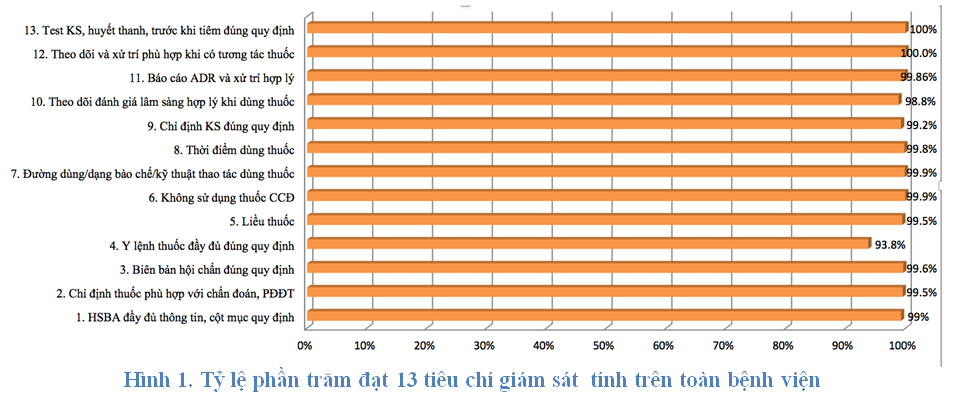
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
Toàn bệnh viện đạt 13 tiêu chí về sử dụng thuốc khoảng > 93% (tăng so với quý 1 -2019 là 86%) vì tiêu chí Y lệnh thuốc tăng; các tiêu chí đánh giá khác đều duy trì tương tự Quý 1-2019 (y lệnh thuốc chưa đúng quy định (KKBYC, Nhi D), báo cáo ADR chưa đầy đủ và kịp thời (CCNL, Nhiễm E), liều thuốc chưa phù hợp (CCNL, Nhiễm B), ngưng hoặc chuyển đổi kháng sinh chưa ghi rõ lý do (Nhiễm B), lưu ý hội chẩn khi sử dụng từ 3 kháng sinh trở lên, chia giờ sử dụng thuốc chưa hợp lý (Nhiễm A, tuy nhiên đã điều chỉnh từ tháng 6-7 của quý))


3.3. Khuyến cáo dược lâm sàng:
Thực hiện Hướng dẫn sử dụng kháng sinh mới và làm Phiếu yêu cầu Kháng sinh hạn chế, Ban QLSDKS có lưu ý sau: - Phân tầng nhóm nguy cơ ghi vào HSBA. Một số HSBA chưa phân tầng nhóm nguy cơ bệnh nhân khi dùng kháng sinh.
-
Ghi các thông tin cận lâm sàng, chẩn đoán hình ảnh cần cho việc duyệt kháng sinh (Công thức máu, SCr,…); đề nghị BS trưởng khoa duyệt nếu có kết quả bồ sung vào phần ý kiến.
-
Hội chẩn BS VS/DLS khi sử dụng từ 3 KS trở lên
-
Lưu ý những trường hợp không cần thiết sử dụng kháng sinh do bệnh cảnh phân biệt với nhiễm trùng (lymphoma, bạch cầu cấp), phân tầng sai do không đánh giá SOFA đúng.
-
Các trường hợp phối hợp azithromycin, khuyến cáo ngưng Azithromycin khi lâm sàng không đáp ứng nếu dùng azithromycin trước, hoặc khi có KQ vi sinh và KSĐ, hoặc đủ liệu trình của azithromycin. Thời gian dùng azithromycin cho viêm phế quản, viêm họng, viêm phổi là 3-5 ngày. Kháng sinh khác nên đánh giá lâm sàng ổn định có thể ngưng dùng ở ngày thứ 7.
Vẫn còn nhập sai tên thuốc và y lệnh (KKBYC và KKB: 78 đơn thuốc < 216 đơn thuốc Quý 1-2019) có cải thiện rõ rệt.
Thời gian chia các cử thuốc chưa phù hợp (Nhiễm A) khuyến cáo chia cử thuốc ngày 2 lần là 10h -20h hoặc khoảng cách liều là 12h.
Sử dụng thuốc chưa theo phác đồ :
-
Điều trị viêm dạ dày, Hp(+) dùng Augmentin (Amoxicillin + acid clavulanic) là không phù hợp;
-
Phác đồ điều trị giun sán còn trường hợp kê toa lập lại nhiều lần ivecmertin uống cách tuần sau khi đã điều trị là không đúng với hướng dẫn của HĐT&ĐTr.
-
Điều trị Hp (+) theo phác đồ điều trị là 2 tuần.
Ghi y lệnh thuốc hướng thần và gây nghiện; thuốc kháng sinh đúng quy định và đánh số ngày sử dụng (Nhiễm C, Nội B, CCNL, CCTE, Nhiễm E)
Khuyến cáo về liều điều trị:
-
Khuyến cáo các thuốc thuộc nhóm PPI nên được uống trước ăn 30 phút để đạt hiệu quả điều trị. PPIs dạng chế phẩm viên bao tan trong ruột không dùng được qua ống thông dạ dày Khuyến cáo dùng các chế phẩm PPIs tiêm hoặc các chế phẩm dạng viên bao chứa vi hạt tan trong ruột. Ví dụ: Nexium mups
-
Khuyến cáo khi kê đơn thuốc lưu ý hàm lượng và dạng dùng để có chế độ liều chính xác, đặc biệt chú ý kê đơn thuốc đúng quy định khi sao chép y lệnh trước.
-
Khuyến cáo Tritenol Fort uống trước ăn 30-60 phút hoặc trước khi ngủ;
-
Domperidone uống trước ăn 15-30 phút.
-
Liều Cotrim trong điều trị Stenotrophomonas maltophilia là 15-20 mg/kg/ngày chia 3-4 lần tính theo trimethoprim (thường tương đương liều 2 viên 960mg q8h).
-
Lưu ý liều của các chế phẩm kẽm trong tiêu chảy nhiễm trùng ở các độ tuổi của trẻ:
Trẻ em < 6 tháng tuổi: 10mg kẽm/ngày
Trẻ em từ 6 tháng trở lên: 20mg/ngày
Tương tác thuốc:
- Có 1 tương tác xảy ra (mức độ 4) có ảnh hưởng trên bệnh nhân. Cần thận trọng ở bệnh nhân sử dụng nhiều thuốc và bệnh nhân sử dụng thuốc tự có, không được cảnh báo trên phần mềm quản lý của bệnh viện.

- Lưu ý những tương tác thuốc mức độ 5. (KKBYC: Efavirenz gây cảm ứng mạnh isoenzymes CYP450 Giảm nồng độ velpatasvir huyết Chống chỉ định Khuyến cáo đổi thuốc điều trị viêm gan C khác).
Pha và truyền thuốc:
- Cần ghi cách pha thuốc viên sủi (Notired) khi kê đơn
4. CHUYÊN ĐỀ: ỨNG DỤNG CÔNG CỤ CẢNH BÁO TƯƠNG TÁC THUỐC TRÊN EHOSPITAL – GIẢI PHÁP PHÒNG NGỪA
Tương tác thuốc – thuốc (Drug drug interaction – DDI) chỉ sự ảnh hưởng của thuốc này với thuốc khác trong cơ thể bệnh nhân dẫn đến tăng/giảm hiệu quả/độc tính của các thuốc. DDI có thể là nguyên nhân gây ra các các phản ứng có hại của thuốc (ADR), những tác dụng này có thể dự đoán khả năng xuất hiện và phòng tránh được. Theo các nghiên cứu đã được công bố:
Đối với bệnh nhân ngoại trú cho thấy tỷ lệ ADR gây ra bởi DDI khoảng từ 2-50%.
Tần suất xuất hiện của các pDDI (potential DDI – tương tác thuốc – thuốc có nguy cơ xảy ra) ước tính dao động từ 15-45% đối với bệnh nhân nội trú.
DDI làm tăng thời gian nằm viện và chi phí điều trị.
FDA cũng đưa ra khuyến cáo về Tương tác thuốc năm 2016: DDI đóng góp từ 3-4% tỷ lệ ADR, nguyên nhân thứ 4 dẫn đến tử vong. Và theo một nghiên cứu tổng hợp từ 23 nghiên cứu về tương tác thuốc, DDI chịu trách nhiệm cho: 0.05% tỷ lệ nhập khoa cấp cứu, 0.6% tỷ lệ nhập viện và 0.1% tỷ lệ tái nhập viện. Đồng thời, DDI là nguyên nhân ước tính gây ra khoảng 2-5% tỷ lệ nhập viện ở người lớn tuổi và khoảng 1% tỷ lệ nhập viện ở dân số chung. Từ đó cho thấy:
Tỷ lệ DDI thực sự gây nguy hại trên bệnh nhân chưa có nhiều dữ liệu, nhưng vẫn có thể gây ra những hậu quả nghiêm trọng.
Khó xác định DDI trên thực tế vì các biểu hiện trên lâm sàng thường chồng chéo với các tình trạng bệnh lý, tác dụng điều trị cũng như ADR của thuốc và việc thực hiện xét nghiệm (TDM nồng độ thuốc, ...) để xác định DDI còn hạn chế.
Tuy nhiên, các nghiên cứu đều khẳng định cần phải cảnh báo về nguy cơ tương tác thuốc có thể xuất hiện nhằm giảm và tránh DDI thực sự xảy ra sẽ gây phức tạp, khó khăn trong quá trình điều trị.
Quan trọng là phòng tránh nguy cơ DDI, do đó cần có Hệ thống cảnh báo kiểm tra nguy cơ tương tác.

Hiện có rất nhiều trang web, phần mềm để hỗ trợ tra cứu thông tin về tương tác thuốc như: Drugs.com, Medscape, Uptodate, Facts & Comparisons,… tương đối thuận tiện và dễ dàng cho các nhà lâm sàng. Tuy nhiên, các công cụ này không thể hỗ trợ để cảnh báo tự động các toa thuốc hoặc y lệnh nội trú tại bệnh viện. Do đó, khoa Dược của bệnh viện Bệnh Nhiệt Đới đã xây dựng nguồn dữ liệu khoảng hơn 1.200 cặp tương tác đối với các thuốc có trong danh mục của bệnh viện và tích hợp trên phần mềm kê đơn cấp phát thuốc của bệnh viện nhằm rà soát và cảnh báo nguy cơ tương tác thuốc trong lúc kê đơn của bác sĩ và duyệt thuốc của dược sĩ lâm sàng. Đồng thời phần mềm cung cấp thông tin trong việc theo dõi, xử trí nhằm giảm thiểu nguy cơ có hại ảnh hưởng trên bệnh nhân.
Sau khi ứng dụng công cụ trên từ tháng 11/2018, đơn vị Dược lâm sàng tiến hành khảo sát đánh giá và báo cáo kết quả tương tác thuốc – thuốc có nguy cơ xảy ra (pDDI) từ phần mềm eHospital ở bệnh nhân ngoại trú và nội trú tại Bệnh viện từ tháng 11/2018 – 4/2019, mục tiêu:
-
Xác định tỷ lệ pDDI đối với bệnh nhân nội trú và ngoại trú.
-
Tần suất, tỷ lệ các cặp hoặc nhóm thuốc thường gây ra nguy cơ tương tác thuốc theo mức độ.
-
Các khuyến cáo ứng dụng trên lâm sàng để tránh nguy cơ tương tác thuốc

4.1. Xác định tỷ lệ pDDI đối với bệnh nhân nội trú và ngoại trú.
Kết quả cho thấy tỷ lệ pDDI xuất hiện trong nội trú khoảng 10% cao hơn so với ngoại trú là 2.5%. Theo một nghiên cứu đánh giá hệ thống tại Iran năm 2014 về tương tác thuốc ở bệnh nhân nội trú và ngoại trú cũng có sự tương đồng khi nội trú có pDDI cao hơn so với ngoại trú (19.2% và 8.5%).
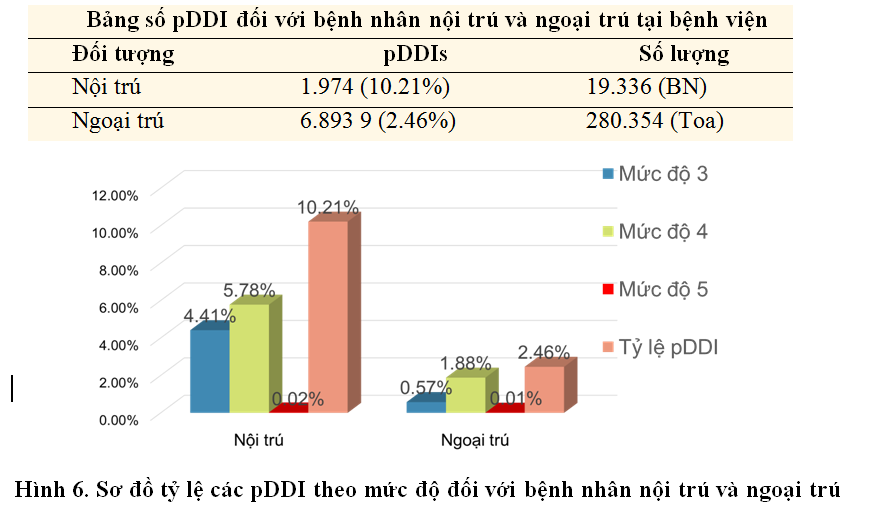
Các nguy cơ tương tác thuốc mức độ 4 (Moderate) chiếm tỷ lệ cao hơn so với mức 3 và 5 ở cả bệnh nhân nội trú và ngoại trú. Mức độ 5 (Severe) có xuất hiện với tỷ lệ thấp lần lượt là 0.02% và 0.01% ứng với nội trú và ngoại trú. Khảo sát ban đầu cho thấy tính ứng dụng của công cụ là phần nào phản ứng sơ bộ các nguy cơ DDI có khả năng xuất hiện trong quá trình điều trị của bệnh nhân nội trú và ngoại trú.
4.2. Tần suất các cặp hoặc nhóm thuốc thường gây ra nguy cơ tương tác thuốc.
Số cặp pDDI/ số lượng pDDI ở nội trú và ngoại trú lần lượt là 179/1974, 105/6893 chứng tỏ các cặp tương tác này xuất hiện nhiều lần trong các toa thuốc và y lệnh. Từ đó, tiến hành tính tần suất của các cặp pDDI mức độ 4-5 và và xác định các cặp pDDI phổ biến ở mức độ 4-5 cần can thiệp như sau:
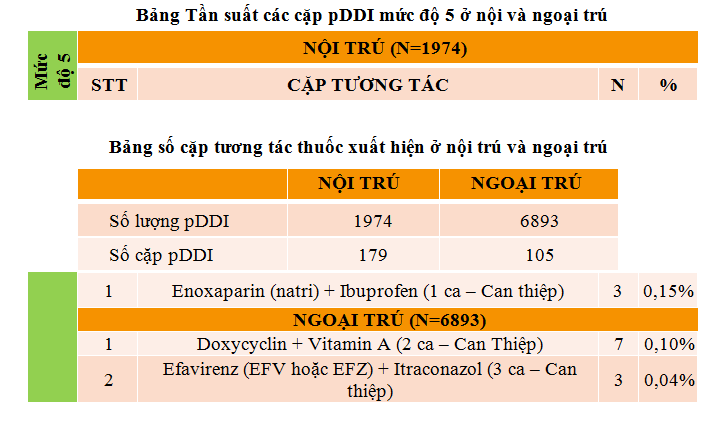
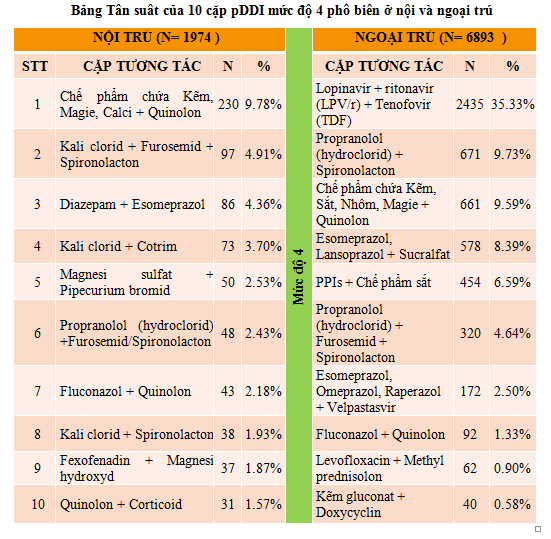
4.3. Báo cáo việc can thiệp các cặp pDDI đã được cảnh báo
Việc can thiệp dựa vào phần mềm cảnh báo tiến hành từ tháng 1/2019. Ở nội trú ghi nhận 6 ca (số lượng thực hiện hội chẩn nhiều hơn nhưng không ghi nhận). Ngoại trú là 2786 trường hợp trên 4506 pDDI mức độ 4+5, chiếm 80%. Cụ thể:
-
Kiểm toa thuốc nội trú 3 khoa CC, dược sĩ lâm sàng đóng chốt tại khoa thực hiện can thiệp khi đi khoa nhưng không ghi nhận trên phần mềm; chủ yếu các tương tác mức độ 4 cần theo dõi điều trị hoặc điều chỉnh liều và 1 ca pDDI mức độ 5. Cần tăng cường ghi nhận các can thiệp vào phần mềm.
-
Ngoại trú thực hiện được 80% các pDDI mức độ 4+5 cho kết quả rất tốt, tuy nhiên cần can thiệp tất cả các pDDI mức độ 5.
-
Phần mềm eHospital không tự liên kết được với phần mềm khác để ghi nhận Can thiệp Dược lâm sàng do đó các dược sĩ lâm sàng cần ghi chú lại và báo cáo 2 lần gây tốn thời gian và mất dữ liệu.
-
Phần mềm không có ghi nhận được bác sĩ đã đọc được cảnh báo và điều chỉnh toa thuốc để dược sĩ không cần can thiệp, có những can thiệp trùng gây mất thời gian cho cả bác sĩ và dược sĩ.
-
Đa số can thiệp là tư vấn và khuyến cáo cho bệnh nhân về cách sử dụng thuốc và theo dõi tác dụng cần lưu ý.
4.4. Các khuyến cáo ứng dụng trên lâm sàng để tránh nguy cơ tương tác thuốc phổ biến tại bệnh viện:
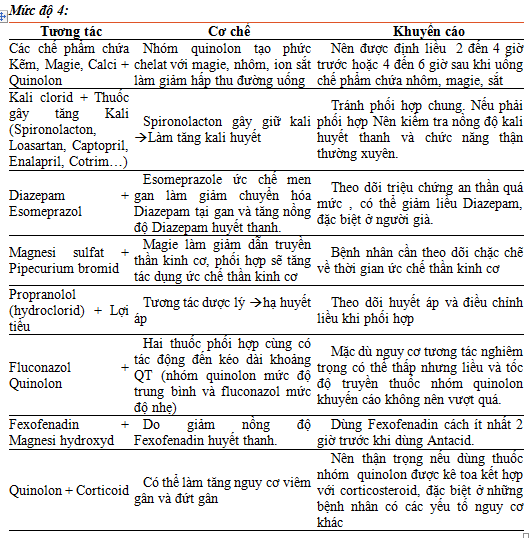
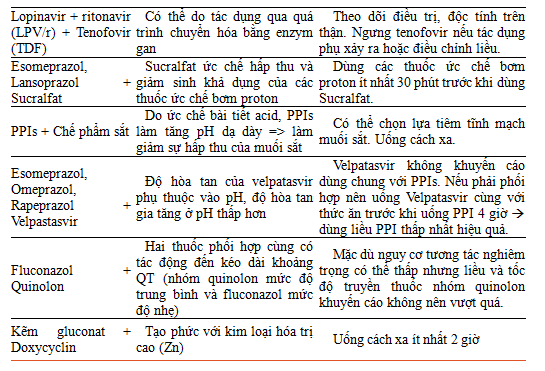
Mức độ 5: cần phải thực hiện tốt các khuyến cáo sau vì đa số là các trường hợp chống chỉ định. Trong một số trường hợp bắt buộc sử dụng nên hội chẩn để có biện pháp theo dõi bệnh nhân nhằm hạn chế ảnh hưởng của tương tác thuốc.
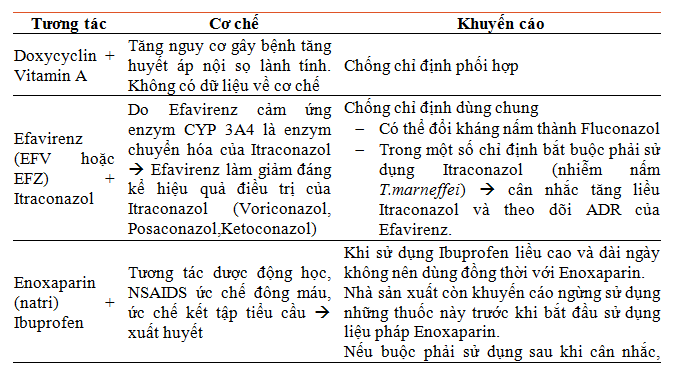
4.5. Kết luận
-
Các tác hại do DDI invitro được xác lập hầu hết được giải thích theo các cơ chế Dược động học hoặc dược lực học.
-
Các nghiên cứu về DDI thực sự có gây hại đến bệnh nhân còn rất khiêm tốn do khó thực hiện.
-
Tỷ lệ pDDI của bệnh nhân tại BVBNĐ từ 11/2018-4/2019 là 2,5% nội trú và 10% ngoại trú.
-
So sánh với nghiên cứu thực hiện tại BVBNĐ 2014: pDDI là 13% ngoại trú, 36% nội trú; mức độ nặng chiếm 10%, cho thấy việc cảnh báo DDI bằng phần mềm bước đầu có hiệu quả.
-
Can thiệp của dược lâm sàng cho bệnh nhân ngoại trú khi toa thuốc có pDDI khoảng 80% so với số toa có pDDI mức độ 4+5 và khoảng 60% so với tổng số toa có pDDI. Nội trú chỉ mới thực hiện ở 3 khoa hồi sức tích cực và còn nhiều can thiệp chưa được ghi nhận trên phần mềm. Cần tăng cường giám sát, thực hiện can thiệp và ghi nhận trên phần mềm.
-
Xác định được 10 cặp DDI phổ biến nhất mức độ 4 và 03 cặp DDI ở mức độ 5 cùng các giải pháp tránh nguy cơ. Đối với cặp tương tác này, bác sĩ nên hướng dẫn bệnh nhân, phối hợp cùng điều dưỡng thực hiện thuốc theo dõi bệnh nhân.
Tài liệu tham khảo
1. Angella Angiji, Adverse Drug Reactions related to mortality and morbidity: Drug-drug interactions and overdoses
2. Bate W et al. JAMA 2007; Nolan L et al. J Am Geriatric Soc 1988
3. Becker ML, et al. Pharmacoepidemiol Drug Saf. 2007;16:641-651.
4. Dechanont S. et al. Hospital admissions/visits associated with drug-drug interactions: a systematic review and meta-analysis. Pharmacoepidemiol Drug Safe 2014 May;23(5):489-97.
5. Ehsan Nabovati et al. Drug-drug interactions in inpatient and outpatient settings in Iran: a systematic review of the literature. 2014; 22(1): 52.
6. Matthew Grissinger, Pa Pat Saf Advis 2016 Dec;13(4):137-148.
7. Reis AMM. Clinics 2011; Moura CS et al. J Pharm Sci 2009 và Clin Drug Investig 2011; Shad MU et al. 2001; Bucsa C et al. 2013.