1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
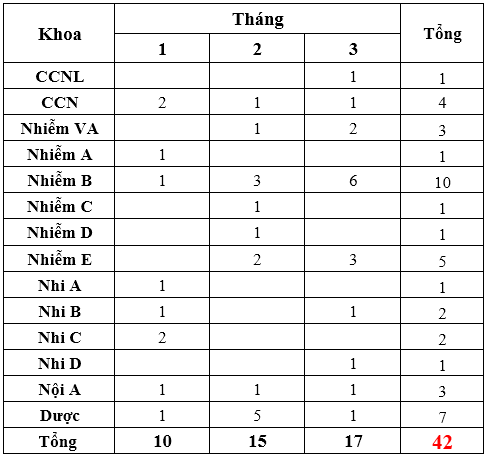
Quý 1-2024 ghi nhận có 42 báo cáo ADR xảy ra tại 14 khoa (theo bảng). Trong đó, khoa Nhiễm B có số báo cáo nhiều nhất là 10 ca. So với 2 quý trước, Quý 1-2024 có giảm số lượng ca báo cáo, tuy nhiên có nhiều ADR đáng lưu ý như sau: - Trên hệ tạo máu: có 2 ca giảm tiểu cầu, 1 ca giảm cả 3 dòng tế bào máu do Cotrim; 1 ca tăng tiểu cầu do Ertapenem; 1 ca tiểu huyết sắc tố do Amphotericin B (cải thiện dần sau khi ngưng thuốc). - Trên hệ thần kinh trung ương, ngoại biên: 2 ca co giật do Imipenem/Cilastatin (thuộc 2 lô thuốc khác nhau); 1 ca run tay, chân do Cotrim (hết run sau khi giảm liều). - Trên da niêm: ghi nhận nhiều báo cáo ca, đáng chú ý có 1 ca do Aciclovir và 1 ca do Ringer lactat. Đây là 2 thuốc gần như không thấy có báo cáo ADR và đã rất thận trọng khi xác định nguyên nhân. Các khoa lâm sàng tiếp tục tăng cường giám sát, theo dõi, xử trí và báo cáo tác dụng phụ không mong muốn của thuốc gửi về khoa Dược trên phần mềm Ehospital.
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
Trong tháng 3, khoa Dược nhận được 02 phản hồi từ khoa lâm sàng về chất lượng cảm quan của thuốc sau khi pha sử dụng: 01 ca Propofol, 01 ca vitamin K1.

Khoa Dược tiến hành đổi trả và cấp phát lọ/ống thuốc mới, đồng thời báo công ty cung ứng về tình hình chất lượng của thuốc. Đến hiện tại chưa ghi nhận thêm trường hợp tương tự từ các khoa lâm sàng về chất lượng các thuốc này. Kính nhờ các khoa lâm sàng tiếp tục theo dõi và phản hồi về khoa Dược các thông tin về chất lượng thuốc để khoa Dược kịp thời có giải pháp xử trí phù hợp.
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 4-2023
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 453 TH nội trú (giảm nhẹ so với quý 4/2023 là 484) và 1.607 toa thuốc ngoại trú (tăng nhẹ so với quý 4/2023 là 1.557) do tình hình bệnh giảm. Đơn vị dược lâm sàng thực hiện 233 can thiệp dược lâm sàng chiếm 11.3% trong các hoạt động thường quy (giảm so với Quý 4/2023 là 14.6%). Chủ yếu là các can thiệp hội ý/hội chẩn về thuốc: liều kháng sinh (TDM voriconazol và linezolid, 88 ca vancomycin, 01 ca AG), phối hợp/lựa chọn kháng sinh và tư vấn về nguy cơ tác dụng bất lợi của thuốc,…và can thiệp trực tiếp khi duyệt nội trú y lệnh hàng ngày.
Trong 233 can thiệp có 78.1% là can thiệp trong việc sử dụng thuốc và tương đương với Quý 4/2023. Quý 1/2024, sự thống nhất ý kiến giữa dược lâm sàng và bác sĩ điều trị là 97,9% (giảm so với quý 4/2023), trong đó có 02 trường hợp đồng ý một phần, 03 trường hợp không đồng ý chủ yếu ở các khoa khám ngoại trú và NTBV. Tuy nhiên, tỷ lệ can thiệp kịp thời khoảng 91%, tăng so với quý 4/2023. Dược sĩ lâm sàng cần tăng cường can thiệp, sâu sát hơn khi duyệt y lệnh nội trú và đi khoa.
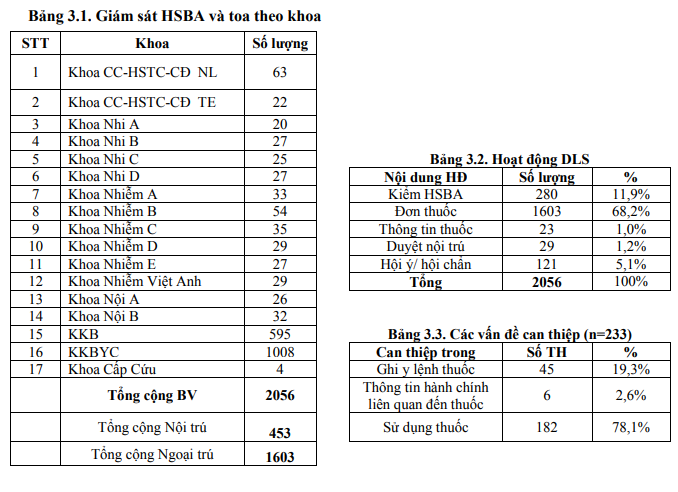
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
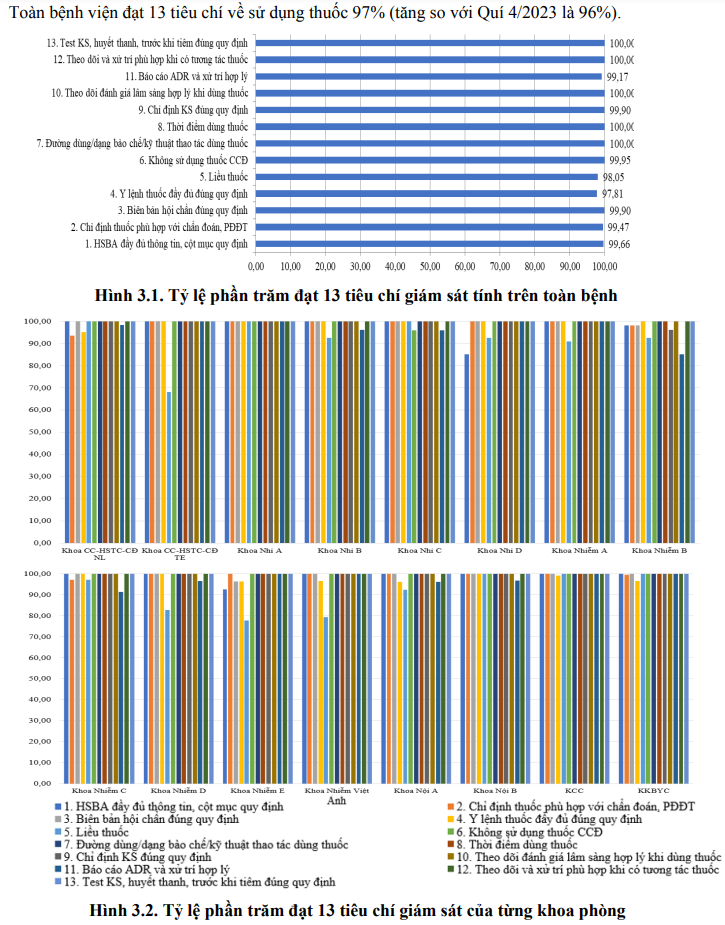
Tiêu chí liều thuốc và y lệnh đầy đủ tăng so với Quý 4/2023. Các khoa thuộc Khối Nhi thực hiện các khuyến cáo về liều thuốc được cảnh báo có cải thiện. Đồng thời, các bác sĩ/điều dưỡng khi nạp y lệnh trên HIS cần chú ý để tránh trùng hoặc sai y lệnh, sai ngày giờ dùng thuốc, ở KKB và KKBYC trong Quý 1-2024 lỗi đánh máy sai tên thuốc giảm so với Quý 4-2023 nhưng tăng về lỗi đánh sai số lượng và liều dùng.
3.3. Khuyến cáo dược lâm sàng:
Quy chế kê đơn:
Khi nạp y lệnh trùng trên hệ thống HIS hoặc đánh nhầm số lượng, tên thuốc, trùng y lệnh; đặc biệt lưu ý khi choàng cử thuốc. Các sai sót này chưa xảy ra và ngăn chặn kịp thời tuy nhiên vẫn lặp lại sai sót trong Quý 1/2024 và có giảm nhẹ so với quý trước. Khuyến cáo các khoa khám bệnh kiểm tra lại đơn thuốc.
Ví dụ:
• Sai liều dùng: 03 trường hợp
• Sai hàm lượng: 03 trường hợp
• Sai số lượng: 06 trường hợp
• Sai tên thuốc: 09 trường hợp
-
Kê đơn PANTOSTAD 40 (Pantoprazol) Nhập PENTOVAS 25 (Tenoforvir alafenamide 25mg)
-
Kê đơn JANUMET 50/850 Nhập GALVUS MET 50/500 (Vildagliptin50/Metformin500)
-
Kê đơn IMENIR 125mg (Cefdinir 125mg) Nhập IMEFED 250mg/31.25mg (Amoxicilin 250mg + acid clavulanic 31.25mg)
-
Kê đơn BIOSUPTIN (Bacillus subtilis) Nhập BIOCEMET DT 500mg/62,5mg (Amoxcilin 500mg+ acid clavulanic 62.5mg)
-
Kê đơn ATINALOX (Nhôm hydroxyd+Magnesi Hydroxyd) Nhập ANTICLOR 2mg (Dexchlorpheniramin 2mg)
-
Kê đơn HASPAN (cao khô lá thường xuân) Nhập GLUCOZIN S (kẽm gluconat 10mg)
-
Kê đơn Flunarizin 5mg Nhập Fluconazol 150mg
-
Kê đơn Ebastin 10mg Nhập Tenofovir alafenamide fumarate 25mg
-
Kê đơn Amlodipin 5mg Nhập Amitriptylin 25mg
Thuốc chủ yếu ở khối ngoại trú, do đó Khoa Dược cập nhật danh mục thuốc LASA của Nhà thuốc bệnh viện và đặt lại tên để cảnh báo việc nhầm lẫn tên thuốc.
Liều:
BN 12 tuổi, 75kg, 160cm. Chẩn đoán viêm phổi. Rx Azithromycin 750mg/ngày
-> Liều Azithromycin NT đường hô hấp: 10-12 mg/kg/ngày. MAX 500 mg/ngày
-> Liều Azithromycin cho tiêu chảy nhiễm trùng: 20 mg/kg/ngày. MAX 1000 mg/ngày.
BN nhiễm trùng huyết Streptococcus oralis, TD viêm nội tâm mạc nhiễm trùng hội ý liều dùng.
-> Khuyến cáo Ampicillin/sulbactam 3g q6h.
Bệnh nhân 81t, 55 kg, 160 cm. Chẩn đoán: Sốc nhiễm trùng từ viêm mô tế bào, nhiễm trùng vết thương vùng cẳng chân (T), cẳng tay 2 bên do MRSA; Tổn thương thận cấp/ TD Bệnh thận mạn. SCr = 381 umol/L, CrCl ~ 10 ml/phút. Rx Linezolid 600 mg q12h, kết quả đo nồng độ đáy Cmin = 34.892 ug/mL.
-> Khuyến cáo tạm ngưng Linezolid trong 24h, tính từ cử sử dụng tiếp theo, liều 450 mg q24
-> Kết quả đo Linezolid Cmin = 6.551 ug/mL, đạt mục tiêu Cmin = 2-7 ug/mL -> Duy trì liều 450 mg q24h, theo dõi PLT và lactate máu bệnh nhân thường xuyên + đáp ứng lâm sàng.
BN bệnh ngày 12, viêm mô tế bào bàn tay (T) do MRSA, TD nhiễm trùng huyết, tổn thương thận cấp Rx 600 mg q12h, nồng độ linezolid Cmin = 22.263 mcg/ml, tiểu cầu chưa ghi nhận bất thường. CrCl ~ < 20 ml/phút
-> BN bị tăng huyết áp có điều trị amlodipin là thuốc được ghi nhận có khả năng tương tác linezolid làm tăng nồng độ linezolid, do đó chưa loại trừ khả năng nồng độ linezolid tăng có phần ảnh hưởng do tương tác này. DLS đề xuất 2 hướng xử trí (1) giảm liều Linezolid 600mg q24h rồi đo lại sau 48h kể từ lúc giảm liều; (2) ngưng amlodipin thay thế bằng một hoạt chất khác, đo lại sau 2-3 ngày rồi xử trí tiếp theo. BS thực hiện ngưng Amlodipine, giữ liều linezolid 600 mg q12h Cmin = 9.15 ug/mL Giảm liều 450 mg q12h -> Xuất viện, không đo lại.
Bệnh nhân 47t, 56kg, 165cm. Chẩn đoán: Nhiễm trùng huyết nghi từ Áp xe mông lưng do MRSA; Nhiễm trùng vết thương; Tổn thương thận cấp có nước tiểu, cải thiện; CrCl ~ 40 ml/phút. *KQ cấy mủ vết thương S.aureus, cấy máu: chưa mọc.
*Vấn đề: Rx Linezolid 600 mg q12h. Kết quả đo nồng độ Linezolid Cmin = 14.94 ug/mL. Bệnh nhân đang Rx đồng thời: Amlodipine, Esomeprazol (chất ức chế P-gp) Tương tác thuốc có thể làm tăng nồng độ linezolid trong máu, hiện vẫn tiếp tục Rx linezolid cho nhiễm trùng + điều trị nội khoa. Khuyến cáo chỉnh liều linezolid như sau:
-> Tạm ngưng linezolid (ước tính thời gian tạm ngưng theo T1/2 – Hội ý/hội chẩn DLS); Giảm liều Linezolid thành 600 mg q24h, đo kiểm tra lại nồng độ Linezolid: Cmin = 5.725 ug/mL -> Duy trì liều
Bệnh nhân 68t, 74 kg, 164cm. Chẩn đoán: Lao phổi AFB (+) tái phát; Sốc nhiễm trùng từ viêm phổi - ARDS; Nhiễm nấm huyết. Rx Caspofungin LD 70 mg. MD 50 mg q24h + Tube R/H + PZA + Ethambutol. Cấy máu (+) Candida albicans
*Vấn đề: Tương tác thuốc với Rifampicin có thể làm giảm nồng độ caspofungin. Cơ chế đề xuất: Rifampin là cơ chất OATP1B1 (protein vận chuyển), rifampin gây sự ức chế trong ngắn hạn và cảm ứng trong dài hạn sự hấp thu caspofungin ở gan qua trung gian OATP1B1 ↓ 30% nồng độ Caspofugin sau 2 tuần Rx
-> Khuyến cáo tăng liều Caspofungin MD 50mg lên 70mg q24h khi sử dụng đồng thời với Rifampicin (TLTK: NSX)
Bệnh nhân Viêm phổi do nấm Asperillus xâm lấn bội nhiễm Rx Voriconazol IV 200mg/12h AST/ALT/GGT: 41/59/528 U/L, X quang phổi (14/1) cải thiện hơn so với (7/1). Nồng độ voriconazol đo được khoảng 4 ug/ml
-> Đối với người Châu Á cần đưa nồng độ < 4 ug/ml, men gan tăng. Khuyến cáo giảm 1/2 liều còn 100mg/12h, tiếp tục theo dõi diến tiến trên gan.
Chẩn đoán: Bại não - Động kinh. Các thuốc đang sử dụng Natri valproate 200mg/ml ( 0.75ml/12h), Oxcarbazepin 60mg/ml (3ml/12h). Bé buồn nôn, nôn ọe cả ngày, chỉ uống được ít sữa Domperidon 1mg/ml (5ml/8h trước ăn 30 phút) tuy nhiên không cải thiện.
-> Có tương tác thuốc xảy ra tuy nhiên chỉ ở mức độ theo dõi điều trị, không chống chỉ định. Bé 15 tuổi tuy nhiên cân nặng 25 kg + chiều cao 120 cm -> nghĩ có thể quá liều thuốc dẫn tới các triệu chứng trên. Do theo Dược thư Quốc gia 2022 liều thuốc Oxcarbazepin đối với dung dịch uống đối với trẻ 6 - 16 tuổi trong cả đơn trị và phối hợp là 8 - 10 mg/kg/ngày chia làm 2 lần -> thay đổi 3ml/12h thành 1.5ml/12h, có thể uống cùng bữa ăn (sinh khả dụng thuốc không bị ảnh hưởng bởi thức ăn). Đề nghị theo dõi đánh giá triệu chứng trên và cả hiệu quả chống động kinh của BN.
Chẩn đoán: Theo dõi viêm nội tâm mạc nhiễm trùng Rx rifampicin 600mg/12h
-> Viêm nội tâm mạc nhiễm trùng: rifampicin 300mg/8h
BN 15 tuổi, 85kg. Chẩn đoán lao màng não do vi khuẩn lao không điển hình. Hiện tại đang điều trị phác đồ RHZE, phối hợp thêm Azithromycin. Liều thuốc đang dùng 5 viên 150mgR/75mgH/400mgZ + 4 viên Ethambutol 400mg + 1 viên Azithromycin 500mg. Chức năng thận của BN tăng cao đột ngột SCr 80 45 umol/L, eCrCl = 240 ml/phút. Hội chẩn liều thuốc kháng lao cho BN tăng thanh thải.
-> Tham khảo bảng liều thuốc kháng lao của Bộ Y tế (QĐ 162/2024), Uptodate, Dailymed Không có thông tin chỉnh liều thuốc ở BN tăng thanh thải đang dùng thuốc kháng lao Dùng liều cao nhất được khuyến cáo theo phác đồ BYT (theo Cân nặng + chức năng thận). Bổ sung thêm 1 viên Pyrazinamid 500mg.
Chẩn đoán: Hoại tử xương hàm trên do nấm Mucor đang Rx Posaconazol 400mg q12h, hiện CrCl 48 ml/phút, nôn ói nhiều BS hội ý điều chỉnh liều và dự định cho BN dùng thuốc Domperidon để xử trí tình trạng nôn.
-> CrCl 48 ml/phút gần mốc giảm liều thuốc (CrCl < 50 ml/phút) chưa chỉnh liều ngay, dặn dò BN uống nhiều nước.
-> Posaconazol, Domperidone có tương tác thuốc làm tăng nồng độ thuốc Domperidon trong huyết thanh, làm tăng nguy cơ loạn nhịp tim không dùng chung, có thể chọn lựa Itoprid.
Bệnh nhân cấy máu (+) B. cepacia đã Rx Meropenem ~ 7 ngày. Bệnh nhân sau đó cần xuất viện để xạ trị K-vú. Bác sĩ hỏi liều Cotrim PO duy trì cho bệnh nhân
-> Khuyến cáo liều Cotrim 8-10 mg/kg/ngày chia mỗi q6h hoặc q8h. Liều tính theo Trimethoprim.
BN 9 tuổi, 30kg. Chẩn đoán viêm gan siêu vi B cấp. Hội chẩn việc dùng silymarin cho TE
-> Các chế phẩm silymarin hiện có trong nội viện không có thông tin điều trị cho trẻ em dưới 12 tuổi. Theo một số các nghiên cứu, silymarin có thể dùng được cho trẻ em <12 tuổi với liều dùng 5-10 mg/kg/ngày chia 2-3 cử.
-> Bác sĩ có thể sử dụng chỉ định off-lablel của silymarin cho trẻ em với chế độ liều như trên, tuy nhiên bệnh nhân tự chi trả chi phí điều trị.
Sử dụng thuốc:
Bệnh nhân 70t, 45kg, 164cm. Chẩn đoán: TD nhiễm trùng huyết từ viêm phổi - Suy hô hấp; TD nhiễm nấm Aspergillus; Tổn thương thận cấp. Rx Vancomycin 750 mg q12h Voriconazol 200 mg q12h. SCr = 69 62 86 97 94 umol/L
*Vấn đề: Diễn tiến suy thận cấp nghi do thuốc, CrCl ~ 41 ml/phút, đã đo và hiệu chỉnh liều Vancomycin. Không khuyến cáo Voriconazol IV nếu CrCl < 50 ml/phút
-> Khuyến cáo: Chuyển Voriconzol IV Voriconazol PO, liều giữ nguyên 200 mg q12h do dạng IV có chứa tá dược ảnh hưởng đến chức năng thận. Theo dõi chức năng thận mỗi ngày
Bệnh nhân 65t, 55 kg, 165 cm. Chẩn đoán: Viêm phổi do nấm Asperillus xâm lấn bội nhiễm. Nấm miệng Rx Fluconazol trước đó 6N. N7 Rx đồng thời Voriconazol N1 + Fluconazol N7.
-> Khuyến cáo ngưng Fluconazol do phổ kháng nấm Voriconazol phủ rộng hơn Fluconazol, không phối hợp 2 thuốc chung nhóm và tình trạng nấm miệng hiện ổn
Chẩn đoán nhiễm Toxocara canis/Dị ứng da. Kê đơn phối hợp 02 loại kháng histamin thế hệ 2 (04 toa):
_ Fexofenadin 180mg + Levocetirizin 5mg
_ Fexofenadin 180mg + Ebastin 10mg
_ Levocetirizin 5mg + Ketotifen 1mg
_ Levocetirizin 5mg + Ebastin 10mg x 2 lần/ngày
-> Đồng thời vừa tăng liều kháng histamin thế hệ 2 vừa phối hợp kháng histamin thế hệ 1 (01 toa):
_ Fexofenadin 180mg x 2 lần/ngày + Dexchlorpheniramin 2mg x 2 lần/ngày
-> Khuyến cáo: Sử dụng theo hướng dẫn điều trị của BV như sau:
• Theo HD điều trị mày đay (Hướng dẫn Chẩn đoán và điều trị các bệnh Da liễu - QĐ 4416/QĐ-BYT): việc kết hợp 2 loại kháng Histamin được cho là không có lợi ích so với sử dụng 1 loại đơn độc,
• Khuyến cáo dùng 1 loại kháng histamin thế hệ 2 nếu không đáp ứng có thể tăng liều 2-4 lần.
• Hoặc theo phác đồ mày đay của bệnh viện Bệnh nhiệt đới: đổi sang dùng kháng histamin thế hệ 2 khác hoặc phối hợp 1 thuốc kháng histamin thế hệ 2 + 1 thuốc kháng histamin thế hệ 1
BN có CĐ Đợt bùng phát viêm gan siêu vi B mạn HBeAg âm. Xơ gan Child C. Dãn tĩnh mạch thực quản độ I. Trào ngược dạ dày thực quản - Loét hành tá tràng. Khó tiêu chức năng. Hạ kali máu. TD bệnh não gan tối thiểu. Nội soi ngày 26/02 thấy có loét dạ dày - tá tràng. Từ lúc nhập viện ngày 14/3 bắt đầu dùng Esomeprazole liều 40 mg sau đó giảm xuống còn 20mg, cảm giác khó chịu khi uống antacid nên đã ngưng. Hiện tại BN còn khó chịu tiêu hóa nhiều. Hội chẩn DLS tối ưu liều PPI cho bệnh nhân xơ gan child C.
-> Về mặt dược động, BN có chức năng gan suy giảm làm tăng nồng độ PPIs trong máu do giảm chuyển hóa. Ở BN Xơ gan Child-Pugh C hoặc xơ gan nặng: Theo EMC, không nên dùng liều esomeprazole quá 20mg/ngày.
-> Theo Uptodate, đa số các chỉ định cho phép dùng liều tối đa 20mg/ngày, riêng hội chứng Zollinger-Elison điều trị khởi đầu với liều Esomeprazole từ 20mg x 2 lần/ngày. Hiện tại BN còn khó chịu tiêu hóa nhiều, có khả năng liên quan đến việc vết loét đang không lành tốt.
-> Khuyến cáo: sử dụng thêm Sucrafat, nếu sau khoảng 2-3 ngày vẫn không đỡ thì cân nhắc liều Esomeprazole lên 20 mg x2 lần/ngày.
Bệnh nhân truyền Nicardipine bị viêm tắc tĩnh mạch tại chỗ tiêm. Bác sĩ hỏi Nicardipine có gây phản ứng viêm tại chỗ tiêm không?
-> Theo ghi nhận từ NSX: Nicardipine được báo cáo có gây viêm tắc tĩnh mạch tại chỗ tiêm (tần suất chưa rõ).Khuyến cáo: Trừ khi được tiêm truyền qua tĩnh mạch trung tâm, cần pha loãng thuốc tiêm truyền trong Glucose 5% đến nồng độ 0.1 đến 0.2 mg/mL trước khi dùng
Bệnh nhân 21t, 48 kg, 160 cm. Chẩn đoán: Viêm mô tế bào bàn chân (T); TD Nhiễm trùng huyết; Thai 17 tuần con lần 1; TD Huyết khối tĩnh mạch chi dưới. Sưng nóng đỏ đau mu bàn chân trái tăng dần, không chảy mủ, không có vết thương ngõ vào. Rx Oxacillin 2g q6h trong 48h.
*Vấn đề: Đã Rx kháng sinh tĩnh mạch 48h, đánh giá lâm sàng: Ngày qua còn sốt cao 3 cữ 39 - 39.8 độ C, lạnh run; xuất hiện hồng ban đỏ rải rác vùng bụng, tay; sang thương da mu bàn chân trái tăng dần. Bác sĩ đánh giá lâm sàng kém đáp ứng, chưa loại trừ tác nhân MRSA và Streptococcus spp. Hội ý DLS về việc sử dụng Clindamycin cho PNCT nhằm dự phòng shock độc tố do Strep. spp
-> Khuyến cáo về việc sử dụng Clindamycin cho PNCT:
a) Clindamycin được khuyến cáo sử dụng cho bệnh nhân mang thai để dự phòng bệnh liên cầu nhóm B ở trẻ sơ sinh (lựa chọn thay thế cho những bệnh nhân có nguy cơ cao bị sốc phản vệ với penicillin (hoặc không rõ nguy cơ) (ACOG 797 2020)
b) Clindamycin đi qua nhau thai và có thể được phát hiện trong máu cuống rốn và mô bào thai (Philipson 1973; Weinstein 1976).
c) Các nghiên cứu trên động vật đã không chứng minh được nguy cơ đối với thai nhi khi điều trị bằng clindamycin và dữ liệu trên người còn hạn chế.
d) Liều Clindamycin trong dự phòng shock độc tố: 600-900 mg q8h, thời gian điều trị cho đến khi ổn định về mặt lâm sàng và huyết động trong ≥48 đến 72 giờ; sau đó ngừng dùng clindamycin và đơn trị liệu bằng thuốc thích hợp
Bệnh nhân 29t, 81kg, 163 cm. Chẩn đoán: Sốc sốt xuất huyết Dengue N5 vào sốc 17h ngày 10/01; Tổn thương gan nặng; TD Suy thượng thận mạn; Xuất huyết tiêu hóa trên nghi do loét dạ dày - tá tràng; TD Rối loạn điện giải; Suy gan cấp; Rối loạn đông máu. XN ngày 12/01: Bilirubin T.P=78.1; Billirubin T.T=43.7 umol/L; AST/ALT=413/158 U/L; PLT = 11 K/uL; TQ = 15.9 giây; Bệnh nhân đang Rx cho CĐ TD viêm phổi, hiện chưa có tác nhân vi sinh, phân nhóm II *Vấn đề: Cefoperazone/Sulbactam ghi nhận báo cáo ADR trên huyết học: Giảm tiểu cầu 0.8% (thoáng qua), giảm prothrompin 3.8%; tình trạng bất thường xác xét nghiệm: Tăng AST 5.7%, ALT 6.2 %, phosphatase kiềm 2.4 % và bilirubin 1.2%; thêm vào đó, thuốc trải trừ qua gan - mật là chủ yếu. Trên nền bệnh nhân rối loạn chức năng gan
_ Kéo dài thời gian bán thải lên 2-4 lần
-> Khuyến cáo trên đối tượng bệnh nhân:
a) Liều sử dụng không quá 2g/ngày ở bệnh nhân suy gan nặng hoặc suy gan kèm suy thận và cần theo dõi nồng độ thuốc KHÔNG thực hiện được
b) Chuyển kháng sinh khác có phổ tương đương (phân nhóm II) + ít tác dụng phụ/ADR trên huyết học và chức năng gan
Tương tác thuốc:
Hoàn thiện cảnh báo mức độ 5 và nội dung ghi chú can thiệp của bác sĩ và DLS trên y lệnh Ehospital theo Quyết định 5948/QĐ-BYT.
Lưu ý tương tác thuốc của Linezolid. Khi sử dụng đồng thời Linezolid và các thuốc ức chế/cảm ứng P-gp (bảng dưới).

Có thể cân nhắc xử trí:
• Đổi thuốc dùng kèm (nếu được)
• Giảm liều linezolid
• Kiểm tra tiểu cầu, chức năng thận, TDM
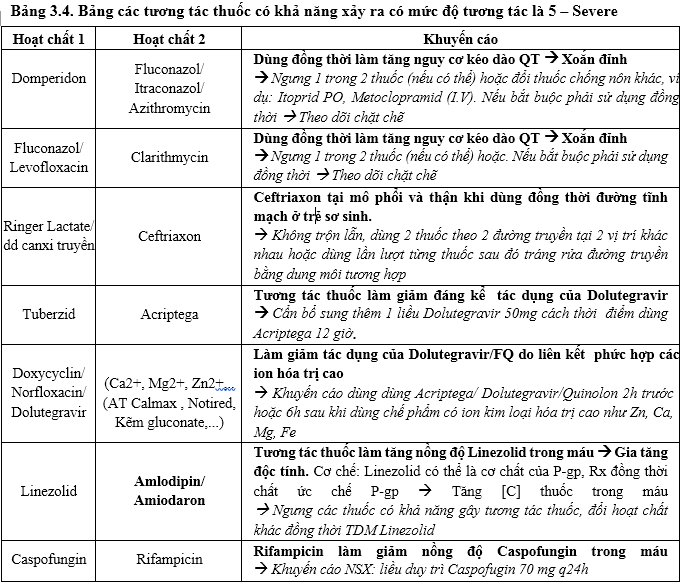
Khuyến cáo Hội đồng thuốc và điều trị - Ban Quản lý sử dụng kháng sinh
Chế phẩm KCl 10% của Công ty Vinphaco có khuyến cáo không sử dụng cùng các dung dịch chứa Glucose vì dung dịch Glucose có thể làm giảm thêm nồng độ kali máu trên các đối tượng bệnh nhân này. Đồng thời, công ty có phúc đáp về vấn đề tương kỵ là khi thử nghiệm pha loãng dung dịch Kali clorid 10% trong dung dịch Glucose 10%, 5% với tỷ lệ 1 lít dung dịch + 3 ống KCl 10% thì KHÔNG CÓ tương tác vậy lý xảy ra.
Hội đồng thuốc và điều trị thống nhất ý kiến việc hạ kali máu khi pha với dung dịch Glucose theo nhà sản xuất khuyến cáo sẽ được bác sĩ điều trị theo dõi và đánh giá; việc pha KCl 10% trong dung dịch Glucose là kỹ thuật thực hành áp dụng từ lâu và chưa có khuyến cáo KHÔNG pha với dung dịch Glucose từ các nhà sản xuất thuốc KCl 10% khác đã cung ứng cho bệnh viện. Vì vậy, việc được chỉ định theo tình trạng lâm sàng của người bệnh và không hạn chế pha hoặc sử dụng cùng với dung dịch Glucose do không có tương tác về mặt vật lý. Hội đồng đề nghị khoa Dược cập nhật nội dung “Chú ý” trong bảng hướng dẫn pha tiêm thuốc KCl 10% của nhà sản xuất Vinphaco như sau: “Phải pha loãng trước khi dùng. Lưu ý: NSX khuyến cáo khi dùng chung với dung dịch có thể giảm Kali máu nên HĐT khuyến cáo theo dõi nồng độ kali máu khi sử dụng. Không có tương kỵ vật lý, hoa học khi dùng hoặc pha chung kali với dung dịch Glucose."
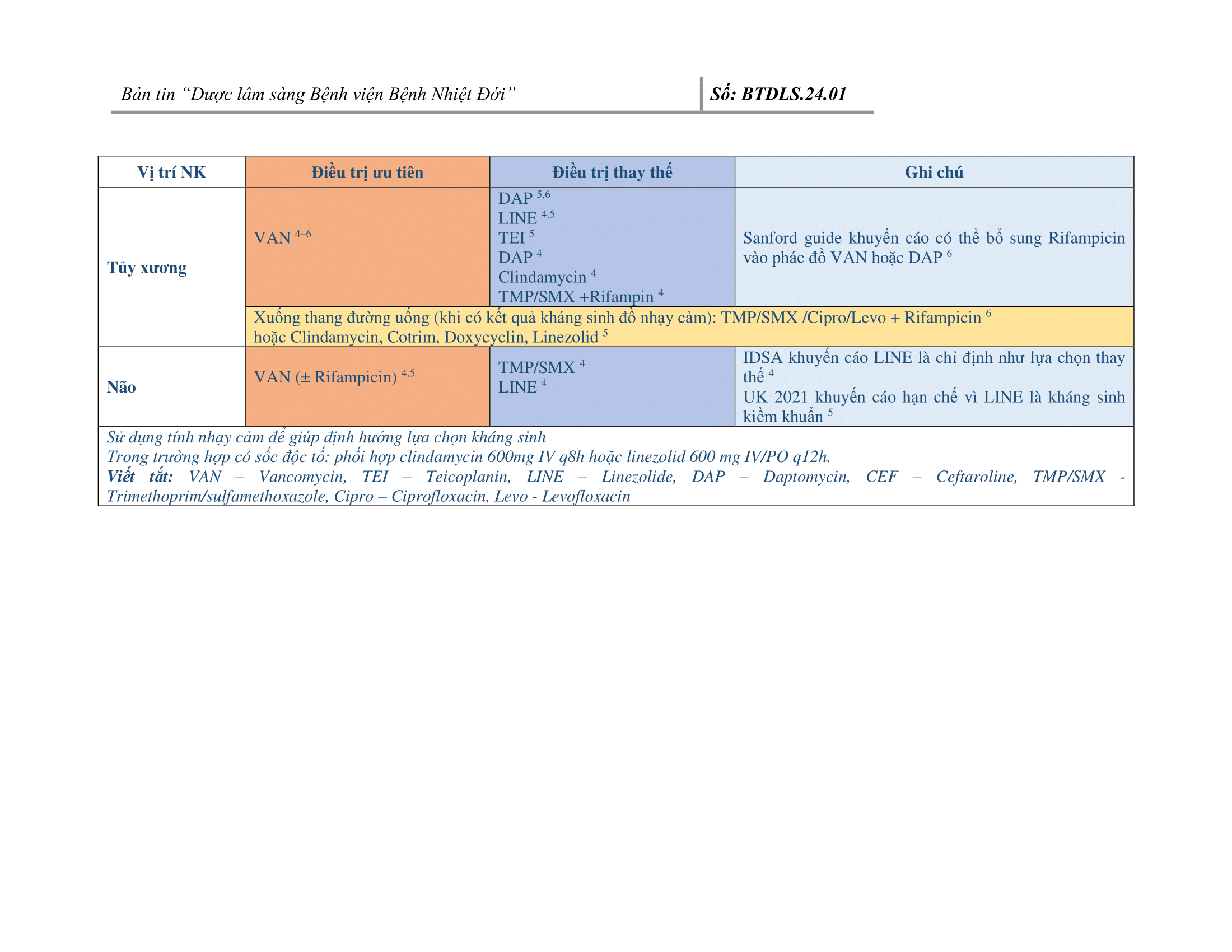
4. CHUYÊN ĐỀ: MRSA VÀ CHIẾN LƯỢC LỰA CHỌN KHÁNG SINH ĐIỀU TRỊ












-
Turner NA, Sharma-Kuinkel BK, Maskarinec SA, et al. Methicillin-resistant Staphylococcus aureus: an overview of basic and clinical research. Nat Rev Microbiol. 2019;17(4):203-218. doi:10.1038/s41579-018-0147-4
-
Creech CB, Al-Zubeidi DN, Fritz SA. Prevention of Recurrent Staphylococcal Skin Infections. Infect Dis Clin North Am. 2015;29(3):429-464. doi:10.1016/j.idc.2015.05.007
-
Inagaki K, Lucar J, Blackshear C, Hobbs CV. Methicillin-susceptible and Methicillin-resistant Staphylococcus aureus Bacteremia: Nationwide Estimates of 30-Day Readmission, In-hospital Mortality, Length of Stay, and Cost in the United States. Clin Infect Dis. 2019;69(12):2112-2118. doi:10.1093/cid/ciz123
-
Clinical Practice Guidelines by the Infectious Diseases Society of America for the Treatment of Methicillin-Resistant Staphylococcus aureus Infections in Adults and Children | Clinical Infectious Diseases | Oxford Academic. Accessed March 31, 2024. https://academic.oup.com/cid/article/52/3/e18/306145?login=false
-
Treatment of methicillin-resistant Staphylococcus aureus (MRSA): updated guidelines from the UK | JAC-Antimicrobal Resistance | Oxford Academic. Accessed April 1, 2024. https://academic.oup.com/jacamr/article/3/1/dlaa114/6127118
-
Sanford Guide 2024.
-
Staphylococcus aureus | Johns Hopkins ABX Guide. Accessed April 16, 2024. https://www.hopkinsguides.com/hopkins/view/Johns_Hopkins_ABX_Guide/540518/all/ Staphylococcus_aureus?refer=true
-
2023 ESC Guidelines for the management of endocarditis | European Heart Journal | Oxford Academic. Accessed April 15, 2024. https://academic.oup.com/eurheartj/article/44/39/3948/7243107
-
Hashemian SMR, Farhadi T, Ganjparvar M. Linezolid: a review of its properties, function, and use in critical care. Drug Des Devel Ther. 2018;12:1759-1767. doi:10.2147/DDDT.S164515
-
Dược Thư 2022.
-
Search - UpToDate. Accessed April 1, 2024. https://www.uptodate.com/contents/search
-
Teicoplanin therapy for MRSA bacteraemia: a retrospective study emphasizing the importance of maintenance dosing in improving clinical outcomes | Journal of Antimicrobial Chemotherapy | Oxford Academic. Accessed April 1, 2024. https://academic.oup.com/jac/article/70/1/257/2911146?login=false
-
Pharmacy | Free Full-Text | Glycopeptide Hypersensitivity and Adverse Reactions. Accessed April 7, 2024. https://www.mdpi.com/2226-4787/8/2/70
-
Teicoplanin/vancomycin | Reactions Weekly. Accessed April 7, 2024. https://link.springer.com/article/10.1007/s40278-019-57874-2
-
Itani KMF, Biswas P, Reisman A, Bhattacharyya H, Baruch AM. Clinical efficacy of oral linezolid compared with intravenous vancomycin for the treatment of methicillin-resistant Staphylococcus aureus-complicated skin and soft tissue infections: a retrospective, propensity score-matched, case-control analysis. Clin Ther. 2012;34(8):1667-1673.e1. doi:10.1016/j.clinthera.2012.06.018
-
Meta-analysis of vancomycin versus linezolid in pneumonia with proven methicillin-resistant Staphylococcus aureus - ScienceDirect. Accessed April 1, 2024. https://www.sciencedirect.com/science/article/pii/S2213716520303234
-
Yue J, Dong BR, Yang M, Chen X, Wu T, Liu GJ. Linezolid versus vancomycin for skin and soft tissue infections. Cochrane Database Syst Rev. 2016;2016(1):CD008056. doi:10.1002/14651858.CD008056.pub3
-
Expert consensus statement on therapeutic drug monitoring and individualization of linezolid - PMC. Accessed April 15, 2024. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9399604/
-
A 10‐Year Experience of Therapeutic Drug Monitoring (TDM) of Linezolid in a Hospital‐wide Population of Patients Receiving Conventional Dosing: Is there Enough Evidence for Suggesting TDM in the Majority of Patients? - Pea - 2017 - Basic & Clinical Pharmacology & Toxicology - Wiley Online Library. Accessed April 15, 2024. https://onlinelibrary.wiley.com/doi/full/10.1111/bcpt.12797
-
Giám sát nồng độ thuốc trong huyết thanh ở bệnh nhân nặng với các thuốc kháng sinh, kháng nấm và kháng virus.
-
Sutrave S, Kikhney J, Schmidt J, et al. Effect of daptomycin and vancomycin on Staphylococcus epidermidis biofilms: An in vitro assessment using fluorescence in situ hybridization. PLoS ONE. 2019;14(8):e0221786. doi:10.1371/journal.pone.0221786
-
Jones TW, Jun AH, Michal JL, Olney WJ. High-Dose Daptomycin and Clinical Applications. Ann Pharmacother. 2021;55(11):1363-1378. doi:10.1177/1060028021991943
-
Treatment strategies for persistent methicillin‐resistant Staphylococcus aureus bacteraemia - Lewis - 2018 - Journal of Clinical Pharmacy and Therapeutics - Wiley Online Library. Accessed April 1, 2024. https://onlinelibrary.wiley.com/doi/10.1111/jcpt.12743
-
Shirley DAT, Heil EL, Johnson JK. Ceftaroline Fosamil: A Brief Clinical Review. Infect Dis Ther. 2013;2(2):95-110. doi:10.1007/s40121-013-0010-x
-
Abate G, Wang G, Frisby J. Ceftaroline: Systematic Review of Clinical Uses and Emerging Drug Resistance. Ann Pharmacother. 2022;56(12):1339-1348. doi:10.1177/10600280221082326
-
Wald-Dickler N, Holtom P, Spellberg B. Busting the Myth of “Static vs Cidal”: A Systemic Literature Review. Clin Infect Dis Off Publ Infect Dis Soc Am. 2018;66(9):1470-1474. doi:10.1093/cid/cix1127
-
Dykhuizen RS, Harvey G, Stephenson N, Nathwani D, Gould IM. Protein binding and serum bactericidal activities of vancomycin and teicoplanin. Antimicrob Agents Chemother. 1995;39(8):1842-1847. doi:10.1128/aac.39.8.1842
-
Jaber RH, Beahm NP. Daptomycin for the treatment of acute bacterial meningitis: A narrative review. Int J Antimicrob Agents. 2023;61(5):106770. doi:10.1016/j.ijantimicag.2023.106770
-
Gerber P, Stucki A, Acosta F, Cottagnoud M, Cottagnoud P. Daptomycin is more efficacious than vancomycin against a methicillin-susceptible Staphylococcus aureus in experimental meningitis. J Antimicrob Chemother. 2006;57(4):720-723. doi:10.1093/jac/dkl007
-
emed.bvbnd. Accessed April 1, 2024. https://emed.bvbnd.vn/wiki/
-
Kawasuji H, Nagaoka K, Tsuji Y, et al. Effectiveness and Safety of Linezolid Versus Vancomycin, Teicoplanin, or Daptomycin against Methicillin-Resistant Staphylococcus aureus Bacteremia: A Systematic Review and Meta-Analysis. Antibiotics. 2023;12(4):697. doi:10.3390/antibiotics12040697
-
Tsai CY, Lee CH, Chen IL. Daptomycin versus teicoplanin for bloodstream infection due to methicillin-resistant Staphylococcus aureus with a high teicoplanin minimal inhibitory concentration ≥1.5 mg/L: a propensity score-based analysis. Infect Drug Resist. 2018;11:2011-2020. doi:10.2147/IDR.S184411
-
Lee JH, Choi MG, Park HJ, Kim HC, Choi CM. Comparison of mortality and clinical failure rates between vancomycin and teicoplanin in patients with methicillin-resistant Staphylococcus aureus pneumonia. BMC Infect Dis. 2022;22:600. doi:10.1186/s12879-022-07549-2
-
Kalil AC, Klompas M, Haynatzki G, Rupp ME. Treatment of hospital-acquired pneumonia with linezolid or vancomycin: a systematic review and meta-analysis. BMJ Open. 2013;3(10):e003912. doi:10.1136/bmjopen-2013-003912
-
Shi Y, Wu HL, Wu YH, et al. Safety and clinical efficacy of linezolid in children: a systematic review and meta-analysis. World J Pediatr. 2023;19(2):129-138. doi:10.1007/s12519-022-00650-1
-
Kaplan SL, Patterson L, Edwards KM, et al. Linezolid for the treatment of community- acquired pneumonia in hospitalized children. Pediatr Infect Dis J. 2001;20(5):488.
-
Torres A, Kuraieva A, Stone GG, Cillóniz C. Systematic review of ceftaroline fosamil in the management of patients with methicillin-resistant Staphylococcus aureus pneumonia. Eur Respir Rev. 2023;32(170). doi:10.1183/16000617.0117-2023
-
Sipahi OR, Bardak-Ozcem S, Turhan T, et al. Vancomycin versus Linezolid in the Treatment of Methicillin-Resistant Staphylococcus aureus Meningitis. Surg Infect. 2013;14(4):357-362. doi:10.1089/sur.2012.091
-
Pintado V, Pazos R, Jiménez-Mejías ME, et al. Linezolid for therapy of Staphylococcus aureus meningitis: a cohort study of 26 patients. Infect Dis. 2020;52(11):808-815. doi:10.1080/23744235.2020.1789212
-
Chen HA, Yang CJ, Tsai MS, Liao CH, Lee CH. Linezolid as salvage therapy for central nervous system infections due to methicillin-resistant Staphylococcus aureus at two medical centers in Taiwan. J Microbiol Immunol Infect. 2020;53(6):909-915. doi:10.1016/j.jmii.2020.08.004
-
Muñoz P, De la Villa S, Martínez-Sellés M, et al. Linezolid for infective endocarditis. Medicine (Baltimore). 2021;100(51):e27597. doi:10.1097/MD.0000000000027597
-
Liu C, Mao Z, Yang M, et al. Efficacy and safety of daptomycin for skin and soft tissue infections: a systematic review with trial sequential analysis. Ther Clin Risk Manag. 2016;12:1455-1466. doi:10.2147/TCRM.S115175
-
Wang SZ, Hu JT, Zhang C, et al. The safety and efficacy of daptomycin versus other antibiotics for skin and soft-tissue infections: a meta-analysis of randomised controlled trials. BMJ Open. 2014;4(6):e004744. doi:10.1136/bmjopen-2013-004744
-
Friedland HD, O’Neal T, Biek D, et al. CANVAS 1 and 2: Analysis of Clinical Response at Day 3 in Two Phase 3 Trials of Ceftaroline Fosamil versus Vancomycin plus Aztreonam in Treatment of Acute Bacterial Skin and Skin Structure Infections. Antimicrob Agents Chemother. 2012;56(5):2231-2236. doi:10.1128/aac.05738-11
-
Trinh TD, Jorgensen SCJ, Zasowski EJ, et al. Multicenter Study of the Real-World Use of Ceftaroline versus Vancomycin for Acute Bacterial Skin and Skin Structure Infections. Antimicrob Agents Chemother. 2019;63(11):e01007-19. doi:10.1128/AAC.01007-19
DS. Trần Bảo Trâm