- 1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
- 2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
- 3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 1-2018
- 4. CHUYÊN ĐỀ: ĐỘ LỌC CẦU THẬN và HIỆU CHỈNH LIỀU THUỐC
1. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
A. Tổng kết công tác báo cáo ADR:
Quý 1-2019 ghi nhận có 10 báo cáo ADR xảy ra ở 7 khoa (theo bảng). Trong đó khoa Nhiễm Việt Anh (2 ca), CCNL (2 ca), các khoa còn lại có báo cáo nhưng ít, tất cả đều được xử trí kịp thời. So với Quý 4-2018 (18 báo cáo), số lượng báo cáo ADR Quý 1-2019 giảm nhiều. Đồng thời, khi theo dõi việc thực hiện báo cáo ADR từ tháng 6 -2018 đến tháng 3-2019, cho thấy số lượng báo cáo giảm đều qua các tháng. Bộ phận dược lâm sàng sẽ tìm hiểu nguyên nhân gây giảm số lượng báo cáo ADR, từ đó tìm cách khắc phục nâng cao công tác báo cáo ADR.
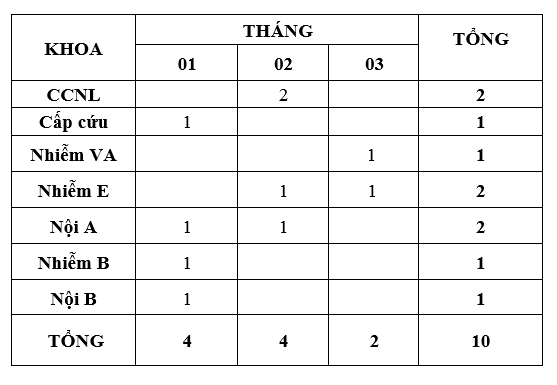
B. Phản hồi các khoa lâm sàng về chất lượng thuốc:
Không có
2. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC:
Xin xem phần: Thông tin thuốc
3. KHUYẾN CÁO DƯỢC LÂM SÀNG QUÝ 1-2018
3.1. Tổng kết công tác giám sát và can thiệp dược lâm sàng:
Công tác giám sát được thực hiện trên 211 HSBA nội trú và 1436 toa thuốc ngoại trú. Ngoài ra, đơn vị dược lâm sàng cũng thực hiện 54 trường hợp hội ý/hội chẩn với các khoa lâm sàng trong quá trình điều trị. Chủ yếu là hội chẩn về liều kháng sinh (đặc biệt là TDM Vancomycin 45/354 trường hợp), phối hợp kháng sinh và tư vấn thông tin thuốc. TDM Aminoglycosid, tiến hành hội chẩn 01 ca Amikacin. Hội ý/ hội chẩn giảm so với quý 4 -2019 (84 trường hợp) và một số ca hội ý qua điện thoại chưa được ghi nhận vào sổ báo cáo tăng cường hoạt động và ghi nhận đầy đủ các can thiệp dược lâm sàng.
Bên cạnh đó, đơn vị dược lâm sàng và thực hiện 504/1674 (khoảng 30%, tăng hơn quý 4 là 14%, và số lượng can thiệp tăng gần gấp đôi 504 so với 279 của quý 4-2018) can thiệp trong quá trình điều trị thuốc để kịp thời hỗ trợ công tác điều trị của bác sỹ. Số lượng can thiệp tăng nhiều do dược sĩ nhà thuốc thực hiện điều chỉnh khi có nguy cơ tương tác thuốc, đồng thời tư vấn hướng dẫn cho bệnh nhân (227/504). Trong 504 can thiệp, có 489 (97%) trường hợp được thực hiện kịp thời chủ yếu là các can thiệp chỉnh liều và thông tin. Trong quý 1-2019, các can thiệp của đơn vị dược lâm sàng đạt được 100% sự thống nhất ý kiến với bác sĩ, một kết quả rất đáng ghi nhận.
Điểm nổi bật của hoạt động giám sát và can thiệp dược lâm sàng trong quý 1-2019:
-
Rà soát và can thiệp các y lệnh, toa thuốc có nguy cơ tương thuốc, cảnh báo dược.
-
Duyệt y lệnh nội trú 03 khoa cấp cứu và duyệt kháng sinh hạn chế (danh sách mở rộng) nguyên ngày và tất cả các ngày làm việc.
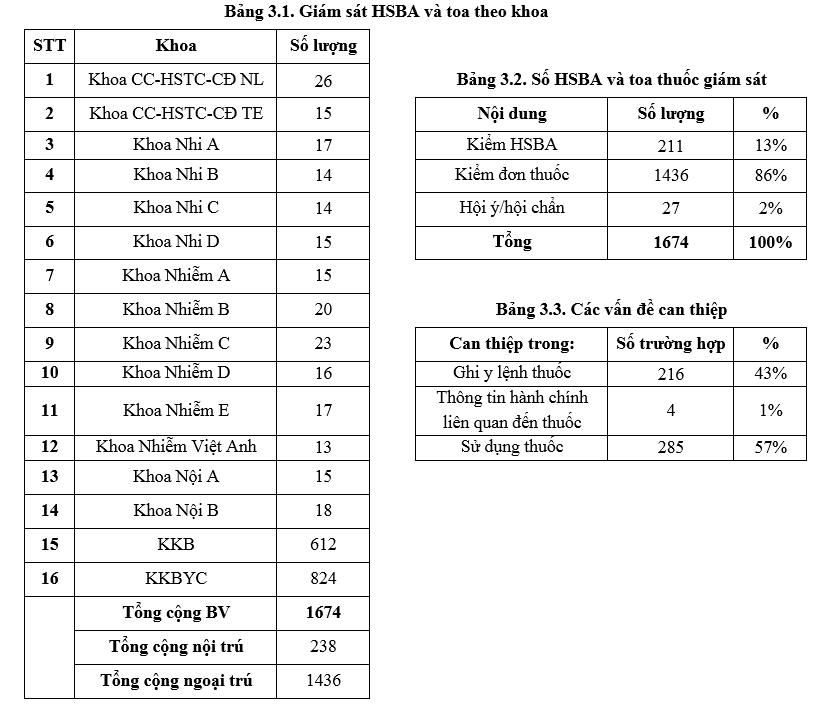
3.2. Kết quả tiêu chí giám sát hồ sơ bệnh án, đơn thuốc và can thiệp DLS:
Toàn bệnh viện đạt 11 tiêu chí về sử dụng thuốc khoảng 86% trở lên (giảm so với quý 4 -2018 (90%)); các tiêu chí đánh giá đều giảm nhẹ so với quý 4-2018 (y lệnh thuốc chưa đúng quy định, báo cáo ADR chưa đầy đủ và kịp thời, chỉ định kháng sinh một số khoa thiếu phân tầng hoặc phân tầng nhóm nguy cơ chưa phù hợp, thiếu/chưa hoàn chỉnh biên bản hội chẩn).
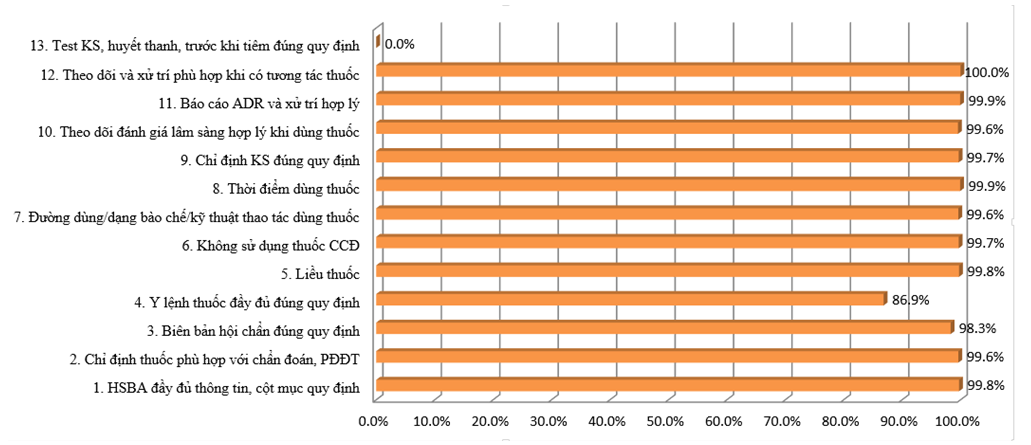
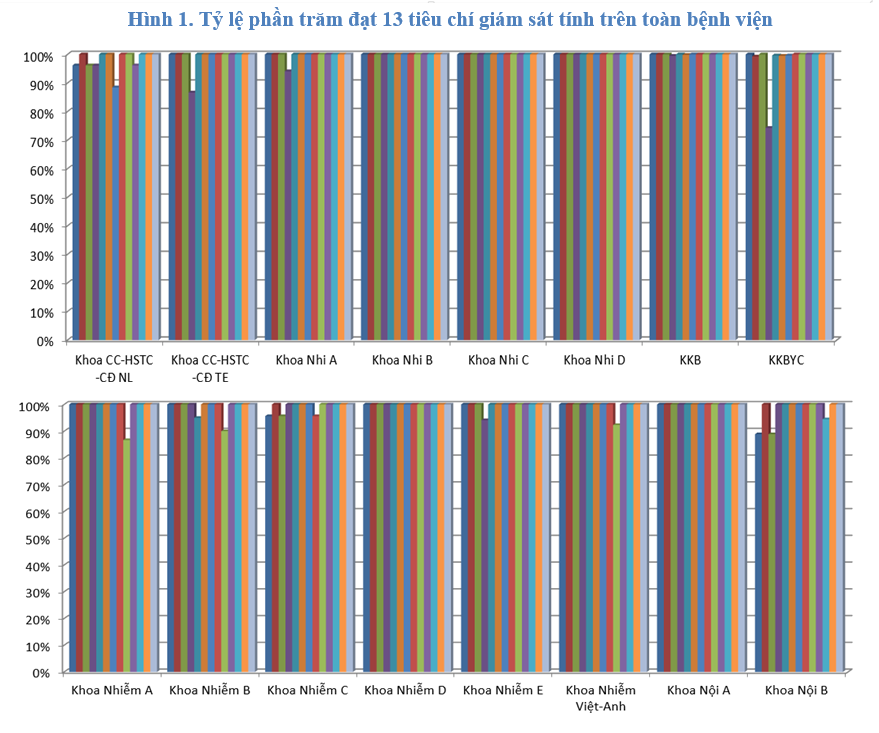

Khoa khám bệnh theo yêu cầu kê toa và ghi y lệnh chưa đúng khá nhiều chiếm gần 26% do sao chép y lệnh BS không đúng (nhầm lẫn trong việc sao chép tên thuốc, trùng hoạt chất); tỷ lệ này cao hơn so với quý 4-2018 (15%).
3.3. Khuyến cáo dược lâm sàng:
a. Thực hiện Hướng dẫn sử dụng kháng sinh mới và làm Phiếu yêu cầu Kháng sinh hạn chế bằng hệ thống FPT. Lưu ý các vấn đề sau:
-
Phân tầng đúng nhóm nguy cơ, nhấn nút “MŨI TÊN” kế bên ô nhóm nguy cơ để phần mềm tự động cập nhật nhóm nguy cơ.
-
Ghi các thông tin cận lâm sàng, chẩn đoán hình ảnh cần cho việc duyệt kháng sinh (Công thức máu, SCr,…).
-
Nếu sử dụng kháng sinh không theo hướng dẫn với nhóm nguy cơ -> Ghi rõ lý do, ý kiến hội chẩn ở cột “Lý do sử dụng kháng sinh”
b. Quy trình duyệt kháng sinh:
-
Làm phiếu và duyệt kháng sinh cấp Trưởng khoa trong 24 giờ.
-
Bộ phận DLS và Ban QLSDKS/P.KHTH duyệt trong 24 giờ.
-
Quy trình này phải hoàn tất trong 48 giờ. -> Ngày thứ 3 chưa hoàn tất phiếu hoặc phiếu không được duyệt đồng ý sẽ CHẶN KHÔNG PHÁT THUỐC. Nếu ngày thứ 6 là ngày thứ 2 của việc dùng thuốc -> Phát thuốc ngày thứ 6 nhưng KHÔNG PHÁT THUỐC ngày thứ 7 – Chủ nhật.
-
Duyệt kháng sinh hạn chế thực hiện nguyên ngày từ Thứ 2- thứ 6. Giờ trực sẽ không duyệt và không chặn thuốc. Nếu có trường hợp nào gấp các khoa lâm sàng có thể liên hệ P. DLS số 208 để hỗ trợ.
-
Khoa dược sẽ báo các trường hợp chặn thuốc cho khoa lâm sàng.
-
DLS gọi báo các trường hợp trả phiếu, có vấn đề khi duyệt.
c. Một số HSBA chưa phân tầng nhóm nguy cơ bệnh nhân khi sử dụng kháng sinh (Nhiễm A, B, E, Nhiễm Việt Anh, CCNL, Nội B).
d. Vẫn còn nhập sai tên thuốc và y lệnh (KKBYC và KKB: 216 đơn thuốc) => kiểm tra kỹ toa thuốc.
e. Một số đơn thuốc bị trùng lắp hoạt chất hoặc các thuốc cùng một nhóm: trùng Levocetirizin, vitamin A (KKBYC: 3 đơn thuốc); phối hợp Adefovir và Tenofovir (KKBYC: 1 đơn thuốc).
f. Lưu ý kê thuốc phù hợp chẩn đoán theo phác đồ điều trị: dự phòng sau phơi nhiễm HIV bằng Lamivudin với liều 150 mg/lần x 2 lần/ngày hoặc 300 mg/lần/ngày. (KKBYC: 2 đơn thuốc kê liều Lamivudin 100mg/ngày chưa đúng phác đồ).
g. Ghi y lệnh thuốc hướng thần và gây nghiện; thuốc kháng sinh đúng quy định và đánh số ngày sử dụng (Nhiễm C, Nội B, CCNL, CCTE, Nhiễm E)
h. Khuyến cáo về liều điều trị:
-
Khuyến cao xem xét kỹ chế độ liều thuốc tránh trường hợp ghi lại y lệnh ngày trước, đặc biệt các thuốc kháng sinh.
-
Thận trọng khi kê đơn trên các đối tượng đặc biệt như phụ nữ có thai, phụ nữ đang trong thời kì cho con bú, trẻ em, bệnh nhân suy gan/thận hoặc có bệnh gan/thận…(Bs kê Dermovat với thành phần Clobetasol chống chỉ định cho trẻ em < 12 tuổi).
-
Thời gian dùng thuốc chưa đúng phác đồ: Chẩn đoán HP(+), bs kê đơn Levofloxacin 500mg: 1 viên/ngày x 3 tuần; Bs cho AT Desloratadin 1 ống (2.5mg / 5ml)/lần x 3 lần/ngày (KKBYC) -> Khuyến cáo Desloratadin liều dùng thông thường cho trẻ em mắc bệnh viêm mũi dị ứng:
≥ 6 tháng <12 tháng: 1 mg, uống mỗi ngày một lần.
≥ 1 tuổi <6 tuổi: 1,25 mg, uống mỗi ngày một lần.
≥ 6 tuổi <11 tuổi: 2,5 mg, uống mỗi ngày một lần.
≥ 12 tuổi, người lớn: 5 mg, uống mỗi ngày một lần.
i. Tương tác thuốc:
-
Các cảnh báo tương tác thuốc có thể xảy ra trong tháng -> khuyến cáo nhằm hạn chế khả năng tương tác, nâng cao việc sử dụng thuốc an toàn, hợp lý và hiệu quả.
-
Lưu ý Hyoscin butylbromid và Kali clorid dùng dạng uống -> giảm nhu động dạ dày và đường ruột -> tạo ra nồng độ cao ion kali, tăng thời gian tiếp xúc với niêm mạc đường tiêu hóa.
-
Lưu ý những tương tác thuốc mức độ 5 và cân nhắc thực hiện theo xử trí được khuyến cáo, đặc biệt những tương tác chống chỉ định phối hợp với nhau. (KKBYC: Efavirenz gây cảm ứng mạnh isoenzymes CYP450 -> Giảm nồng độ velpatasvir huyết -> Chống chỉ định MỨC ĐỘ 5 -> Khuyến cáo đổi thuốc điều trị viêm gan C khác).
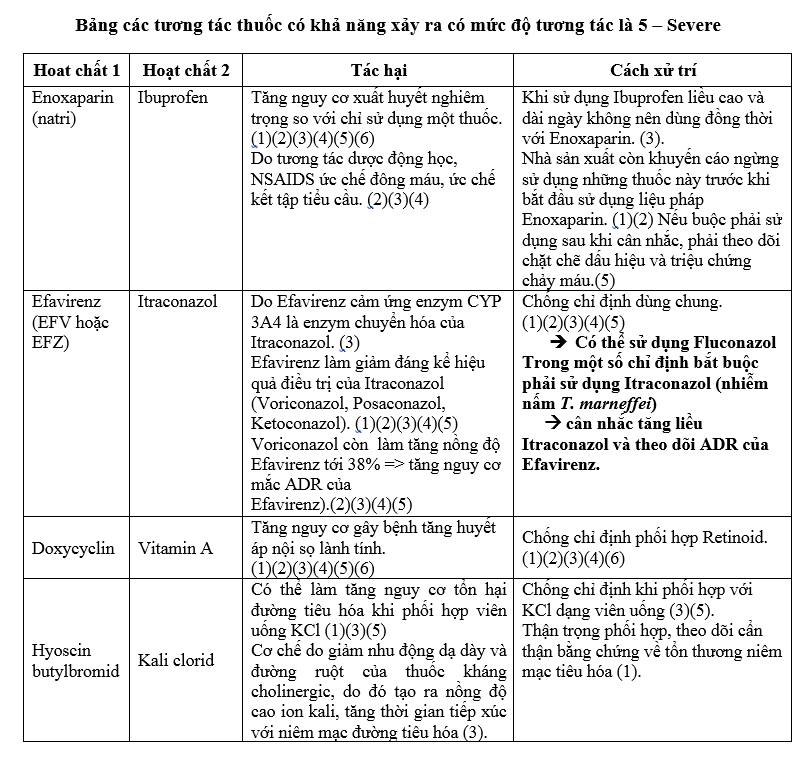
j. Pha và truyền thuốc:
-
Pha truyền các loại dung dịch dinh dưỡng (amino acid, lipid,…) cần tham khảo ý kiến của Dược vì tính tương kỵ/tương đồng của các chế phẩm khác nhau.
-
Lưu ý thời điểm dùng thuốc khi kê đơn để đạt được hiệu quả tối đa và giảm thiểu được tác dụng phụ của thuốc => theo NSX, các thuốc PPI được khuyến cáo dùng trước ăn ít nhất 30 phút và Kaliclorid dùng trong hoặc sau khi ăn với nhiều nước.
-
Sử dụng PPI dạng chế phẩm vi hạt bao tan trong ruột cho bệnh nhân uống qua sonde dạ dày để bảo đảm hiệu quả của PPI.
4. CHUYÊN ĐỀ: ĐỘ LỌC CẦU THẬN và HIỆU CHỈNH LIỀU THUỐC
Độ lọc cầu thận (GFR – Glomerular filtration renal) thường được khuyến cáo như một chỉ số để đánh giá chức năng thận của bệnh nhân, đặc biệt có ứng dụng rất quan trọng trên lâm sàng như chẩn đoán hoặc đánh giá nguy cơ suy thận mạn, tổn thương thận cấp, tình trạng suy thận tiến triển và hiệu chỉnh liều thuốc. Tuy nhiên, đo trực tiếp và xác định chính xác GFR là không thể nên chúng ta thường sử dụng các công thức ước tính dựa vào các dấu chỉ sinh học như creatinine máu, cystatin-C máu và các yếu tố cá thể như tuổi, giới, chủng tộc, cân nặng, … Trong những thập niên gần đây, cùng với sự phát triển vượt bậc của khoa học kỹ thuật thúc đẩy sự ra đời của các công thức ước tính GFR mới như MDRD, CKD-EPI,…bên cạnh nhưng công thức cổ điển như Cockcroft-Gault, Salazar-Corcoran, …Và cũng từ đó xuất hiện những tranh cãi, không thống nhất giữa các nhà lâm sàng là “Công thức ước tính GFR nào là chính xác nhất có thể ứng dụng trên lâm sàng, đặc biệt là trong việc hiệu chỉnh liều thuốc?”. Vì vậy, trong chuyên luận này góp nhặt những khuyến cáo của các chuyên gia trên thế giới để phần nào trả lời vấn đề còn tranh luận trên.
4.1. Các công thức ước tính độ lọc cầu thận
Công thức Cockcroft-Gault:
Do Cockcroft DW, Gault MH được phát triển từ năm 1973, thường được biết như là độ thanh thải creatinine (CrCl – Creatinin clearance).[1]
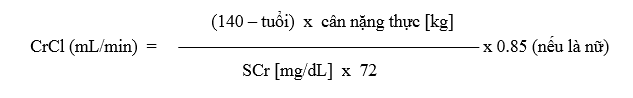
Tuy nhiên, công thức này không áp dụng cho bệnh nhân béo phì hoặc suy kiệt thiếu ký, trẻ <18 tuổi, phụ nữ có thai. Công thức này không hiệu chỉnh theo diện tích bề mặt cơ thể do đó nên chuyển đổi về giá trị chuẩn theo diện tích bề mặt cơ thể sẽ cho giá trị chính xác hơn khi cần so sánh với giá trị chức năng thận chuẩn bình thường.
Ngày này, qua các giai đoạn phát triển công thức này được biến đổi dựa vào hiệu chỉnh cân nặng của bệnh nhân.[4,7]

Công thức MDRD (Modification of Diet in Renal Disease):
Năm 1999 [3, 4, 7]
Công thức này ước tính GFR theo diện tích bề mặt cơ thể nên đơn vị tính là mL/phút/1.73m2

Công thức CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration):
Được áp dụng từ năm 2009 [3, 4, 7]
Công thức này ước tính GFR theo diện tích bề mặt cơ thể nên đơn vị tính là mL/phút/1.73m2

Công thức Salazar – Corcoran:
Được phát triển từ năm 1988 [2, 6]

Công thức này được ứng dụng trên đối tượng là bệnh nhân béo phì (BMI ≥30 m2) trên đa số các công cụ ước tính độ lọc cầu thận đối với người béo phì. Tuy nhiên, theo một nghiên cứu tiến hành năm 2012 của Winter MA và cộng sự thì đề xuất với đối tượng người béo phì nên sử dụng công thức Cockcroft-Gault với cân nặng hiệu chỉnh 40% vì [8]:
• Công thức Cockcroft-Gault theo cân nặng thực thường ước tính chức năng thận ở ngưỡng cao
• Công thức Cockcroft-Gault theo cân nặng lý tưởng và cân nặng hiệu chỉnh theo lượng cơ thường ước tính chức năng thận ở ngưỡng thấp
• Công thức Cockcroft-Gault theo cân nặng hiệu chỉnh 40% cho sự ước tính chính xác nhất (thường trong khoảng chênh lệch 5 mL/min)
Đối lập với ý kiến trên, có một nghiên cứu năm 2009 do Demirovic JA và cộng sự cho thấy [2]:
• Công thức Cockcroft-Gault theo cân nặng thực thường ước tính chức năng thận ở ngưỡng rất cao.
• Công thức Cockcroft-Gault theo cân nặng hiệu chỉnh 30% hoặc 40%, công thức Salazar thường ước tính chức năng thận ở ngưỡng cao.
• Công thức Cockcroft-Gault theo cân nặng lý tưởng, công thức MDRD thường ước tính chức năng thận ở ngưỡng thấp.
• Công thức MDRD là ước tính ít chính xác nhất chức năng thận
Hiện tại, bệnh viện Bệnh Nhiệt Đới đang áp dụng công thức Salazar hoặc công thức Cockcroft-Gault theo cân nặng hiệu chỉnh 40% cho đối tượng bệnh nhân béo phì trong việc đánh giá chức năng thận và hiệu chỉnh liều thuốc.
4.2. So sánh giữa 3 công thức ước tính GFK thường sử dụng: Cockcroft-Gault, MDRD và CKD-EPI
Công thức Cockcroft-Gault được sử dụng sớm nhất và ứng với giá trị SCr được đo bằng phương pháp enzyme truyền thống (Jaffe) và bị sai số ở ngưỡng cao khoảng 10-40% so với độ thanh thải creatinin nếu sử dụng giá trị SCr bằng phương pháp đo tiêu chuẩn – IDMS mới hiện nay [7]. Do đó, việc ước tính GFR bằng công thức Cockcroft-Gault với SCr đo bằng IDMS không được khuyến cáo. [3, 4, 7]
Các tài liệu khuyến cáo hiện nay đều công nhận MDRD và CKD-EPI chính xác hơn phương pháp Cockcroft-Gault cổ điển khi ước tính độ lọc cầu thận, đặc biệt là khi sử dụng giá trị SCr đo theo phương pháp IDMS. Tuy nhiên, hiện nay Bệnh viện Bệnh Nhiệt Đới vẫn đang sử dụng phương pháp Jaffe để đo SCr nên áp dụng công thức gốc MDRD để ước tính GFR và không áp dụng được công thức CKD-EPI.
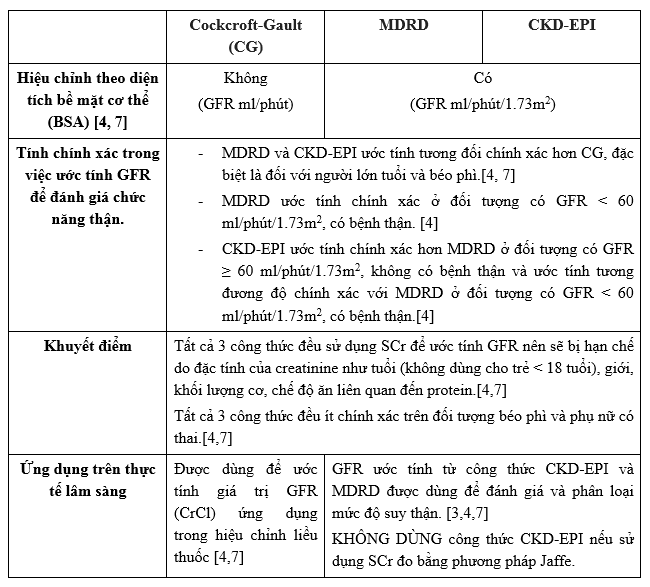
Có các nghiên cứu so sánh giữa các phương pháp để xác định phương pháp chính xác ước tính GFR (eGFR) dùng trong hiệu chỉnh liều thuốc. Tuy nhiên, kết quả cho thấy không có sự khác biệt về liều hiệu chỉnh theo từng công thức ước tính. Đồng thời, cả 3 công thức đều có những hạn chế trong việc ước tính độ lọc cầu thận. Một số khuyến cáo về các công thức ước tính chức năng thận:
• Có thể dùng các công thức MDRD, CKD-EPI, CG để ước tính GFR và hiệu chỉnh liều. Theo các nghiên cứu thì ước tính GFR theo CG kém chính xác hơn các phương pháp còn lại. Vì vậy, việc chỉnh liều không nên giới hạn chỉ bằng công thức CG, mà có thể dùng các công thức chính xác hơn. [7]
• GFR tính theo công thức MDRD mới cập nhật (ứng dụng khi SCr được đo bằng IDMS) được Hướng dẫn của National Kidney Diseases Education Program 2013 khuyến cáo để phân loại tình trạng suy thận mạn tính.
• Tương tự, GFR tính theo công thức CKD-EPI (ứng dụng khi SCr được đo bằng IDMS) được Hướng dẫn của Kidney Disease Improving Global Outcomes (KDIGO) 2012 khuyến cáo để phân loại tình trạng suy thận mạn tính. Bệnh viện Bệnh Nhiệt Đới không ứng dụng công thức này do không dùng phương pháp đo SCr bằng IDMS.
• Hiện nay các tài liệu khuyến cáo hiệu chỉnh liều thuốc vẫn áp dụng công thức Cockcroft-Gault, ví dụ: Sanford Guide 2018, Lexicomp drug reference hand book, Antibiotic Essentials 2016, Drug Prescribing in Renal failure 15th , vì những lý do :
-
Công thức CG ra đời và ứng dụng từ đầu trong các nghiên cứu dược động học dùng để hiệu chỉnh liều thuốc. Được công bố trong các tài liệu hướng dẫn dùng thuốc của nhà sản xuất nên trở thành một tiêu chuẩn cho việc chỉnh liều.[4]
-
Không có sự khác biệt về chế độ liều điều chỉnh khi sử dụng công thức MDRD và CG để ước tính GFR. [3, 4]
-
Theo KDIGO 2012, việc hiệu chỉnh liều thuốc nên dựa trên giá trị GFR (ml/phút) – không hiệu chỉnh theo BSA, do đó khi áp dụng công thức MDRD phải tính lại với BSA thực tế của bệnh nhân. Tuy nhiên, chưa có nghiên cứu so sánh rõ ràng ảnh hưởng của việc hiệu chỉnh theo hoặc không theo BSA này, nên chưa có khuyến cáo chính xác.[3, 4, 7]
4.3. Kết luận:
Với những khuyến cáo trên, hiện tại Bệnh viện Bệnh Nhiệt Đới đang sử dụng công thức Cockcroft-Gault ước tính độ thanh thải theo kết quả xét nghiệm đo creatinine máu ngay trên phiếu trả kết quả để bác sĩ dựa vào đó hiệu chỉnh liều thuốc. Đồng thời, các công thức ước tính GFR như Cockcroft-Gault, MDRD (để phân loại mức độ suy thận), Salazar (cho bệnh nhân béo phì), Schwartz (cho trẻ em) được tích hợp trên ứng dụng app/web EMED.BVBND.VN của Bệnh viện để bác sĩ tính toán và ước tính GFR cho bệnh nhân.
Tóm lại, chỉnh liều thuốc quan trọng vẫn phải theo tình trạng đáp ứng lâm sàng, cân nhắc giữa các lợi ích và nguy cơ có hại khi sử dụng chế độ liều cụ thể trên từng cá thể bệnh nhân. Đánh giá và theo dõi các vấn đề về chức năng thận phải kết hợp nhiều yếu tố lâm sàng trong cả quá trình diễn tiến bệnh và không nên hoàn toàn dựa vào giá trị SCr hoặc GFR đơn thuần.
Tài liệu tham khảo
- Cockroft D.W., Gault M.H. Prediction of creatinine clearance from serum creatinine. Nephron. 1976;16(1):31-41Uptodate, (2019).
-
Demirovic JA, Pai AB, Pai MP. Estimation of creatinine clearance in morbidly obese patients. Am J Health Syst Pharm. 2009 Apr 1;66(7):642-8
-
KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease 2013 Jan; 3(1).
-
National Kidney Disease Education Program. Chronic kidney disease and drug dosing: information for providers. Available at: http:// www.nkdep.nih.gov/professionals/drugdosing-information.htm. Posted September 2009. Revised January 2010. Accessed Friday, June 11, 2010.
-
Stevens LA, Nolin TD, Richardson MM, et al. on behalf of the Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI). Comparison of drug dosing recommendations based on measured GFR and kidney function estimating equations. Am J Kidney Dis. 2010;55(4):660-670.
-
Salazar DE, Corcoran GB. Predicting creatinine clearance and renal drug clearance in obese patients from estimated fat-free body mass. Am J Med. 1988 Jun;84(6):1053-60
-
Uptodate 2018.
-
Winter MA, Guhr KN, Berg GM. Impact of various body weights an serum creatinine concentrations on the bias and accuracy of Cockcroft-Gault equation. Pharmacotherapy. 2012:32(7):604-12.