- A. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
- B. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC
- C. GIÁM SÁT HSBA VỀ THUỐC
- D. CHUYÊN ĐỀ: “HIỆU CHỈNH LIỀU KHÁNG SINH Ở BỆNH NHÂN ĐANG TIẾN HÀNH CRRT”
- 1. Tình trạng bệnh lý của bệnh nhân
- 2. Đặc tính của thuốc kháng sinh
- 2.1. Trọng lượng phân tử
- 2.2. Tỷ lệ gắn kết protein
- 2.3. Thể tích phân
- 2.4. Thải trừ
- 3. Đặc tính CRRT
- 3.1. Phương thức CRRT
- 3.2. Màng lọc (Quả lọc)
- 3.3. Tốc độ dòng
- 3.4. Độ thanh thải trong các phương thức CRRT
- 4. Thực hành lâm sàng hiệu chỉnh liều kháng sinh khi bệnh nhân đang tiến hành CRRT
- 5. Kết luận
A. PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR):
1. Tổng kết công tác báo cáo ADR:
Quý 1-2017 ghi nhận có 29 báo cáo ADR xảy ra ở 09 khoa (theo bảng).

Trong đó có 1 ca đe dọa tính mạng do Vitamin K1, tất cả đều được xử trí kịp thời. 18 trường hợp (62%) là do kháng sinh, chủ yếu là vancomycin (5/18 ca), tiếp theo là Ceftriaxone (4/18 ca). 11 ca do các thuốc khác thì chủ yếu là Diazepam (6/11 ca).
2. Phản hồi Trung tâm DI&ADR Quốc gia về các ADR của Bệnh viện Bệnh Nhiệt Đới:
a. Về ADR do Vancomycin: sốc phản vệ
Phản ứng phản vệ và sốc phản vệ là phản ứng có hại hiếm gặp khi sử dụng Vancomycin (1/1000).
Để xử trí phản ứng, cần tuân thủ theo phác đồ cấp cứu sốc phản vệ do Bộ Y tế ban hành: ngừng dùng thuốc nghi ngờ, cho bệnh nhân nằm tại chỗ, sử dụng thuốc tiêm: tiêm dưới da adrenalin dung dịch 1/1,000 và các thuốc chống dị ứng đặc hiệu, thở oxy, bù nước, dung dịch điện giải nếu cần. Theo tài liệu mới cập nhật về sốc phản vệ của "Viện quốc gia Hoa Kỳ về Dị ứng và Bệnh nhiễm trùng" năm 2006, có thể xử trí bằng cách tiêm bắp ngay ở trước bên đùi 0,3-0,5ml dung dịch adrenalin 1/1000 (trẻ em: 0,01mg/kg cân nặng) lặp lại mỗi 5-15 phút (có thể ngắn hơn 3-5 phút tùy đáp ứng và độ nặng trên lâm sàng), thở oxy, đặt nội khí quản nếu cần, truyền dịch tĩnh mạch (NaCl 0,9%) để tăng thể tích huyết tương, dùng thuốc kháng Histamin, hít thuốc chủ vận beta-adrenergic nếu co thắt phế quản, tiêm tĩnh mạch Hydrocortison hoặc Prednisolon.
b. Về ADR do Amphotericin B: Hạ Kali máu.
Để xử trí phản ứng, bổ sung kali cho bệnh nhân theo đường uống hoặc tĩnh mạch. Tiếp tục theo dõi kali máu của bệnh nhân để có bước xử trí tiếp theo.
Theo Dược thư Quốc gia Việt Nam 2 năm 2015, amphotericin B có thể gây ra các phản ứng trên chuyển hóa như rối loạn điện giải giảm kali huyết, giảm magnesi huyết (1/100). Amphotericin B dạng phức hợp lipid và dạng liposom đều ít gây độc thận hơn so với chế phẩm thông thường, tuy nhiên vẫn gây độc thận và thường hồi phục. Tổn thương vĩnh viễn có thể xảy ra với chế phẩm thông thường với liều>1mg/kg/ngày hoặc đã có tổn thương thận từ trước, điều trị kéo dài, cơ thể mất natri hoặc dùng đồng thời thuốc có tiềm năng gây độc cho thận. Các dấu hiệu nhiễm độc thận bao gồm tăng urê huyết, tăng creatinin huyết thanh, giảm Kali, Magnesi huyết và nhiễm acid ống thận. Có thể làm giảm nhiễm độc thận bằng cách tiêm truyền dung dịch NaC 0,9% 250-1000ml trong vòng 30-45 phút ngay trước khi dùng Amphoterin B. Có thể tiêm truyền lại ngay dung dịch NaCl 0,9% sau khi tiêm truyền Amphotericin B. Thể tích và tốc độ truyền dung dịch NaCl 0,9% phụ thuộc vào cân nặng và tình trạng tim mạch của người bệnh.
Theo khuyến cáo trong nhãn thuốc chứa Amphotericin B lưu hành tại Anh, cán bộ y tế cần lưu ý thận trọng trong trường sử dụng thuốc kéo dài cho bệnh nhân, thường xuyên theo dõi các chỉ số điện giải, đặc biệt kali và magnesi máu và tiến hành kiểm tra chức năng gan, thận vào tạo máu của bệnh nhân ít nhất 1 lần/tuần. Điều này đặc biệt quan trọng trên bệnh nhân sử dụng đồng thời các thuốc khác có độc tính trên thận. Nếu xảy ra suy giảm chức năng thận hoặc rối loạn điện giải mức độ nghiêm trọng, cân nhắc giảm liều thuốc, tạm thời ngừng hoặc ngừng hẳn thuốc.
c. Về ADR do Vitamin K1: sốc phản vệ
Theo Dược thư Quốc gia Việt Nam năm 2009, phản vệ là phản ứng có hại nghiêm trọng đã được ghi nhận khi sử dụng Phytomenadion. Cơ sở dữ liệu Quốc gia về ADR giai đoạn 2010-2012 đã ghi nhận 09 báo cáo liên quan đến Phytomenadion, trong đó có 03 báo cáo về phản ứng phản vệ, sốc phản vệ.
Để xử trí phản ứng, cần tuân thủ theo phác đồ cấp cứu sốc phản vệ do Bộ Y tế ban hành.
Ngoài ra, cán bộ y tế cũng cần lưu ý khuyến cáo cách sử dụng Phytomenadion (theo Dược thư Quốc gia năm 2015) như sau:
-
Có thể dùng đường tiêm dưới da (tùy theo khuyến cáo của nhà sản xuất). Nên tránh tiêm bắp vì có nguy cơ bị tụ máu. Chỉ dùng đường tĩnh mạch khi không thể dùng đường uống hoặc trong trường hợp cấp cứu, chảy máu nặng sau khi dùng các thuốc kháng Vitamin K.
-
Khi tiêm tĩnh mạch, cần tiêm/truyền thật chậm dạng dung dịch mixen , tốc độ truyền không quá 1mg/phút (3mg/m2/phút ở trẻ em và trẻ sơ sinh). Dạng dung dịch trong dầu không nên dùng đường tĩnh mạch.
-
Có thể truyền Vitamin K1 cùng với dung dịch tiêm truyền Natri Clorid 0,9% hoặc Glucose 5%.
*Chú ý: sản phẩm Vitamin K1 10mg/1ml được sản xuất bởi Công ty TW 25 hiện có tại BV chỉ tiêm bắp, tiêm truyền tĩnh mạch chậm)
B. THÔNG TIN THUỐC, CẢNH GIÁC DƯỢC
Xem phần Thông tin thuốc.
C. GIÁM SÁT HSBA VỀ THUỐC
Công tác giám sát được thực hiện trên 1.231 HSBA nội trú và HƠN 392 toa thuốc ngoại trú bởi các khoa, phòng -> thấp hơn so với quý 4-2016. Tỷ lệ trung bình các tiêu chí của cả bệnh viện đạt trên 95%.
Về thuốc, được giám sát theo 11 tiêu chí đối với nội trú (Hình 1).

Nhìn chung kết quả giám sát tỷ lệ phù hợp theo 11 tiêu chí của hầu hết các khoa khá cao (khoảng từ 80%) và tuy nhiên 03 tiêu chí “Biên bản hội chẩn dùng thuốc, Chỉ định sử dụng KS, Báo cáo ADR” có tỷ lệ đạt thấp hơn các tiêu chí khác nhưng cũng đã tăng so với quý 4-2016.
Tuy nhiên vẫn còn một số sai sót cần cải thiện:
-
HSBA còn một số thiếu sót lưu ý: không đánh số thứ tự ngày dùng thuốc, ghi không đúng thứ tự kê toa thuốc, thiếu biên bản hội chẩn dùng thuốc, chưa ký tên khi sửa hoặc gạch bỏ.
-
Một số trường hợp kê thuốc không phù hợp: sử dụng các thuốc chống chỉ định tương đối hoặc cần thận trọng khi dùng trên 1 số đối tượng đặc biệt (meloxicam, acetylcystein trên bệnh nhân tiền sử hen suyễn), bệnh nhân dấu chứng nhiễm trùng chưa rõ dùng KS.
-
Một số trường hợp xảy ra tác dụng phụ có ghi xử trí và theo dõi trong HSBA nhưng không làm báo cáo ADR, thường cần DLS khuyến cáo mới làm báo cáo (nhiễm E, nhiễm B).
-
Tiêu chí “Chỉ định KS đúng quy định” đã tăng so với quý 4-2016 là 96.1% do các khoa tích cực thực hiện -> tỷ lệ từng khoa cũng tăng. Ví dụ: Nhiễm B 86.3%, Nội A 91.5% cao hơn so với quý 4-2016. Tuy nhiên, tỷ lệ đạt vẫn thấp hơn so với các tiêu chí khác. Chủ yếu là các khoa thiếu phân tầng khi sử dụng kháng sinh, đặc biệt là các kháng đướng uống không nằm trong danh mục kháng sinh hạn chế và phân tầng chưa hợp lý.
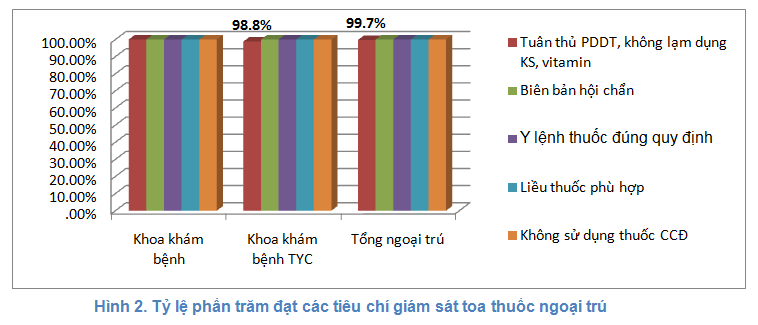
Đối với khoa khám bệnh ngoại trú đánh giá 4 tiêu chí (Hình 2).
Kết quả tỷ lệ phù hợp của 4 tiêu chí ở khoa khám bệnh đạt 100%. Riêng khoa khám bệnh theo yêu cầu có tỷ lệ thấp hơn nhưng vẫn trên 98%.
Khuyến cáo:
a. Trong biên bản hội chẩn đề nghị bác sĩ ghi tác dụng phụ hoặc nghi ngờ tác dụng phụ, có hướng xử trí trên lâm sàng, báo cáo ADR đúng qui trình (Nhiễm E, Nhiễm B).
b. Phân tầng kháng sinh theo qui định, vẫn còn các ca bệnh chưa phân tầng hoặc phân tầng chưa hợp lý. Đề nghị làm phiếu duyệt kháng sinh hạn chế đúng thời gian qui định. Vẫn có khoa duyệt trễ so với quy định > 3ngày (Nhiễm Việt Anh, Nhiễm A). Đề nghị các bác sỹ làm phiếu kháng sinh hạn chế nên ghi đầy đủ các thông tin cận lâm sàng có được để duyệt toa được dễ dàng và thuận tiện hơn (KSĐ, xét nghiệm CTM, các thủ thuật …).
c. Lưu ý theo dõi chức năng thận và cân nhắc chỉnh liều khi chức năng thận thay đổi.
d. Cân nhắc xuống thang theo KSĐ.
e. Không uống cùng thời điểm Ciprofloxacin và Kẽm (Zinenutri) do mất tác dụng KS.
f. Cách pha thuốc:
-
MgSO4 không pha chung với các dung dịch chứa kim loại nặng do tạo kết tủa như chứa Calci (CaCl2)… MgSO4 pha loãng trong NaCl 0.9%, Glucose 5%, và có thể tương thích với KCl.
-
Khuyến cáo pha loãng vitamin K1 khi TTM (với ≤10ml NaCl 0.9% hoặc Glucose 5% - do K1 dạng dầu), tiêm tốc độ chậm: 1mg K1/ 1 phút à nên sử dụng bơm tiêm tự động.
-
Omelupem (Omeprazol 40mg inj) NSX khuyến cáo truyền tĩnh mạch: 1 lọ 40mg + 100 ml NaCl 0.9%/Glucose 5%, truyền trong 20 – 30 phút. Dung dịch sau pha ổn định trong 12h (NaCl) và 3h (Glucose).
g. Luật dược năm 2017: Hạn dùng của thuốc đối với thuốc chỉ ghi tháng, năm là ngày cuối tháng. VD date 04/2017 à hạn dùng là cuối ngày 30/04/2017, sau ngày này không được dùng.
h. HĐT&ĐT khuyến cáo về sử dụng Linezolide:
-
Là thuốc dự trữ cho trường hợp kháng Vancomycin nên cần hạn chế không sử dụng rộng rãi.
-
Không phối hợp Vancomycin và Linezolide vì cùng phổ kháng khuẩn và chưa có tài liệu chứng minh tác dụng hiệp đồng của 2 thuốc này.
-
Tài liệu nghiên cứu trái chiều và không rõ ràng về việc Linezolide thấm qua hàng rào máu não.
D. CHUYÊN ĐỀ: “HIỆU CHỈNH LIỀU KHÁNG SINH Ở BỆNH NHÂN ĐANG TIẾN HÀNH CRRT”
VIẾT TẮT
-
IHD: Intermittent Hemodialysis – Thẩm tách máu ngắt quãng (chạy thận nhân tạo)
-
CRRT: Continuous renal replacement therapy – Trị liệu thay thế thận liên tục
-
CVVH: Continuous veno-venous hemofiltration
-
CVVHD: Continuous veno-venous hemodialysis
-
CVVHDF: Continuous veno-venous hemodiafiltration
Trong khoảng 20 năm gần đây, phương pháp trị liệu thay thế thận liên tục – CRRT (hay còn gọi là lọc máu liên tục) được sử dụng ngày càng nhiều như là một phương thức lọc sạch máu ngoài cơ thể cho những bệnh nhân nặng bị sốc nhiễm trùng, nhiễm trùng nặng đe dọa tính mạng nằm ở khoa Cấp Cứu Hồi Sức và Chống Độc (CCHS-CĐ). CRRT không chỉ dành riêng cho các bệnh nhân suy thận cấp có huyết động không ổn định mà đã được mở rộng chỉ định điều trị cho nhóm bệnh nhân không suy thận. Và đã có rất nhiều bệnh nhân mắc những bệnh nặng khó qua khỏi hiện nay có thêm cơ hội được điều trị và sống nhờ kỹ thuật CRRT.
Mặc khác, một trong những vấn đề rất quan trọng liên quan chặt chẽ đến tỷ lệ tử vong và bệnh tật của bệnh nhân nằm ở khoa CCHS-CĐ là liệu pháp điều trị kháng sinh nhằm kiểm soát tình trạng nhiễm trùng. Mục tiêu cần đạt được trong việc sử dụng kháng sinh là liều thuốc phải đảm bảo được nồng độ đạt hiệu quả điều trị đồng thời trong ngưỡng an toàn hạn chế mức tối thiểu tác dụng phụ. Tuy nhiên, tình trạng bệnh nhân nhiễm trùng nặng, sốc, suy thận cấp, đang tiến hành CRRT ảnh hưởng đến cả dược động học và dược lực của kháng sinh sử dụng một cách rất khó dự đoán. Còn rất hạn chế các nghiên cứu về liều kháng sinh sử dụng trên bệnh nhân nằm ICU và chạy CRRT nên rất khó và gần như không thể có được một hướng dẫn cụ thể, hoàn thiện và chính xác về liều của các kháng sinh cho tất cả các bệnh nhân khi đang CRRT. Nói chung, quá trình điều trị cần cá thể hóa và cụ thể trên tình trạng lâm sàng thực tế của từng bệnh nhân.
Một trong những vấn đề được các bác sĩ lâm sàng đưa ra bàn luận là “Liệu liều kháng sinh có đủ để điều trị nhiễm trùng khi tiến hành chạy CRRT cho bệnh nhân không suy thận hay không? Vì vậy, chuyên đề này sẽ bàn luận các yếu tố ảnh hưởng đến việc loại bỏ thuốc kháng sinh trên bệnh nhân đang tiến hành CRRT từ đó làm cơ sở để phần nào dự đoán được liều kháng sinh hợp lý cho bệnh nhân hoặc ít nhất cũng nắm được nguyên tắc cơ bản để hiệu chỉnh liều kháng sinh cho bệnh nhân.
Các yếu tố ảnh hưởng: Tình trạng bệnh lý của bệnh nhân, đặc tính thuốc kháng sinh, đặc tính CRRT
1. Tình trạng bệnh lý của bệnh nhân
Bệnh nhân nặng thường có những rối loạn chức năng cơ quan, huyết động không ổn định dẫn tới các thay đổi về các thông số dược động học của thuốc và kết quả cuối cùng là làm biến đổi nồng độ thuốc trong máu.

2. Đặc tính của thuốc kháng sinh
Một số tính chất nội tại của thuốc ảnh hưởng đến sự thải trừ thuốc bằng CRRT: kích thước phân tử, thể tích phân bố, gắn kết protein, cơ chế thải bỏ.
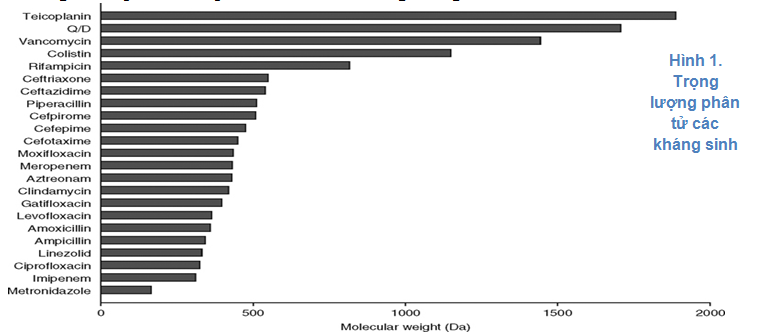
2.1. Trọng lượng phân tử
Thuốc có TLPT nhỏ (< 500 Da) được thải trừ có hiệu quả bằng cơ chế thẩm tách dòng thấp (IHD) và CRRT. Ngoài ra, CRRT còn có thể thải bỏ các thuốc có TLPT lớn và thậm chí thải được các phức hợp phân tử lớn có gắn kết protein (khoảng 20.000-50.000 Da) -> lưu ý liều bổ sung khác nhau giữa IHD và CRRT vì CRRT thải bỏ lượng thuốc gắn kết protein và phân tử thuốc có trọng lướng lớn nhiều hơn IHD.
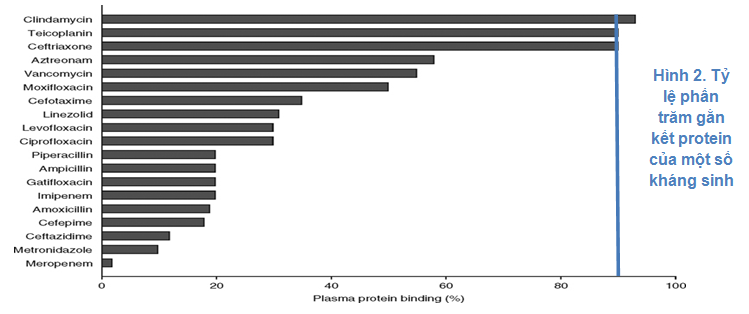
2.2. Tỷ lệ gắn kết protein
Mức độ gắn kết với protein của thuốc ảnh hưởng đến khả năng bị loại thải bởi CRRT. Thuốc gắn kết protein thường tạo thành phức hợp phân tử lớn, nếu > 50.000 Da sẽ khó loại thải bằng CRRT. Những thuốc không gắn kết protein dễ dàng được lọc qua màng lọc.
Ở những bệnh nhân nặng quan sát thấy có tình trạng thấp albumin máu và tỷ lệ thuốc không gắn kết protein (dạng thuốc tự do) tăng từ trung bình đến cao và vì vậy độ thanh thải các thuốc này cũng tăng. Quan trọng hơn, sự gắn kết protein thường là trạng thái cân bằng động nên nồng độ thuốc trong máu sẽ nhanh chóng ổn định hoặc tăng nhẹ nếu sự thanh thải thuốc và chuyển hóa của thuốc bình thường hoặc tăng.
Cần lưu ý đối với các thuốc có tỷ lệ gắn kết protein từ 80-90% trở lên vì khi có sự thay đổi protein máu sẽ ảnh hưởng đáng kể đến nồng độ thuốc.
2.3. Thể tích phân
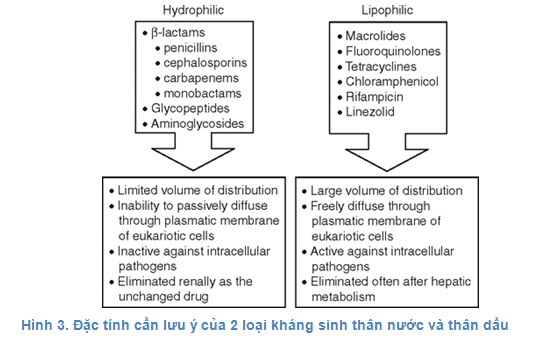
Các thuốc có thể tích phân bố thấp thường thân nước và giới hạn trong lòng mạch máu hoặc khoang kẽ giữa các tế bào và thường được thải trừ dưới dạng không đổi qua thận nên dễ dàng bị loại thải bằng CRRT. Ví dụ: β-lactam, glycopeptid, aminoglycoside, ngoại trừ ceftriaxone và oxacillin vì 2 thuốc này thải trừ qua mật không bị ảnh hưởng lớn bởi CRRT. Ngược lại, những thuốc thân dầu có thể di chuyển tự do qua màng sinh học và phân bố rộng rãi ở các mô tế bào thể tích phân bố lớn và hầu hết được chuyển hóa ở gan trước khi thải trừ và thuốc này thường thải trừ không qua con đường thận (nonrenal elimination) -> ít bị ảnh hưởng khi có sự thay đổi chức năng thận cũng như bị loại bỏ không đáng kể qua CRRT. Ví dụ: macrolid, quinolon, cyclin, chloramphenicol, rifampicin và linezolid, ngoại trừ levofloxacin, ciprofloxacin thải trừ qua thận nên bị loại bỏ qua CRRT. Điều này có nghĩa hầu hết những kháng sinh thân nước sẽ được loại thải bởi CRRT nhiều hơn các kháng sinh thân dầu -> cần thiết có liều bổ sung trong quá trình CRRT.
2.4. Thải trừ
Những thuốc được thải trừ qua thận sẽ dễ dàng loại thải bởi CRRT. Hơn nữa, cần lưu ý thêm liều với những bệnh nhân có chức năng thận bình thường hoặc vẫn còn bảo lưu 1 phần chức năng thận mà đang tiến hành chạy CRRT. Tuy nhiên, cách tăng liều cũng như liều khuyến cáo chưa được chính xác và hoàn thiện mà phụ thuộc vào từng loại kháng sinh, tình trạng bệnh nhân và chế độ CRRT vì mỗi khuyến cáo liều đều dựa vào một nghiên cứu PK/PD cho từng nhóm bệnh cụ thể -> không thể áp dụng đồng loạt và rộng rãi cho tất cả bệnh nhân.
3. Đặc tính CRRT
Cơ chế vận chuyển chất hòa tan trong CRRT, các phương thức lọc (CVVH, CVVHD, CVVHDF…), đặc tính màng lọc, tốc độ dòng máu (QB), tốc độ dịch siêu lọc (QUF), và dịch thẩm tách (QD)… đều ảnh hưởng đến sự thanh lọc thuốc.
3.1. Phương thức CRRT
Có 3 kỹ thuật chính thường sử dụng: siêu lọc – CVVH, thẩm tách – CVVHD, siêu lọc thẩm tách – CVVHDF; cơ chế mỗi loại khác nhau. Nguyên tắc chung, hiệu quả loại thải thuốc của các kỹ thuật khác nhau thường là CVVHDF/CVVHD>CVVH>IHD. Tuy nhiên, độ thanh thải của CRRT (ClCRRT) có thể thay đổi khá đa dạng và chủ yếu phụ thuộc vào tính chất lý hóa đặc thù và dược động học của mỗi hoạt chất.
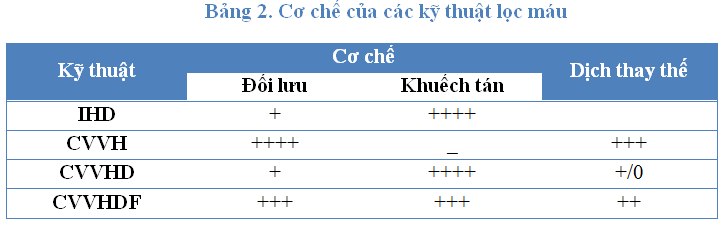
3.2. Màng lọc (Quả lọc)
Tính thấm, cấu tạo và diện tích của màng lọc có ảnh hưởng đáng kể đến quá trình thải bỏ thuốc khi CRRT. Trong CRRT thường sử dụng màng lọc “high flux” có kích thước lỗ lớn hơn và có thể thải bỏ các chất có TLPT lên đến 50.000 Da. Cấu tạo màng lọc trong CRRT cũng khác so với trong IHD thường là các chất tổng hợp: polyacrylonitile, polyamide, polysonfone -> CRRT loại bỏ các chất hoàn tan hiệu quả hơn so với IHD. Khả năng thấm qua màng lọc của 1 chất được thể hiện bằng hệ số lọc (SC –Sieving coefficient).
SC = CUF/CP
CUF: nồng độ thuốc trong dịch siêu lọc
CP: nồng độ thuốc trong huyết tương
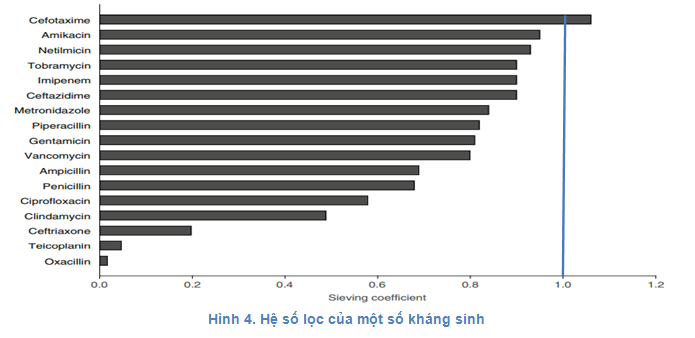
Thuốc có SC=1 có thể tự do qua màng lọc, ngược lại SC = 0 không đi qua màng lọc.
3.3. Tốc độ dòng
Nói chung, tốc độ dòng máu, dòng thẩm tách và dòng siêu lọc càng cao thì loại thải các chất càng nhiều tăng liều thuốc hoặc rút ngắn khoảng cách liều.
3.4. Độ thanh thải trong các phương thức CRRT
Các đặc tính của CRRT cùng cộng hưởng tác động đến độ thanh thải thuốc của khi chạy CRRT (ClCRRT). Chúng ta có thể ước tính ClCRRT dựa vào các chỉ số đặc tính của từng phương thức CRRT.

4. Thực hành lâm sàng hiệu chỉnh liều kháng sinh khi bệnh nhân đang tiến hành CRRT
Hiện nay, hầu hết các tài liệu khuyến cáo liều hiệu chỉnh kháng sinh khi bệnh nhân đang CRRT thường áp dụng trong những trường hợp bệnh nhân có tình trạng suy thận cấp, vô niệu, thiểu niệu. Đây là trạng thái thận của bệnh nhân gần như giảm hoàn toàn, nên độ thanh thải của bệnh nhân lúc này có thể ước tính gần bằng độ thanh thải của CRRT. Và cách hiệu chỉnh liều khi CRRT thường được áp dụng phổ biến là theo các khuyến cáo liều của các tài liệu về kháng sinh (Sanford guide, Antibiotics Essentials, Lexicomp, Uptodate,…) hoặc nhà sản xuất. Tuy nhiên, nếu bệnh nhân có chức năng thận vẫn còn được bảo tồn thì liều hiệu chỉnh khuyến cáo có thể không đủ để cho nồng độ thuốc điều trị hiệu quả. Về nguyên tắc chung, khi đó độ thanh thải của bệnh nhân đang CRRT sẽ bằng độ thanh thải của cá thể bệnh nhân còn được bảo tồn + độ thanh thải của CRRT. Vì vậy, nhìn chung lượng thuốc được loại thải cơ thể của đối tượng bệnh nhân này sẽ nhiều hơn so với bệnh nhân CRRT có tình trạng suy thận. Chưa có tài liệu nào chính thức khuyến cáo liều cho những trường hợp này, nên thường các nhà lâm sàng sẽ tự cân nhắc theo tình trạng lâm sàng của bệnh nhân và ước tính liều sử dụng sẽ cao hơn so với liều hiệu chỉnh CRRT thông thường. Chúng ta có thể ước tính độ thanh thải của bệnh nhân dựa vào các công thức trên và từ đó ước tính liều cần sử dụng. Tuy nhiên, sự ước tính này chỉ mang tính chất tương đối và không hoàn toàn chính xác. Phương pháp chính xác hiện nay là theo dõi nồng độ thuốc trong máu (TDM) và hiệu chỉnh liều theo nồng độ thuốc đo được. Tuy nhiên phương pháp TDM hiện tại chỉ áp dụng hạn chế 1 số thuốc như aminoglycoside, vancomycin, teicophanin do các thuốc này có khoảng trị liệu hẹp (cần thực hiện TDM ngay trên bệnh nhân thông thường).Việc thực hiện TDM ở bệnh nhân CRRT không suy thận là cần thiết tuy nhiên khó thực hiện do cơ sở y tế không đủ điều kiện khoa học kỹ thuật và tính khả thi về tài chính. Việc ước tính liều sẽ dựa vào độ thanh thải ước tính (ClCRRT + ClCr bảo tồn của bệnh nhân) và tình trạng lâm sàng của bệnh nhân, trong trường hợp cần thiết có thể dùng liều cao nhất khuyến cáo. Hơn nữa, một yếu tố rất quan trọng cần tính toán là đảm bảo đạt được thông số PK/PD của từng loại kháng sinh theo MIC của chủng vi khuẩn cấy được. Ví dụ, Vancomycin cần AUC/MIC ≥ 400 đối với MRSA để cho hiệu quả điều trị tốt nhất. Và khi hiệu chỉnh liều cũng cân nhắc yếu tố PK/PD nếu kháng sinh phụ thuộc thời gian thì khuyến cáo nên giữ nguyên liều đồng thời rút ngắn khoảng cách liều và kháng sinh phụ thuộc nồng độ thì nên tăng liều sử dụng, giữ nguyên khoảng cách liều.
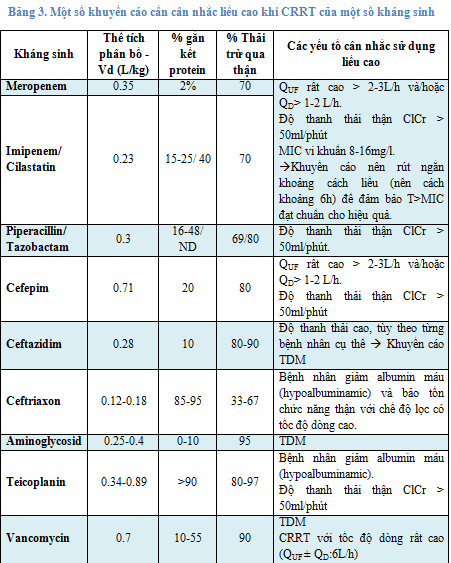
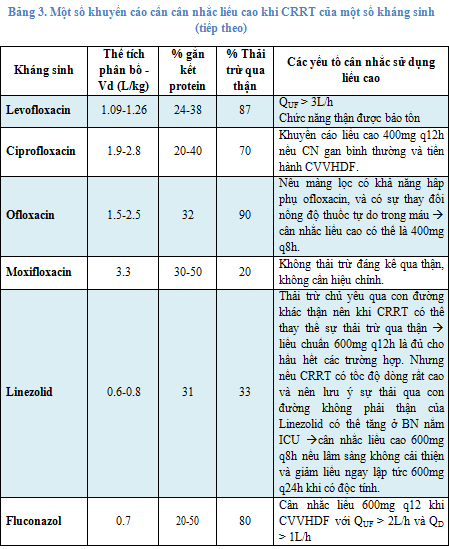
5. Kết luận
Chính thức chưa có tài liệu khuyến cáo toàn vẹn và chính xác về liều hiệu chỉnh khi bệnh nhân CRRT, đặc biệt là các trường hợp CRRT mà chức năng thận vẫn còn bảo tồn. Việc hiệu chỉnh sẽ dựa theo các tài liệu nghiên cứu trên từng nhóm bệnh nhân CRRT cụ thể nên thường không được khuyến cáo rộng rãi và chính thống. Vì vậy, khi nắm các nguyên tắc và các yếu tố ảnh hưởng đến thanh thải của bệnh nhân trong CRRT sẽ phần nào hỗ trợ nhà thực hành lâm sàng có đủ phương tiện để cân nhắc, ước tính và sử dụng liều trên bệnh nhân một cách hợp lý nhất có thể tùy theo tình trạng lâm sàng của từng cá thể người bệnh. Các vấn đề cần xem xét về liều kháng sinh trên bệnh nhân CRRT:
-
Những kháng sinh có độ thanh thải qua thận cao sẽ được loại thải qua CRRT (có hệ số lọc - SC cao) nên liều cần phải hiệu chỉnh (thường là tăng liều so với khi suy thận và IHD). Ngược lại, thuốc thường không thải qua con đường thận thì sẽ có ClCRRT thấp và không cần hiệu chỉnh liều so với khi chức năng thận bình thường.
-
Chỉ có dạng thuốc tự do mới dễ dàng bị loại thải qua CRRT, màng lọc “high flux” có thể loại được phức hợp phân tử đến 50.000 Da -> ước tính lượng thuốc được thải ra thường sử dụng tỷ lệ phần trăm thuốc tự do trong máu (giá trị này ko hoàn toàn chính xác, đo nồng độ thuốc mới là giá trị tin cậy).
-
Khi tiến hành CRRT thường có những nguyên tắc chung gần giống nhau về các đặc tính CRRT như quả lọc, QUF, QD áp dụng cho các đối tượng bệnh nhân. Nếu các yếu tố này không thay đổi, có thể ứng dụng các bảng liều (monogram) có sẵn được khuyến cáo -> hầu hết cho liều hiệu chỉnh tương đối chính xác. Hiện Bệnh viện Bệnh Nhiệt Đới cũng có bảng liều khuyến cáo cho bệnh CRRT dễ dàng và tiện lợi khi sử dụng. Tuy nhiên, cần phải lưu ý khi tiến hành CRRT với các đặc tính thay đổi so với bình thường ví dụ như QUF, QD rất cao (lên tới 6 L/h)-> bảng liều trên không phù hợp, thông thường sẽ cần liều cao hơn, thậm chí có thể cao hơn so với liều dùng cho bệnh nhân có chức năng thận bình thường.
-
Cần phải xem xét các yếu tố bệnh lý lâm sàng của bệnh nhân (tình trạng dịch, albumin máu, chức năng thận được bảo tồn …) ảnh hưởng đến dược động học của thuốc và sẽ làm thay đổi sự thanh thải của thuốc. Các bệnh nhân có chức năng thận được bảo tồn (đặc biệt là khi ClCr > 50ml/phút)-> cân nhắc sử dụng liều kháng sinh có thể cao hơn liều hiệu chỉnh thông thường ghi trong bảng liều có sẵn.
-
Việc hiệu chỉnh liều khánh sinh, đặc biệt là khi dùng liều cao cần phải tùy theo lâm sàng bệnh nhân và cân nhắc yếu tố nguy cơ - lợi ích cho bệnh nhân. Nên cân nhắc thông số PK/PD, MIC của vi khuẩn để vừa đảm bảo hiệu quả tốt nhất và hạn chế được độc tính của thuốc khi điều trị.
TÀI LIỆU THAM KHẢO
1. D. Kuang and C. Ronco, Adjustment of Antimicrobial Regimen in Critically Ill Patients Undergoing Continuous Renal Replacement Therapy, Intensive Care Medicine 2007: 592-606.
2. Federico Pea, et al. Pharmacokinetic considerations for antimicrobial therapy in patients receiving renal replacement therapy, Clinical Pharmakinetic2007; 46 (12): 997-1038.
3. Vũ Đình Thắng và cộng sự, Lọc máu liên tục – CRRT, Nhà xuất bản Y Học, 2013.
4. William H. Fissell, Antimicrobial dosing in acute renal replacement, Advance Chronic Kidney Diseases 2013 January; 20 (1).